肥胖和糖尿病瘦素抵抗小鼠肠道微生物群和内源性大麻素系统张力的改变:对脂肪组织中apelin调节的影响
- 1鲁汶药物研究所代谢与营养研究小组,Université鲁汶天主教,布鲁塞尔,比利时
- 2瑞士日内瓦日内瓦大学医院基因组研究实验室
- 3.荷兰瓦赫宁根大学微生物实验室
- 4INSERM U1048,第三小组,疾病研究所Métaboliques和心血管,Université Paul Sabatier, Université de Toulouse,图卢兹,法国
- 5鲁汶药物研究所生物活性脂类生物分析和药理学实验室,Université鲁汶天主教,布鲁塞尔,比利时
- 6赫尔辛基大学兽医生物科学系,芬兰赫尔辛基
- 7瑞士日内瓦日内瓦大学医院细菌学实验室
越来越多的证据支持肠道菌群在肥胖、2型糖尿病和低度炎症发展中的作用。脂肪组织的内分泌活动已被发现有助于调节葡萄糖稳态和低度炎症。在由该组织产生的关键激素中,apelin已被证明可以调节葡萄糖稳态。最近,有人提出肠道菌群通过内源性大麻素系统(eCB)和肠道菌群衍生化合物即脂多糖(LPS)参与脂肪组织代谢。我们研究了肥胖和糖尿病瘦素抵抗小鼠的肠道微生物群组成(db/db)通过结合焦磷酸测序和系统发育微阵列分析16S核糖体RNA基因序列。我们观察到厚壁菌门、变形菌门和纤维菌门的丰度显著较高db/db比较瘦的老鼠。基因型对10个属的丰度有显著影响。我们确定了eCB和LPS在遗传性肥胖和糖尿病小鼠apelin能系统调节(apelin和APJ mRNA表达)中的作用。通过使用在活的有机体内而且在体外在模型中,我们已经证明了eCB和低级别炎症在脂肪组织中差异地调节apelin和APJ mRNA的表达。最后,深层肠道菌群分析显示,2型糖尿病小鼠的肠道微生物群落与瘦小鼠有显著不同。这表明了肠道微生物群和平林能系统的调节之间的具体关系。然而,特定细菌在形成表型中的确切作用db/db老鼠还有待确定。
简介
肥胖和相关的代谢紊乱(如胰岛素抵抗、2型糖尿病和心血管疾病)与低度炎症状态密切相关(Olefsky和Glass, 2010).大量研究表明,在肥胖情况下,脂肪组织的内分泌活动和巨噬细胞浸润都参与了低级别炎症的发展(Olefsky和Glass, 2010).令人信服的证据支持脂肪因子参与调节葡萄糖稳态和低度炎症的观点(邓和Scherer, 2010;费德里科等人,2010).在最近发现的脂肪因子中,apelin被认为是一种新型的关键肽,参与多种生理功能的调节。Apelin和APJ mRNA在哺乳动物中广泛表达,并在中枢神经系统和外周发挥功能作用(Sorli et al., 2006).Apelin在心血管系统中起着关键作用,作用于心脏收缩力、血压、液体稳态、血管形成和细胞增殖(Maenhaut and Van, 2011).Apelin血清水平与啮齿动物和人类的营养状况和血浆胰岛素水平有关(Dray et al., 2008;Duparc等人,2011a).此外,与瘦人相比,肥胖受试者和高胰岛素血症肥胖小鼠的apelin血浆浓度增加(Dray et al., 2010).有趣的是,apelin已被证明通过amp -激酶和一氧化氮(NO)依赖机制来控制葡萄糖稳态(Dray et al., 2008;Duparc等人,2011).最近,有人提出炎症可能参与apelin的产生及其受体表达的调节(戴维等人,2006年;Han et al., 2008a,b).然而,apelin及其特异性G蛋白偶联受体APJ的调控机制尚未完全阐明。
越来越多的证据支持肠道菌群在肥胖、2型糖尿病、胰岛素抵抗和低度炎症发展中的作用(Backhed等人,2004年;Ley等人,2006年;Turnbaugh等人,2006年;Cani等人,2007a,2008,2009;马丁内斯等人,2009年;维杰-库马尔等人,2010).然而,肠道菌群的组成和存在于肠道中的微生物的确切作用仍然不明确。尽管如此,用于表征微生物多样性的非培养方法的进步有助于评估这一大群微生物在宿主代谢中的功能贡献(马丁等人,2008年;Turnbaugh等人,2009年).例如,最近的数据表明,肠道菌群组成和肠道屏障功能的变化在肥胖相关炎症的发展中起着关键作用(Brun等人,2007年;Cani et al., 2008,2009;De La Serre等人,2010).因此,我们提出肥胖相关的低级别炎症和脂肪生成过程可能与肠道微生物群有关,其机制涉及内源性大麻素系统(eCB)和细菌衍生的脂多糖(LPS;Cani等人,2007a,b,2008,2009;De La Serre等人,2010;穆奇奥利等人,2010年).
eCB系统由内源性脂质组成,激活特定的G蛋白偶联受体,称为大麻素受体1和2 (CB1和CB2).在这些脂质中,N-花生四烯酮酰乙醇胺(anandamide, AEA)和2-花生四烯酮酰甘油(2-AG)研究最多(兰伯特和穆奇奥利,2007年).AEA和2-AG都广泛存在于全身,它们的组织水平由合成和灭活之间的平衡调节。简单地说,N-酰基磷脂酰乙醇胺(NAPEs)是AEA的前体N-酰基磷脂酰乙醇胺选择性磷脂酶d (NAPE-PLD),而2-AG主要通过二酰基甘油脂肪酶(DAGL;Muccioli 2010).令人信服的有力证据表明,内源性大麻素水平的严格控制失调可能导致病理情况,如肥胖和相关代谢综合征或神经障碍(兰伯特和穆奇奥利,2007年).负责其降解的主要酶是脂肪酸酰胺水解酶(FAAH;Cravatt等人,1996年)和单酰甘油脂肪酶(MGL;Dinh等人,2002年),分别。肥胖和2型糖尿病与更强的eCB系统张力相关(NAPE-PLD、CB1mRNA和血浆或脂肪组织中较高的eCB水平;穆奇奥利等人,2010年).此外,已知LPS可刺激eCB的合成(Liu et al., 2003;穆奇奥利等人,2010年),而肠道菌群参与这一复杂的调节(穆奇奥利等人,2010年).
虽然肥胖小鼠肠道菌群的变化(ob/ob)或高脂肪饮食引起的肥胖小鼠明显(Ley等人,2005年;Cani等人,2007a,b;Turnbaugh et al., 2008,2009;Hildebrandt等人,2009年)、二型糖尿病小鼠肠道菌群的确切组成(db/db)仍然未知。鉴于这些最新发现,我们还决定研究这三个关键参与者(eCB、LPS和肠道微生物群)在脂肪组织中apelin和APJ表达调控中的潜在意义。因此,我们结合多种分子方法,包括条形码焦磷酸测序和16S核糖体RNA (rRNA)基因的系统发育微阵列分析,比较遗传肥胖和糖尿病小鼠与其瘦仔鼠的肠道微生物群落。本文的数据表明,apelin和APJ的表达在生理条件下被eCB下调,而在病理条件下被细菌来源的复合物LPS上调。此外,肠道菌群分析揭示了肠道菌群与apelinergic系统调节之间的特定关系,以及对宿主代谢至关重要的潜在新细菌靶点。
材料与方法
老鼠
六个db/db老鼠或瘦弱的同窝动物(n= 6 /组;C57BL/6背景,jackson实验室,Bar Harbor, ME, USA)被安置在受控环境中(日光周期12小时,下午6点熄灯),每组2只小鼠/笼。两组小鼠都免费获得类似的对照饮食(A04, Villemoisson sur Orge,法国)和自来水,持续1周。
所有小鼠实验均经当地伦理委员会批准并按照其指导方针进行。比利时1993年11月14日关于保护实验动物的法律规定了住房条件(协议号LA1230314)。
组织抽样
7周龄小鼠空腹5h后腹腔注射氯胺酮100 mg/kg和甲苯嗪10 mg/kg麻醉。采集血样作进一步分析。颈椎脱位处死小鼠。皮下脂肪沉积被解剖,立即浸泡在液氮中,并保存在−80°C下进行进一步分析。
等离子体组织Apelin
根据制造商的说明,使用Apelin EIA试剂盒(Phoenix多肽)测量Apelin。
Anandamide (AEA)组织水平测定
组织在CHCl中均质3.(10毫升),氘化标准品(d-AEA;加入200 pmol)。甲醇(5ml)和H2加入O (2.5 ml),然后通过剧烈混合提取脂质。离心后,有机层被回收,在氮流下干燥2并用二氧化硅固相萃取纯化,然后用乙酸乙酯-丙酮(1:1)溶液洗脱(穆奇奥利和斯特拉,2008年;穆奇奥利等人,2010年).使用LTQ Orbitrap质谱仪(Thermo Fisher Scientific)耦合Accela HPLC系统(Thermo Fisher Scientific)对所得的脂质部分进行HPLC - ms分析。分析物分离采用C-18 Supelguard预色谱柱和Supelcosil LC-18色谱柱(3 μM, 4 × 150 mm;Sigma-Aldrich)。流动相A和B由MeOH-H组成2o -乙酸75:25:10 .1 (v/v/v)和meoh -乙酸100:0.1 (v/v)。梯度(0.5 ml/min)设计如下:在15分钟内线性从100% A过渡到100% B,然后在100% B处线性过渡10分钟,然后在100% A处重新平衡。我们使用APCI电离源在正模式下进行质谱分析。毛细管和APCI蒸发器温度分别设置为250°C和400°C。用同位素稀释法定量了Anandamide,使用各自的氘化标准,保留相同。所生成的校正曲线如先前所述(穆奇奥利和斯特拉,2008年),数据按组织样本权重归一化。
小鼠盲肠DNA的分离
采集小鼠盲肠内容物事后剖析储存在−80°C。从盲肠内容物中提取宏基因组DNA (5db/db根据制造商的说明,使用QIAamp DNA Stool Mini试剂盒(Qiagen, Hilden, Germany)。由于技术原因,两个盲肠内容物未被纳入进一步的肠道微生物区系分析。
16S RRNA基因扩增及测序
对于每个样本,我们扩增了对应的细菌16S rRNA基因V1-3区域大肠杆菌16S rRNA基因位置28-514,不包括引物序列。pcr包括50×稀释纯化DNA 1 μl,正向B-8fhomd (5 ' -gccttgccagcccgctcag-) 0.5 μM交流- gagtttgatcmtggctca G-3 '), 0.05 μM的正向B-8f-Bifido (5 ' -gccttgccagcccgctcag-交流- agggttcgattctggctcag -3 ')和0.5 μM的条形码反向a - 534rhomddega引物(5 ' - gcctccctcgcgccatcagg - nnnnnnn -在-CCGCGGCTGCTGGCAC-3 ')添加至PrimeStar HS Premix (Takara)中。这些引物包括(i) 454个生命科学19碱基适配器A(小写下划线)或B(小写素色);(ii)八碱基样本特异性条形码序列(NNNNNNNN;编号692-701哈马迪等人(2008);表A1);(iii)宽范围16S正向或反向引物的序列(大写);以及(iv)在16S引物和条形码序列之间引入的二核苷酸序列(小写斜体),旨在防止不同条形码与rDNA靶标配对。
pcr在98°C持续10秒,56°C持续15秒,72°C持续1分钟的条件下进行29个循环。使用DNA1000实验室芯片在Agilent 2100生物分析仪上运行一微升的样品以确认合适的大小。用QIAquick PCR纯化试剂盒(Qiagen)对两个重复反应进行聚合和清洗。DNA浓度用NanoDrop 1000分光光度计测定。将每个纯化样品的100纳克汇集在基因组测序FLX系统(Roche)上进行测序。
与几个不相关项目相关的条形码16S rDNA扩增子被包括在相同的测序运行中。共有39548个阅读,质量评分<20,对应于盲肠的本研究中展示的10只小鼠的样本。
信息化分析
除去含有未命名碱基、不正确引物序列或≥10个相同核苷酸的序列。读取16S rDNA正向寡核苷酸序列CCGCGRCTGCTGGCGC,在3 '端倒数第二个位置包含G而不是A,可能是由于引物合成或测序伪效应(Lazarevic等人,2010),如果满足其他质量标准,则不会从数据集中删除。修剪引物序列后,读取<200或>290 nt和那些不完全覆盖的引物序列大肠杆菌16S rRNA基因位置288-514,使用RDP焦磷酸测序工具确定科尔等人,2009年),被丢弃,留下31577个序列。使用MG-RAST服务器检查序列是否存在潜在的嵌合体(梅耶等人,2008年).
利用CD-HIT将序列以97%的同源性(97%- id phylotypes)分配给代表性的系型(Huang等,2010).97% id系型之间的距离以MUSCLE对齐(埃德加,2004)以FastTree (Price等人,2009年).采用UniFrac (Lozupone等人,2006).使用RDP分类器(王等,2007),建议置信度下限为50%。这些序列(31,577次读取)在MG-RAST存储库(梅耶等人,2008年)。
MITChip: PCR引物和条件
小鼠肠道芯片(MITChip)是一种系统发育芯片,由3580种不同的寡核苷酸组成,专门用于小鼠肠道菌群(Derrien et al., in preparation)。MITChip的设计和分析都是按照前面描述的对人类芯片进行的(Rajilic-Stojanovic等人,2009).简而言之,使用盲肠DNA提取物20 ng,用引物扩增16S rRNA基因T7prom- bact -27 for (5 ' -T GAATTGTAATACGACTCACTATAGGGgtttgatcctggctcag-3 ')和uni1492 -rev (5 ' -CGGCTACCTTGTTACGAC-3 ')。随后,一个在体外用Cy3和Cy5染料进行转录和标记。将Cy3/ cy5标记的目标混合物破碎,然后在62.5°C的旋转烤箱中杂交16小时(Agilent Technologies, Amstelveen,荷兰)。扫描前将玻片清洗干燥。信号强度数据从微阵列图像使用安捷伦特征提取软件,版本9.11.使用一组基于r的脚本进行微阵列数据归一化和进一步分析2结合定制设计的关系数据库,该数据库在MySQL数据库管理系统下运行3..
RNA制备及实时QPCR分析
使用TriPure试剂(Roche)从组织中制备总RNA。在Agilent 2100生物分析仪(Agilent RNA 6000 Nano Kit, Agilent)上运行每个样品1 μl,对总RNA进行定量和完整性分析。cDNA通过逆转录系统试剂盒(Promega, Leiden, Netherlands)对1 μg总RNA进行逆转录制备。使用StepOnePlus进行实时pcr™实时PCR系统和软件(应用生物系统公司,Den Ijssel,荷兰)使用Mesa Fast qPCR™(Eurogentec, Seraing, Belgium)根据制造商的说明进行检测。选择RPL-19 RNA作为管家基因。RPL-19、IL-1、F4-80、CD68、MCP-1、TNF-α、Apelin、APJ、CB1、MGL、FAAH和NAPE-PLD的引物序列先前已被描述(Cani et al., 2008,2009;Dray et al., 2008;Muccioli 2010).CD11c引物序列为f - acg - tca - gta - cata - gga - gat - gtt - gga和r - atc - cta - ttg - cagg - aat - gct - tct - tta - cc。所有样品在一个96孔反应板中重复运行,数据根据2−ΔCT方法。通过扩增结束时的熔解曲线分析,验证扩增产物的性质和纯度。
脂肪组织移植培养
精确解剖10只C57BL/6J(野生型瘦)小鼠皮下脂肪库,去除所有可见血管、颗粒和结膜组织。然后用剪刀将脂肪组织剪成小块(4毫米)3.),混合后置于含2% (w/v)不含脂肪酸BSA、青霉素(100 IU/ml)、链霉素(100 μg/ml)和两性霉素B (2.5 μl/ml;英杰公司)。将250mg脂肪组织用磷酸盐缓冲盐水冲洗,并在100mm含有10ml MEM的培养皿中培养,培养皿中加入Earle’s盐(Invitrogen),其中添加0.5%不含脂肪酸的BSA、青霉素(100iu /ml)、链霉素(100 μg/ml)和两性霉素B (2.5 μl/ml;英杰公司)。所有条件在四到五个不同的盘子中重复(n= 4 - 5)。培养皿在37°C的5% CO中培养24小时2的气氛。新鲜培养基中葡萄糖的基础浓度为5 mmol/l,而皮质醇和胰岛素的基础水平极低(分别为~ 0.5 nmol/l和3 pmol/l)。根据实验方案,以不同的组合方式使用不同的药理制剂。有限合伙人(大肠杆菌055:B5, 100 ng/ml, Sigma)和HU-210 (100 nM, Tocris)在DMSO中稀释,也作为对照。细胞活力在实验过程中没有变化(数据未显示)。在实验结束时,脂肪材料在磷酸盐缓冲盐水中冲洗,收集,立即在液氮中冷冻,并在−80°C保存,直到后续的mRNA分析。
统计分析
数据以均数±标准差表示。两组之间的差异是使用未配对的双尾学生的评估t以及。细菌群落的统计比较使用双尾学生进行t -检验,将方差视为等效。相关性分析采用Pearson相关系数。使用GraphPad Prism版本5.00 for Windows (GraphPad Software, San Diego, CA, USA)和JMP 8.0.1 (SAS Campus Drive, Cary, NC, USA)分析数据。结果被认为有统计学意义P< 0.05。
结果
肥胖和糖尿病小鼠与瘦小鼠肠道细菌16S RRNA分析
肥胖(ob/ob)小鼠和饮食诱导肥胖小鼠的特征是肠道微生物群的组成发生了改变(Ley等人,2005年;Cani等人,2007a,b;Turnbaugh et al., 2008,2009).迄今为止,瘦素抵抗性肥胖和2型糖尿病患者肠道微生物群的组成(db/db)小鼠从未被报道过。两者的主要区别ob/ob而且db/db老鼠首先处于瘦素系统中,ob/ob小鼠缺乏瘦素ob基因),而db/db小鼠具有瘦素抵抗性(中枢神经系统改变了它们的“瘦素受体”),其次,从表型上看,这两只小鼠都是嗜食、严重肥胖和脂肪肝。然而,db/db小鼠在出生后(几周)就患上了2型糖尿病。这两个模型之间的主要区别是db/db小鼠在研究肠道菌群在这种表型中的作用方面具有明显的优势。在这个肥胖和糖尿病模型中,肠道微生物群的确切组成仍然未知。因此,我们对肥胖和糖尿病患者的肠道菌群组成进行了特征分析db/db通过两种互补的方法:焦磷酸测序和系统发育微阵列分析从小鼠盲肠样本中分离的16S rRNA基因。
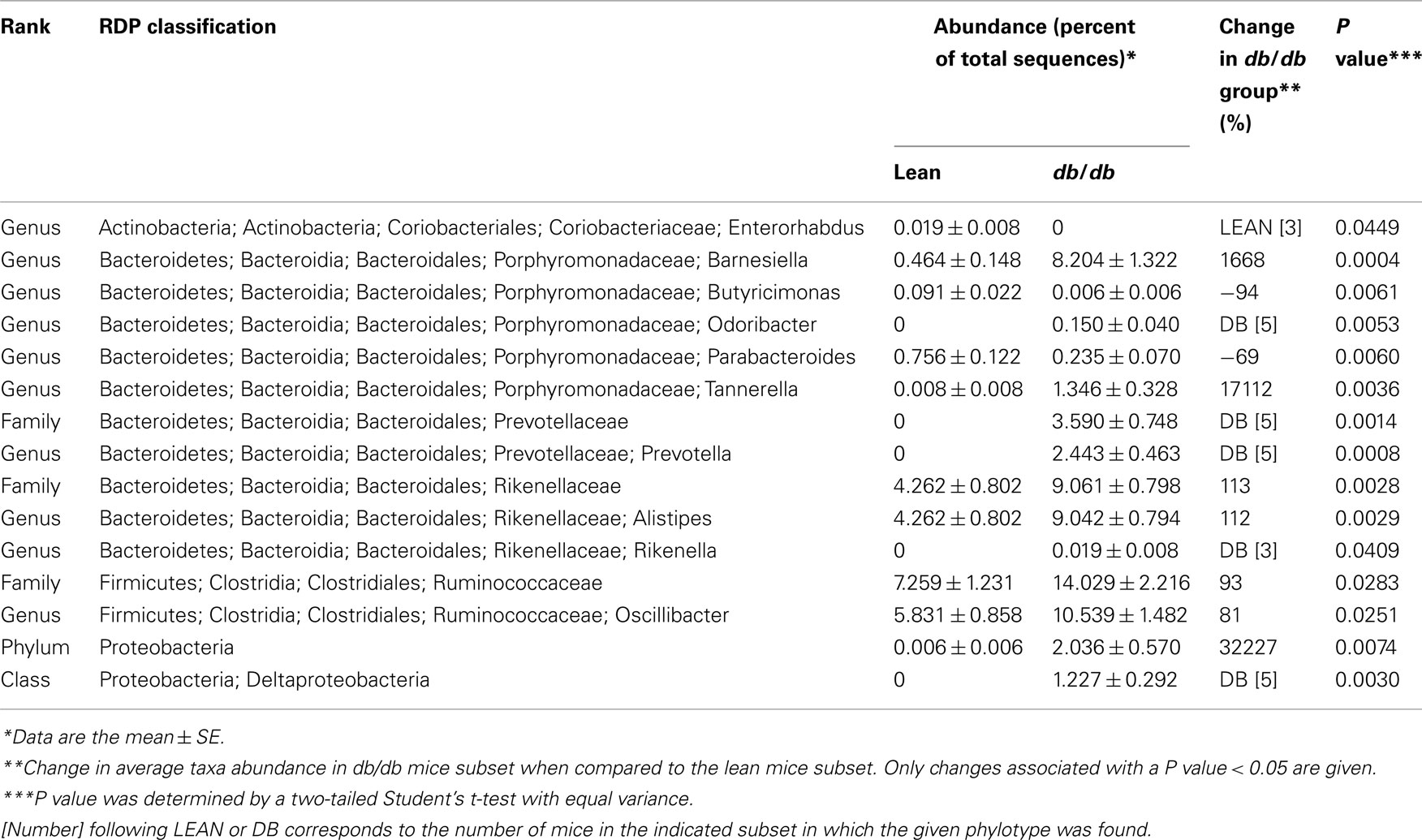
为了探索盲肠样本中的细菌多样性,我们以16S rDNA高变区V3为目标。共有31,577个序列读取通过了所有质量控制步骤。我们观察到Proteobacteria的显著增加(32,227%)db/db与瘦老鼠相比(表1).基因型对10个属的丰度有显著影响1).有趣的是,属Odoribacter,普氏菌,Rikenella只在db/db组,而Enterorhabdus仅在瘦弱小鼠中被识别(表1).重要的是,丰富的Tannerella属增加了约17,112%db/db老鼠。三角洲变形杆菌纲的代表和拟杆菌门的三个属的代表,都是在db/db小鼠,是革兰氏阴性细菌。表A2在附录中显示了96种系统类型(定义为97% id)中富集或缺失的显著差异db/db老鼠。此外,UniFrac的分析结果(Lozupone等人,2006)清楚地显示db/db盲肠群落之间的相似性比对照组瘦小鼠的群落更大(图1A).基于unifrac的群落结构两两比较的主坐标分析(PCoA)显示了两种饲料条件对应的两个聚类(图1B).重要的是,我们发现属之间有显著的正相关关系Oscillibacterapelin和APJ的表达(r= 0.88,P= 0.0006,和r= 0.87,P= 0.0011)。我们还使用MITChip进行了深度和全球微生物区系分析,这是一种高通量系统发育微阵列,设计于人类对应的(Rajilic-Stojanovic等人,2009),之前与454焦磷酸测序(克莱森等人,2009年).通过对超过3500个寡核苷酸探针进行杂交,获得盲肠菌群的剖面,并可视化所有目标操作分类单位(OTUs)的存在或不存在。MITChip分析显示两个治疗组有明显的单独聚类(图2C,D)相似度为81.2(±2.6)% (Pearson积矩相关系数)。我们观察到拟杆菌门和脱铁杆菌门的相对丰度和绝对丰度较低db/db与瘦组小鼠相比(图2A,B,D),而我们发现丰度较高的厚壁菌门,变形菌门和纤维菌门db/db与瘦组小鼠相比(图2A, B, D)。根据焦磷酸测序分析,两组均以基因型特异性的方式聚类。除了焦磷酸测序分析中观察到的特定变化外,我们还在较低的分类水平上发现了一些以前未识别的修改,特别是的绝对和相对增加普氏菌Spp .(未显示)。

图1。通过16S rRNA焦磷酸测序分析肥胖糖尿病小鼠和瘦小鼠肠道细菌群落.(一)基于未加权UniFrac分析和97% id系统分型,对两个测试组的小鼠盲肠微生物群落进行聚类。红色为糖尿病小鼠(db/db),蓝色代表瘦弱的老鼠。分支长度表示UniFrac单元中环境之间的距离,由比例尺(n= 5 /组)。(B)基于UniFrac非加权(存在/不存在)分析和97% id系统型的PCoA分析。代表单个样本的每个符号(填充的圆圈或填充的正方形)根据饮食条件着色:红色对应db/db,蓝色代表lean (n= 5 /组)。
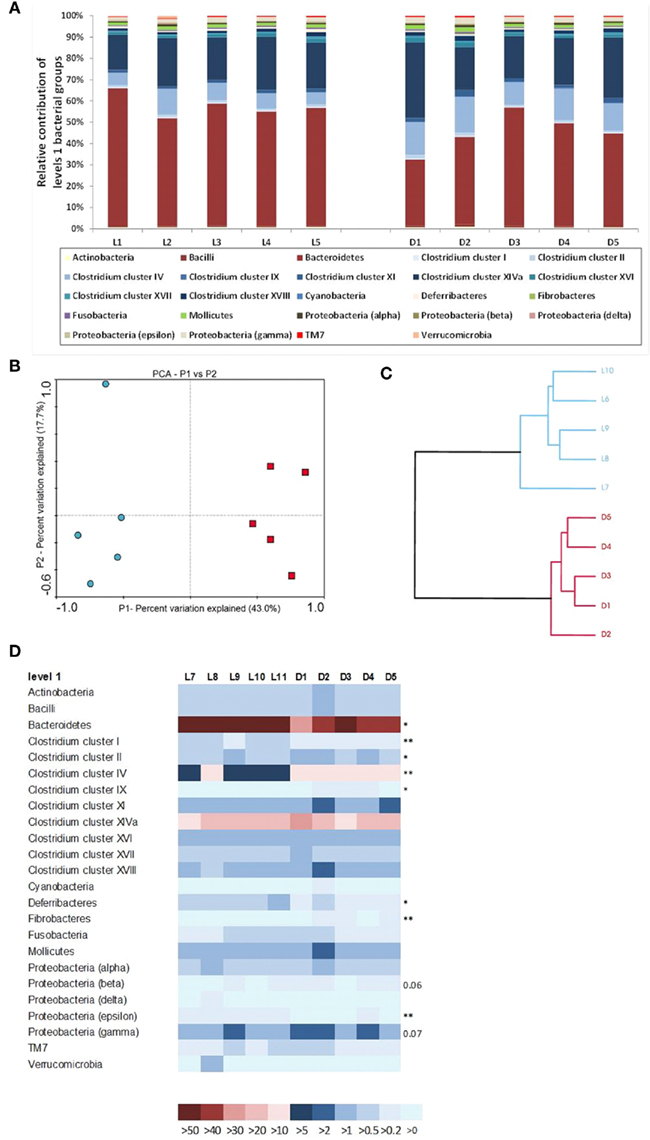
图2。肥胖糖尿病小鼠或瘦小鼠肠道细菌群落的系统发育微阵列分析.(一)每个群落的百分比由指示的1级细菌群。(B)基于MITChip系统发育指纹的肠道菌群PCoA分析,来自盲肠内容物db/db还有瘦弱的老鼠。(C)分层聚类可视化系统发育MITChip指纹的相似性。样本基于Pearson相关进行层次聚类。(D)不同种类细菌的相对丰度以总探针信号的百分比表示(n= 5 /组)。*P< 0.05, **P< 0.01由双尾学生决定t以及。
肥胖和糖尿病小鼠在脂肪组织中表现出较高的内源性大麻素系统张力
我们之前已经证明,肠道菌群在生理和病理情况下都有助于调节脂肪组织中的eCB系统张力(穆奇奥利等人,2010年).此外,人类和啮齿动物肥胖的特征是较高的eCB系统张力(Engeli等人,2005年;Bluher等人,2006;马蒂亚斯等人,2006年;Cote et al., 2007;D 'Eon et al., 2008;Starowicz等人,2008年;伊佐等人,2009年;穆奇奥利等人,2010年).与这些发现一致的是,我们发现db/db喂食标准饮食的小鼠表现出增加的eCB系统张力(AEA水平和mRNA表达)。叫花生四烯酸乙醇胺(AEA);Devane等人,1992年)是内源性CB1和CB2配体。在这里,我们发现脂肪组织中AEA水平显著增加(约50%)(图3.A).根据这一结果,NAPE-PLD和CB1mRNA表达显著增加,而aea降解酶FAAH的mRNA表达降低(图3.B, C, D)。值得注意的是,降解内源性大麻素2-花生四烯油酰甘油(2-AG)的主要酶单酰甘油脂肪酶(MGL)在小鼠脂肪组织中的表达趋于升高db/db老鼠(图3.E),这与脂肪组织中观察到的2-AG水平降低相一致(图3.F).总而言之,这些数据第一次证明db/db小鼠在脂肪组织中显示出改变的eCB系统色调,更具体地说,它们显示出内源性大麻素AEA信号的增加。
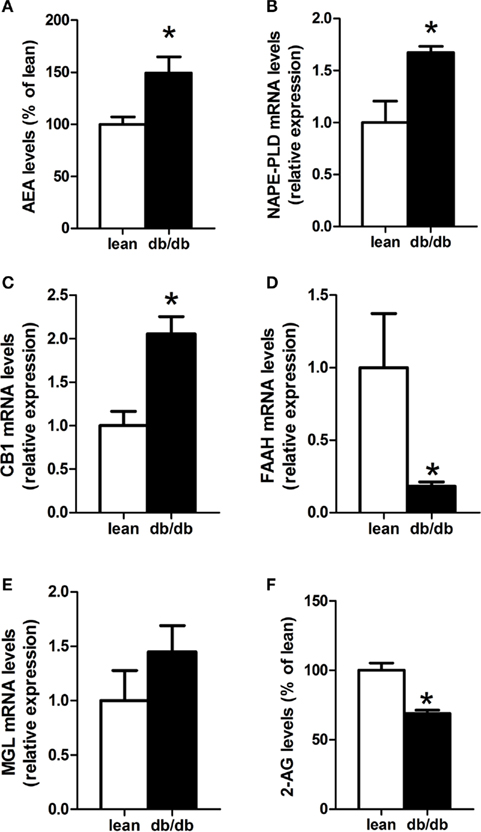
图3。脂肪组织中较高的内源性大麻素系统db/db老鼠.(一)ae组织含量(精瘦百分比),(B)NAPE-PLD,(C)CB1,(D)FAAH;(E)MGL mRNA表达(F)测定脂肪组织中2-AG组织含量(精瘦百分比)。均值±SEM,n= 6/group, *P< 0.05由双尾学生的结果确定t以及。
肥胖和糖尿病小鼠脂肪组织Apelin和APJ表达增加
最近的证据表明,在病理生理条件下(肥胖和2型糖尿病),外周无鳞胺能系统似乎被解除调控(Dray et al., 2008,2010;Duparc等人,2011a).迄今为止,肥胖和糖尿病小鼠脂肪组织中apelin和APJ表达的调控机制尚不完全清楚。因此,我们在该模型中研究apelin能系统tone,发现apelin和APJ mRNA水平在大鼠脂肪组织中分别显著增加了2倍和3倍db/db与瘦弱的同窝同伴相比(图4A、B)。血浆apelin增加约30%,但未达到显著性(db/db: 7.1±1,精瘦:5.8±0.8 pg/ml)。
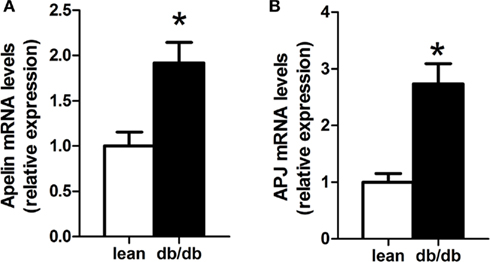
图4。脂肪组织apelin和APJ mRNA表达增加db/db老鼠.(一)组织Apelin和(B)脂肪组织中APJ mRNA表达的测定。均值±SEM,n= 6/group, *P< 0.05由双尾学生的结果确定t以及。
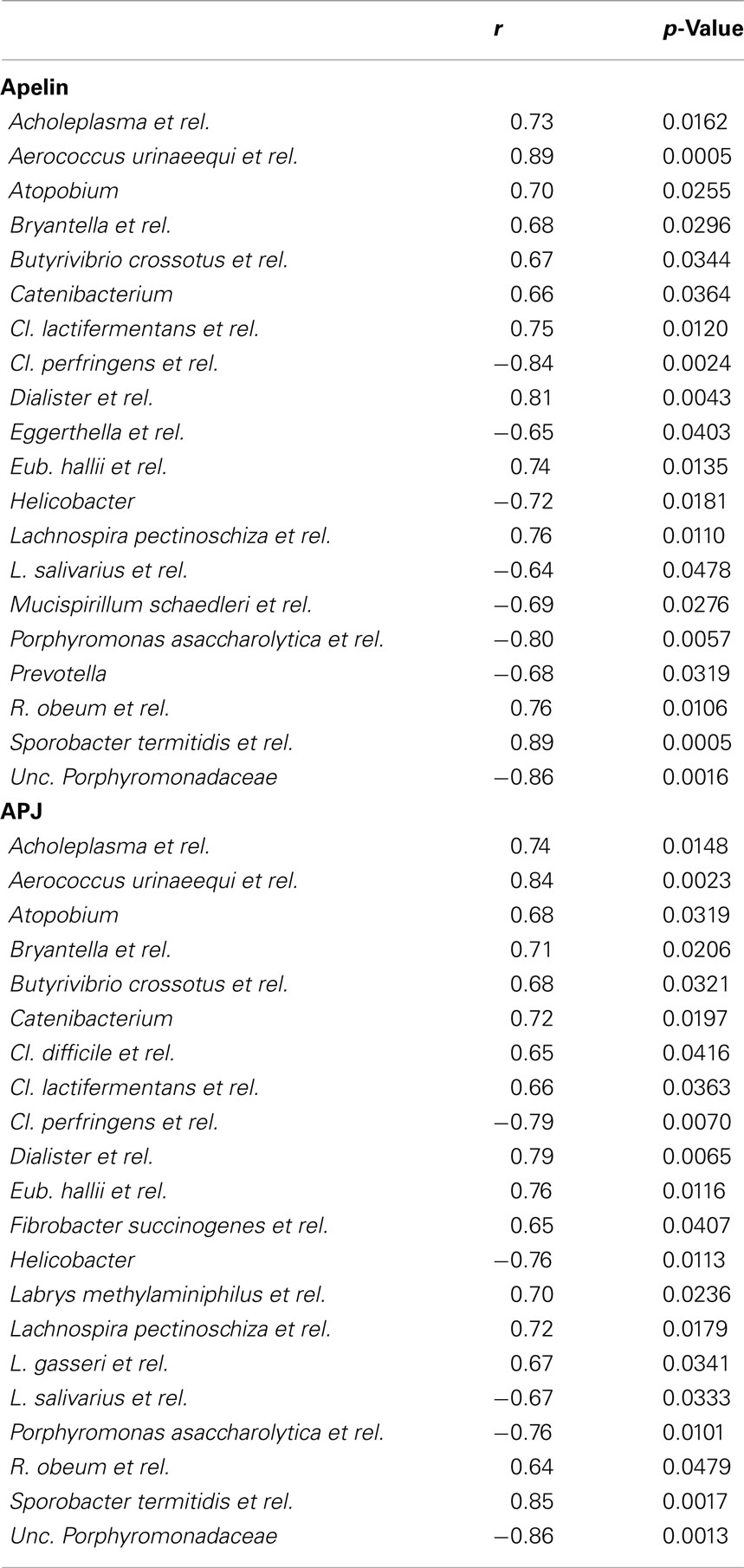
有趣的是,我们发现特定细菌的丰度与apelin/APJ表达之间存在一些正相关和负相关,这表明特定肠道细菌与apelin能系统的调节之间存在潜在的关系(表2)2).
db/db小鼠脂肪组织低级别炎症增加
我们之前已经证明,在肥胖和糖尿病小鼠的脂肪组织中观察到的较高的eCB系统张力直接依赖于低级别炎症张力(穆奇奥利等人,2010年).此外,db/db小鼠被认为是一种广泛使用的模型,用于研究与肥胖和2型糖尿病相关的代谢特征。这些小鼠的特征是低级别炎症,血浆LPS水平较高,血浆IL-1β、IL-6、TNF-α和INF-γ水平显著升高(Brun等人,2007年).此外,脂肪组织炎症的评估显示,与促炎巨噬细胞相对应的冠状结构数量增加,这些细胞为F4/80和CD11c阳性(Mihara et al., 2010;赫尔曼等人,2011年).与之前许多研究该模型中元炎症的报告一致,我们发现在我们的细胞中炎症和巨噬细胞浸润标记物显著增加db/db老鼠。在本研究中研究的标志物(IL-1,单核细胞趋化蛋白-1 (MCP-1), F4/80, CD11c和CD68 mRNA表达)都显著增加了50 - 400%db/db与瘦老鼠相比(图5a e)。
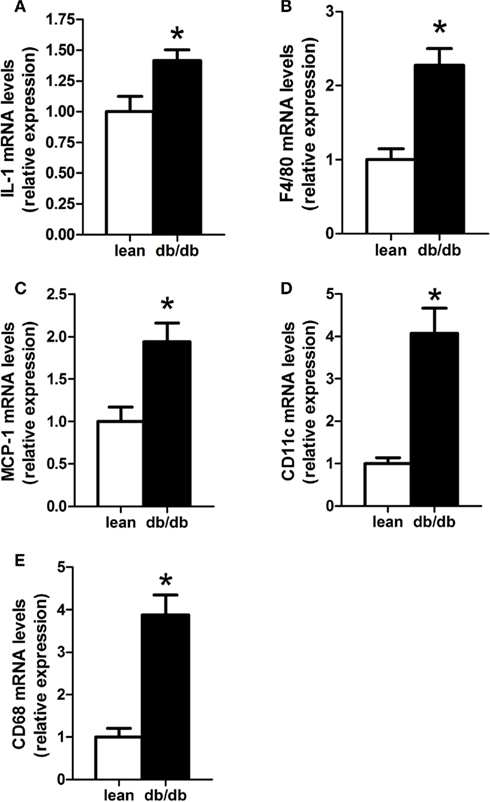
图5。脂肪组织炎症标志物增加db/db老鼠.(一)il - 1,(B)F4/80,(C)MCP-1,(D)CD11c,(E)测定脂肪组织中CD68 mRNA的表达。均值±SEM,n= 6/group, *P< 0.05由双尾学生的结果确定t以及。
eCB系统和低级别炎症均参与脂肪组织Apelin和APJ表达的调节
了解改变无鳞胺能系统的分子机制对于找到调节脂肪组织代谢的假定新靶点是至关重要的。我们之前已经证明,在肥胖和相关疾病中观察到的低级别炎症张力和较高的eCB系统张力都可能与肠道菌群组成有关(Cani et al., 2009;穆奇奥利等人,2010年;Cani和Delzenne, 2011).更重要的是,先前已经证明炎症同时调节apelin和APJ mRNA的表达(戴维等人,2006年;Melgar-Lesmes等人,2011).此外,我们的在活的有机体内实验和多重相关分析表明炎症与apelinergic系统的调节之间存在联系(图A1).然而,这些参数与脂肪组织apelin和APJ表达的调节之间的因果关系仍有待证实。
考虑到难以破译低级别炎症(即血浆LPS或细胞因子)和eCB系统张力对apelinergic系统的影响在活的有机体内,我们决定探索这些机制在体外培养脂肪组织外植体。值得注意的是,这些外植体来自健康、瘦弱的C57BL/6小鼠,使我们能够研究生理或病理样情况,即eCB系统的张力调节伴或不伴炎症情况。
在这里,我们发现大麻素受体激动剂(HU-210)对eCB系统的激活显著降低了apelin和APJ mRNA的表达(图6A、B)。与使用大麻素受体激动剂获得的结果一致在体外在瘦的野生型小鼠中,我们发现在活的有机体内通过给药有效FAAH抑制剂抑制AEA降解(URB597;Kathuria等人,2003年)显著降低apelin和APJ mRNA的表达(图A2).这些数据支持了eCB系统在生理状态下下调平胺能系统的观点。然而,我们发现低剂量LPS显著增加了这两个标记物。更重要的是,用大麻素受体激动剂和LPS处理的脂肪组织外植体表现出apelin和APJ mRNA表达的显著增加(图6A、B)。综上所述,这组实验表明eCB系统和低级别炎症张力均参与脂肪组织apelin和APJ的调节。有趣的是,eCB激动剂和LPS的同时刺激导致了平苷能系统的上调。同时,我们发现两个关键的炎症标志物(IL-1和TNF-α)在LPS-eCB治疗后同样上调(图)6C, D)。这些数据进一步证实:(i)在肥胖和2型糖尿病患者的情况下,eCB系统和低级别炎症都可能过度活跃,(ii) LPS和/或炎症在apelinergic系统的调节中起着总开关的作用。
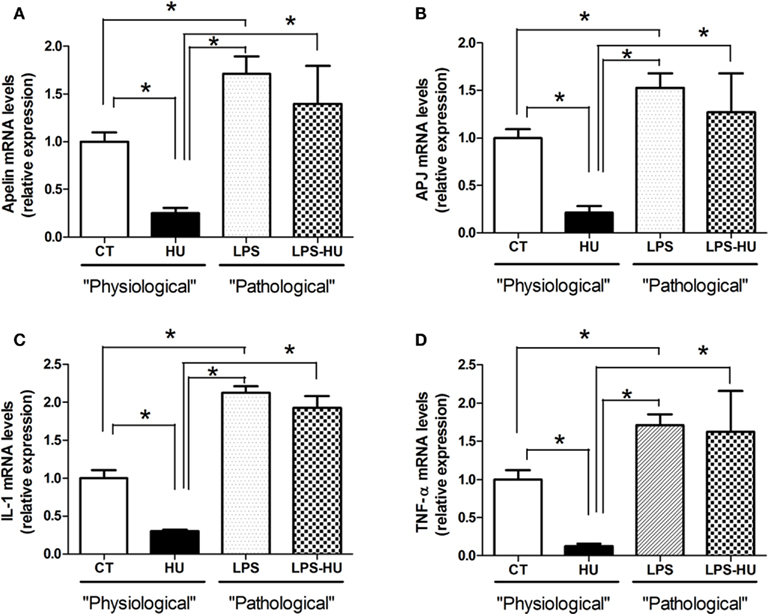
图6。在脂肪组织外植体培养中,eCB系统下调lps诱导的炎症(IL-1和TNF-α mRNA表达)和apelin能系统(apelin和APJ mRNA表达).mRNA表达水平(一)组织Apelin,(B)已,(C)il - 1,(D)暴露于载物(CT)、LPS (LPS)或大麻素受体激动剂HU-210 (HU;100 nM)单独或与LPS联合使用(100 ng。ml, LPS-HU) 24 h。*表示P药效< 0.05;一个双尾学生的t以及。
讨论
这项研究为2型糖尿病患者肠道菌群的改变提供了新的证据,与脂肪喂养无关。事实上,我们证明了肠道微生物群落受到基因型的深刻影响,而不一定是饮食db/db与同窝的小鼠相比,小鼠的肠道菌群组成发生了深刻的变化。此外,我们发现一些类群在糖尿病小鼠中存在或不存在。这些重要的发现质疑了这些细菌在表征该模型的表型改变发生时的潜在影响。尽管微生物群分析依赖于互补技术和分类方法,但数据显示了细菌群落特定聚类的相似模式。我们观察到拟杆菌门丰度下降,厚壁菌门丰度增加。重要的是,我们发现变形菌门在焦磷酸测序方法后急剧增加。此外,已鉴定出10个丰度受基因型显著影响的属。有趣的是,我们发现了几个革兰氏阴性细菌类群,它们的频率显著较高或仅在db/db老鼠。由于来自革兰氏阴性细菌的LPS引发了低级别炎症,并刺激了apelin和APJ的表达,我们假设这些特定的变化有助于在病例中观察到的表型db/db与苗条的老鼠相比。除了假定肠腔内LPS含量较高外,以前已经表明db/db小鼠的特点是更大的肠道炎症和肠道通透性(Brun等人,2007年;Duparc等人,2011).因此,除了以该小鼠模型为特征的瘦素作用的功能障碍外,我们提出,观察到的肠道微生物群落的变化也有助于在大肠杆菌中发现的复杂表型的发展db/db老鼠。然而,考虑到这些修饰的复杂性和发现的相关性数量,一个或多个特定类群与影响宿主生理的变化之间的直接联系仍有待研究。因此,需要进一步的工作来了解肠道细菌的代谢/分解代谢活动与其对宿主代谢的影响之间的功能联系。例如,在无菌条件下研究这种遗传模型,以确定肠道微生物对2型糖尿病发病的具体影响,这将是有趣的。重要的是,当我们将焦磷酸测序的分类结果与系统发育微阵列的分类结果进行比较时,我们观察到更多的差异归因于对系统发育微阵列的深入分析(<0.1%的群落;Rajilic-Stojanovic等人,2009)比焦磷酸测序。最近,454焦磷酸测序评估了不同引物的使用影响,并可能影响微生物分析(van den Bogert等人,2011),值得注意的是,深度焦磷酸测序和系统发育微阵列提供了类似的生物学结论,尽管分类可能与先前报道的系统不同(克莱森等人,2009年).
本研究还提供了新的机制,涉及eCB和低级别炎症强度在调节一种特定脂肪因子及其受体apelin和APJ中的重要作用。因此,多重相关分析表明,特定肠道微生物与apelin和APJ mRNA呈正相关或负相关。该研究还支持将高通量培养独立方法与生理评估相结合,以确定肠道微生物群落与宿主代谢之间的关系。然而,考虑到这些生物系统的复杂性,一个或多个细菌群与影响宿主生理的变化之间的直接联系仍有待证实。
在过去的几年里,大量的研究已经证明了能量代谢和周围apeelin作用之间的明确关系。在病理生理条件下,外周无鳞胺能系统似乎不受控制(Dray et al., 2008,2010;Duparc等人,2011a).一些研究人员发现,肥胖糖尿病患者和小鼠的血浆apeelin水平升高(海诺宁等人,2005年;Dray et al., 2008)及处于胰岛素抵抗状态(索里格尔等人,2009),其他研究表明,2型糖尿病患者的血浆apeelin水平降低(Erdem等人,2008).最近,胰岛素抵抗的严重程度可能会影响apelin和APJ表达的调节(Dray et al., 2010).
在这项研究中,我们首先证明了eCB系统音调的增加(更高的AEA水平,NAPE-PLD和CB)1脂肪组织中FAAH的表达和低表达)db/db老鼠。在这里,我们首次表明脂肪组织中的AEA水平增加,这与我们之前的发现一致(穆奇奥利等人,2010年).同时,我们发现apelin和APJ的表达均显著增加。通过使用多重相关分析,我们观察到eCB系统和尾线能系统之间存在非常强的关系,支持eCB系统在尾线能色调中的潜在含义。然而,db/db小鼠还具有较高的炎症张力(Brun等人,2007年),根据我们的结果,apelin/APJ与apelin/APJ呈正显著相关。考虑到db/db小鼠也表现出较好的eCB系统张力和炎症反应,我们研究了内源性大麻素的直接影响。为了澄清这一问题,我们在抑制FAAH后增加了瘦弱小鼠脂肪组织中的内源性AEA水平(穆奇奥利等人,2010年),主要的亚甲基亚胺降解酶(Muccioli 2010).引人注目的是,我们发现该方法显著降低了apelin和APJ的表达。与这些相似在活的有机体内大麻素激动剂刺激脂肪组织外植体可显著降低apelin和APJ的表达。此外,知道db/db当小鼠出现低度炎症反应时,可能与肠道菌群来源的LPS有关,我们研究了LPS在调节这些肽中的作用。有趣的是,我们证明了LPS直接增加了脂肪组织中的平苷能系统张力。我们还发现LPS治疗完全抵消了ecb依赖性apelin和APJ的下调。综上所述,所有这些数据都有力地支持了这一概念,即这两个系统都涉及平能调的调节。然而,我们在活的有机体内而且在体外数据表明,在这个相声中,炎症是主要的控制因素。基于这些数据,我们推测,在生理条件下,eCB系统的色调参与了平苷能系统的下调,而在病理条件下,低级别的炎症色调作为主开关同时增加eCB系统的色调和平苷能系统。虽然我们的数据依赖于不同的调节机制(eCB张力和代谢性内毒素血症),但两者都明显与肠道菌群组成相关(Cani和Delzenne, 2011).因此,了解肠道微生物群的复杂性对于破译宿主和微生物之间的潜在相互作用越来越重要。
总之,我们证明了eCB和低级别炎症张力密切参与脂肪组织apelin和APJ表达的调节。此外,我们发现遗传肥胖和2型糖尿病小鼠的肠道菌群组成与瘦小鼠相比发生了深刻的变化。虽然我们发现了特定细菌和无鳞能系统之间强烈的正相关和负相关,但几种细菌对塑造这些小鼠表型的确切影响仍有待研究。
利益冲突声明
作者声明,这项研究是在没有任何商业或财务关系的情况下进行的,这些关系可能被解释为潜在的利益冲突。
致谢
Patrice D. Cani是比利时FRS-FNRS(科学研究基金会)的研究助理。Jacques Schrenzel和Patrice François分别得到了瑞士国家科学基金会的资助,编号为#31003A-124717/1和3100A0-116075。Nathalie M. Delzenne和Patrice D. Cani是FSR和FRSM基金(Fonds spéciaux de recherches, UCL,比利时;科学研究基金会médicale,比利时)。
脚注
参考文献
Backhed, F., Ding, H., Wang, T., Hooper, L. V., Koh, G. Y., Nagy, A., Semenkovich, C. F.和Gordon, J. I.(2004)。肠道微生物群是调节脂肪储存的环境因素。Proc。国家的。学会科学。美国101年,15718 - 15723。
布卢赫,M.,恩格斯利,S., Kloting, N., Berndt, J.,法肖尔,M., Batkai, S., Pacher, P., Schon, M. R., Jordan, J., and Stumvoll, M.(2006)。腹部肥胖中外周和脂肪组织内源性大麻素系统的失调。糖尿病55岁,3053 - 3060。
Brun, P., Castagliuolo, I., Leo, V. D., Buda, A., Pinzani, M., Palu, G., and Martines, D.(2007)。肥胖小鼠肠道通透性增加:非酒精性脂肪性肝炎发病机制的新证据。点。j .杂志。Gastrointest。肝脏杂志。292年,G518-G525。
Cani, P. D., Amar, J., Iglesias, M., Poggi, M., Knauf, C., Bastelica, D., Neyrinck, A., Fava, F., Tuohy, K. M., Chabo, C., Waget, A., Delmee, E., Cousin, B., Sulpice, T., Chamontin, B., Ferrieres, J., Tanti, J. F., Gibson, G. R., cassteilla, L., Delzenne, N. M., Alessi, M. C.和Burcelin, R. (2007a)。代谢性内毒素血症引起肥胖和胰岛素抵抗。糖尿病56岁,1761 - 1772。
Cani, P. D., Neyrinck, A. M., Fava, F., Knauf, C., Burcelin, R. G., Tuohy, K. M., Gibson, G. R.和Delzenne, N. M. (2007b)。肠道菌群中双歧杆菌的选择性增加通过与内毒素血症相关的机制改善高脂饮食诱导的小鼠糖尿病。Diabetologia50岁,2374 - 2383。
Cani, P. D., Bibiloni, R., Knauf, C., Waget, A., Neyrinck, A. M., Delzenne, N. M.和Burcelin, R.(2008)。肠道菌群的变化控制代谢内毒素诱导的炎症在高脂饮食诱导的肥胖和糖尿病小鼠。糖尿病57岁,1470 - 1481。
Cani, P. D., Possemiers, S., Van de, W. T., Guiot, Y., Everard, A., Rottier, O., gerurts, L., Naslain, D., Neyrinck, A. M., Lambert, D. M., Muccioli, G. G.和Delzenne, N. M.(2009)。肥胖小鼠肠道菌群的变化通过glp -2驱动改善肠道通透性的机制控制炎症。肠道今年58岁,1091 - 1103。
克莱森,M. J,奥沙利文,O.,王,Q.,尼克拉,J.,马切西,J. R.,史密特,H.,德沃斯,W. M.,罗斯,R. P.和欧图尔,P. W.(2009)。焦磷酸测序和系统发育微阵列用于探索人类远端肠道微生物群落结构的比较分析。公共科学图书馆。一个4, e6669。doi: 10.1371 / journal.pone.0006669
Cole, J. R., Wang, Q., Cardenas, E., Fish, J., Chai, B., Farris, R. J., Kulam-Syed-Mohideen, A. S., McGarrell, D. M., Marsh, T., Garrity, G. M.和Tiedje, J. M.(2009)。核糖体数据库项目:改进的比对和rRNA分析的新工具。核酸测定。37岁的D141-D145。
Cote, M., Matias, I., Lemieux, I., Petrosino, S., Almeras, N., Despres, J. P.和Di, Marzo V.(2007)。肥胖男性循环内源性大麻素水平、腹部肥胖和相关心脏代谢危险因素Int。j . ob。(Lond)。31日,692 - 699。
戴维,D.,布歇,J.,盖斯塔,S.,德雷,C.,圭涅,C.,奎略特,D.,阿亚夫,A.,齐格勒,O.,卡彭,C.,索尔尼尔-布拉什,J. S.,男仆,P.和卡斯坦-劳雷尔,I.(2006)。TNFalpha上调人和小鼠脂肪组织apelin表达。美国实验生物学学会联合会J。20岁,1528 - 1530。
De La Serre, C. B., Ellis, C. L., Lee, J., Hartman, A. L., Rutledge, J. C.和Raybould, H. E.(2010)。大鼠高脂饮食诱导的肥胖倾向与肠道菌群和肠道炎症的变化有关。点。j .杂志。Gastrointest。肝脏杂志。299年,G440-G448。
D 'Eon, t.m., Pierce, K. A., Roix, J. J., Tyler, A., Chen, H., and Teixeira, s.r.(2008)。脂肪细胞胰岛素抵抗在肥胖相关内源性大麻素升高的发病机制中的作用。糖尿病57岁,1262 - 1268。
Devane, W. A., Hanus, L., Breuer, A., Pertwee, R. G., Stevenson, L. A., Griffin, G., Gibson, D., Mandelbaum, A., Etinger, A.和Mechoulam, R.(1992)。一种与大麻素受体结合的脑成分的分离和结构。科学258年,1946 - 1949。
丁,T. P.,卡朋特,D.,莱斯利,F. M.,弗洛因德,T. F.,卡托纳,I.,森西,S. L.,卡图里亚,S.和Piomelli, D.(2002)。脑单甘油酯脂肪酶参与内源性大麻素失活。Proc。国家的。学会科学。美国99年,10819 - 10824。
德雷,C.,德巴德,C.,耶格尔,J.,迪斯,E.,戴维,D.,马丁,P.,阿塔尼,C.,瓦内克,E.,桂尼,C.,博斯特,F.,坦蒂,J. F.,拉维尔,M.,维达尔,H.,瓦莱特,P.,卡斯坦-劳雷尔,I.(2010)。Apelin和APJ在2型糖尿病小鼠和人脂肪组织和骨骼肌中的调控。点。j .杂志。性。金属底座。298年,E1161-E1169。
德雷,C.,可耐夫,C.,戴维,D.,瓦吉特,A.,布歇,J.,布里昂,M.,卡尼,P.,阿塔尼,C.,圭涅,C.,卡彭,C.,布塞林,R.,卡斯坦-劳雷尔,I.和瓦莱特,P.(2008)。Apelin刺激正常和肥胖胰岛素抵抗小鼠的葡萄糖利用。细胞金属底座。8, 437 - 445。
杜帕克,T.,科罗姆,A.,卡尼,P. D.,马萨利,N.,拉斯特雷利,S.,德拉加德,A., Le, G. S., Mouledous, L., Frances, B.,勒克莱尔,I., Llores-Cortes, C., Pospisilik, J. A., Delzenne, N. M., Valet, P., Castan-Laurell, I.,和Knauf, C. (2011a)。在小鼠中,中央顶elin通过一氧化氮依赖通路控制葡萄糖稳态。Antioxid。氧化还原信号.doi: 10.1089 / ars.2010.3454。[印刷前Epub]
Duparc, T., Naslain, D., Colom, A., Muccioli, G. G., Massaly, N., Delzenne, N. M., Valet, P., Cani, P. D.和Knauf, C. (2011b)。肥胖和糖尿病小鼠的空肠炎症损害肠内葡萄糖检测并改变下丘脑中的一氧化氮释放。Antioxid。氧化还原信号。14日,415 - 423。
恩格利,S.,博恩克,J.,费尔德波什,M.,戈尔泽尼亚克,K.,扬克,J.,巴特凯,S.,帕彻,P.,哈维-怀特,J.,卢夫特,F. C.,夏尔马,A. M.和乔丹,J.(2005)。人类肥胖中外周内源性大麻素系统的激活。糖尿病54岁,2838 - 2843。
Erdem, G., Dogru, T., Tasci, I., Sonmez, A.和Tapan, S.(2008)。新诊断的2型糖尿病患者血浆皮质素水平低。Exp。中国。性。糖尿病116年,289 - 292。
韩晟,王国强,齐晓霞,李海明,英格兰德,王志伟,格里利,王志伟(2008b)。低氧诱导的apelin表达在肠内细胞增殖中的可能作用。点。j .杂志。Regul。中国。广告样稿,杂志。294年,R1832-R1839。
海诺宁,M. V.,普尔霍宁,A. K.,米耶蒂宁,P., Paakkonen, M.,皮里宁,E.,阿尔哈瓦,E.,阿克曼,K.和赫齐格,K. H.(2005)。Apelin, orexin-A和瘦素血浆水平在病态肥胖和胃束带的影响。Regul。Pept。130年,7 - 13。
Hellmann, J., Tang, Y., Kosuri, M., Bhatnagar, A., and Spite, M.(2011)。Resolvin D1降低肥胖-糖尿病小鼠脂肪组织巨噬细胞积累并改善胰岛素敏感性美国实验生物学学会联合会J。25日,2399 - 2407。
Hildebrandt, m.a., Hoffmann, C., Sherrill-Mix, s.a., Keilbaugh, s.a., Hamady, M., Chen, y.y., Knight, R., Ahima, r.s., Bushman, F., and Wu, g.d.(2009)。高脂肪饮食决定了独立于肥胖的小鼠肠道微生物群的组成。胃肠病学137年,1716 - 1724。
伊佐,A. A.,皮西泰利,F.,卡帕索,R.,阿维罗,G.,罗马诺,B.,博雷利,F.,彼得罗西诺,S.和迪,M. V.(2009)。肥胖中的外周内源性大麻素失调:与食物剥夺和再喂食引起的肠道运动和能量处理有关。Br。j .杂志。158年,451 - 461。
Kathuria, S., Gaetani, S., Fegley, D., Valino, F., Duranti, A., Tontini, A., Mor, M., Tarzia, G., La, R. G., Calignano, A., Giustino, A., Tattoli, M., Palmery, M., Cuomo, V., and Piomelli, D.(2003)。通过阻断anandamide水解调节焦虑。Nat,地中海。9日,76 - 81。
Lazarevic, V., Whiteson, K., Hernandez, D., Francois, P.和Schrenzel, J.(2010)。唾液微生物群个体间和个体内变异的研究。BMC基因组学11日,523年。doi: 10.1186 / 1471-2164-11-523
莱,R. E,巴克赫德,F.,特恩鲍,P.,洛祖彭,C. A.,奈特,R. D.和戈登,J. I.(2005)。肥胖会改变肠道微生物生态。Proc。国家的。学会科学。美国102年,11070 - 11075。
刘俊,Batkai, S., Pacher, P., Harvey-White, J., Wagner, J. A., Cravatt, B. F., Gao, B.和Kunos, G.(2003)。脂多糖通过CD14/MAPK/phosphoinositide 3-kinase/NF-kappaB诱导巨噬细胞内的anandamide合成,独立于血小板激活因子。生物。化学。278年,45034 - 45039。
Lozupone, C., Hamady, M.和Knight, R.(2006)。UniFrac—一个在线工具,在系统发育的背景下比较微生物群落多样性。BMC生物信息学7日,371年。doi: 10.1186 / 1471-2105-7-371
Martin, F. P., Wang, Y., Sprenger, N., Yap, I. K., Rezzi, S., Ramadan, Z., Pere-Trepat, E., Rochat, F., Cherbut, C., van, B. P., Fay, L. B., Kochhar, S., Lindon, J. C., Holmes, E.和Nicholson, J. K.(2008)。在人源化微生物组小鼠模型中有条件的益生元调节跨基因组相互作用的自上而下系统生物学集成。摩尔。系统。医学杂志。4、205。
马丁内斯,I.,华莱士,G.,张,C.,莱格,R.,本森,A. K.,卡尔,T. P.,森山,E. N.和沃尔特,J.(2009)。在高胆固醇血症仓鼠模型中,饮食诱导的代谢改善与肠道菌群的改变密切相关。达成。环绕。Microbiol。75年,4175 - 4184。
Matias, I., Gonthier, M. P., Orlando, P., Martiadis, V., De, P. L., Cervino, C., Petrosino, S., Hoareau, L., Festy, F., Pasquali, R., Roche, R., Maj, M., Pagotto, U., Monteleone, P., and Di, M. V.(2006)。内源性大麻素在脂肪和胰腺细胞模型以及肥胖和高血糖中的调节、功能和调节异常。j .中国。性。金属底座。91年,3171 - 3180。
Melgar-Lesmes, P., Pauta, M., Reichenbach, V., Casals, G., Ros, J., Bataller, R., Morales-Ruiz, M.和Jimenez, W.(2011)。缺氧和促炎因子上调人星状细胞和肝细胞apelin受体表达。肠道.doi: 10.1136 / gut.2010.234690。[Epub提前付印]。
梅耶,F.,帕尔曼,D., D 'Souza, M., Olson, R., Glass, E. M., Kubal, M., Paczian, T., Rodriguez, A., Stevens, R., Wilke, A., Wilkening, J.和Edwards, R. A.(2008)。宏基因组RAST服务器——用于宏基因组自动系统发育和功能分析的公共资源。BMC生物信息学9日,386年。doi: 10.1186 / 1471-2105-9-386
Mihara, M., Aihara, K., Ikeda, Y., Yoshida, S., Kinouchi, M., Kurahashi, K., Fujinaka, Y., Akaike, M.和Matsumoto, T.(2010)。抑制凝血酶作用改善2型糖尿病db/db小鼠的胰岛素抵抗。内分泌学151年,513 - 519。
穆奇奥利,G. G.,纳斯兰,D.,巴克赫德,F., Reigstad, C. S.,兰伯特,D. M., Delzenne, N. M.和Cani, P. D.(2010)。内源性大麻素系统将肠道微生物群与脂肪形成联系起来。摩尔。系统。医学杂志。6、392。
Rajilic-Stojanovic, M., Heilig, H. G., Molenaar, D., Kajander, K., Surakka, A., Smidt, H., and de Vos, W. M.(2009)。人类肠道芯片的开发和应用,一种系统发育微阵列:分析青年人和老年人丰富的微生物群中普遍保守的系统型。环绕。Microbiol。11日,1736 - 1751。
Soriguer, F., Garrido-Sanchez, L., Garcia-Serrano, S., Garcia-Almeida, J., Garcia-Arnes, J., Tinahones, F. J.和Garcia-Fuentes, E.(2009)。Apelin水平在患有2型糖尿病的病态肥胖受试者中升高。ob。杂志。19日,1574 - 1580。
Sorli, s.c., van den Berghe, L., Masri, B., Knibiehler, B., and Audigier, Y.(2006)。干扰apelin信号的治疗潜力。药物。今天11日,1100 - 1106。
斯塔罗维茨,K. M.,克里斯提诺,L.,马蒂亚斯,I.,卡帕索,R.,拉科奥皮,A.,伊佐,A. A.和迪,M. V.(2008)。高脂饮食喂养小鼠胰腺和脂肪组织内源性大麻素失调。肥胖(银。春天)16, 553 - 565。
特恩宝,P. J.,里道拉,V. K.,费斯,J. J.,雷伊,F. E.,奈特,R.和戈登,J. I.(2009)。饮食对人类肠道微生物群的影响:人源化gnotobiomice的宏基因组分析。科学。Transl。地中海。1、6 ra14。
van den Bogert, B., de Vos, W. M., Zoetendal, E. G.和Kleerebezem, M.(2011)。微阵列分析和条形码焦磷酸测序提供一致的微生物概况取决于人类肠道样本的来源。达成。环绕。Microbiol。77年,2071 - 2080。
维杰-库马尔,M.,艾特肯,J. D.,卡瓦略,F. A., Cullender, T. C., Mwangi, S., Srinivasan, S., Sitaraman, S. V., Knight, R., Ley, R. E.和Gewirtz, A. T.(2010)。缺乏toll样受体5的小鼠代谢综合征和肠道菌群改变。科学328年,228 - 231。
关键词:肠道菌群、2型糖尿病、炎症、LPS、内源性大麻素、apelin、APJ、代谢性内毒素血症
引用:Geurts L, Lazarevic V, Derrien M, Everard A, Van Roye M, Knauf C, Valet P, Girard M, Muccioli GG, François P, de Vos WM, Schrenzel J, Delzenne NM和Cani PD(2011)肥胖和糖尿病瘦素抵抗小鼠肠道微生物群和内源性annabinoid系统张力的改变:对脂肪组织中apelin调节的影响。前面。Microbio。2: 149。doi: 10.3389 / fmicb.2011.00149
收到:2011年3月31日;接受:2011年6月26日;
网上发表:2011年7月13日。
编辑:
Peter J. Turnbaugh美国哈佛大学版权:©2011 Geurts, Lazarevic, Derrien, Everard, Van Roye, Knauf, Valet, Girard, Muccioli, François, De Vos, Schrenzel, Delzenne和Cani。这是一篇开放获取的文章,受作者和前沿媒体SA之间的非排他性许可的约束,允许在其他论坛上使用、分发和复制,前提是原作者和来源的署名和遵守其他前沿条件。
*通信:Patrice D. Cani,鲁汶药物研究所代谢与营养研究小组,Université鲁汶天主教,E. Mounier大道,73 B1-73.11, B-1200布鲁塞尔,比利时。电子邮件:patrice.cani@uclouvain.be