摘要
背景:
英国的癌症存活率低于欧洲平均水平,这至少在一定程度上归因于英国患者的诊断处于晚期。在整个英格兰,癌症存活率存在很大的地区和人口差异。大多数患者是在出现症状或偶然症状后确诊的。本研究定义了一种方法,通过该方法,患者遵循的诊断路线可以分类,以检查延迟诊断的人口统计学、组织、服务和个人原因。
方法:
行政医院病例统计数据与癌症等待时间数据、癌症筛查方案数据和癌症登记数据相关联。使用这些数据集,英格兰在2006-2008年间确诊的每一个癌症病例,都被归类为八种“诊断路径”之一。
结果:
不同的癌症类型在每种途径的病例比例上有很大的差异,这与以往的临床研究相一致。通过急诊途径就诊的患者1年相对生存率明显较低。
结论:
关联的癌症注册和管理数据可用于对所有患者的癌症诊断路径进行可靠分类。这些分类可用于加强对延迟诊断的理解和探索可能的原因。
主要
提高癌症存活率是一项关键挑战。改善预后:癌症的策略”(卫生部,2011年).目前,英国的癌症存活率估计低于许多欧洲国家。如果英国的癌症存活率与欧洲平均水平相当,那么诊断后5年内就可以避免5000人或更多的死亡。Abdel-Rahman等人,2009;理查兹,2009).与欧洲相比,英格兰诊断后第一年观察到的较低生存率在很大程度上可以解释为诊断较晚的证据(汤姆森和福尔曼,2009年).比较英格兰、挪威和瑞典的研究也发现,英格兰的超额死亡人数较高,主要发生在诊断的第一年,主要发生在老年患者(Holmberg等人,2010年;Møller等人,2010;莫里斯等,2011年).随后,诊断可能由表现延迟、初级护理延迟、初级和二级护理之间的延迟以及二级护理延迟(鲁宾等,2011年).在癌症改革战略中宣布的国家意识和早期诊断倡议(卫生部,2007年)旨在协调和支援促进癌症早期诊断的活动和研究。识别和分类患者所采取的癌症诊断路线将揭示不同表现路线之间的生存差异,并帮助我们理解预后不良的患者如何进入二级护理。这可以为有针对性地实施意识和早期诊断举措提供信息,并能够评估其成功与否。为患者确定不同的治疗途径也将使进一步的具体研究能够在癌症类型的基础上进行,以提高对癌症表现的理解,并有助于重点改善为预后差的患者提供的服务。
之前关于诊断途径的研究主要集中在2000年引入的两周等待转诊系统(TWW)的影响上(在该系统中,被全科医生紧急转诊为疑似癌症的患者可以在2周内得到专家的诊治)。他们检查了单一二级护理单位或地理上聚集的全科医生诊所的患者队列(巴雷特和汉密尔顿,2005年,2008;Blick等人,2010年),或检讨有关研究(索恩等,2009年).总体而言,以往的研究显示,不同癌症类型的诊断路径存在差异,但也始终显示,很大一部分病例没有遵循常规、紧急或TWW GP转诊路线。
本研究探讨了使用常规收集的数据来评估2006年至2008年间在英格兰被诊断为恶性癌症的患者(739667个肿瘤)如何获得癌症诊断的二级护理的可行性,以及这些“诊断路径”是否与生存率差异相关。
材料与方法
“诊断路径”被定义为患者与医疗保健系统之间的相互作用序列,根据诊断设置、路径和转介到二级护理的路径,导致癌症诊断。在许多情况下,这条路线始于全科医生会诊。目前可获得的数据将国家数据集中可观察到的部分路线限制在筛查服务和二级保健内,尽管这确实包括初级保健的转诊方法。
许多途径涉及与卫生保健系统不同部分的多重互动。通过结合诊断、途径和转诊途径的设置,可以确定大量的单独路径,在本队列中确定了71种不同的组合。为了便于分析,必须将这些数据聚合到可管理的更广泛的类别中。
经过检查,确定了两类,它们代表了质量上不同的路径(屏幕检测和仅死亡证书(DCO))。三种途径反映转诊的紧迫性(急诊、TWW转诊和其他全科医生转诊)。另外两条路线表示显然是从二级护理开始的病例(住院选修课和其他门诊患者),最后一条路线反映了在诊断路线上没有有用信息的病例(未知)。这八组详细介绍表1.
2006年至2008年间在英国居民中诊断的所有新诊断的恶性肿瘤(不包括非黑素瘤皮肤癌(ICD-10 C00-C97,不包括C44)的癌症登记记录都是从国家癌症数据存储库(NCDR;国家癌症情报网络,2010).这些癌症登记记录在患者层面与2003-2004年至2008-2009年的行政住院和门诊HES数据集(国民保健服务卫生和社会保健信息中心,2011年);2005年11月至2009年1月全国癌症候诊时间监测数据集(信息标准委员会,2002年);2005年至2008年全国乳腺普查计划数据(乳房外科协会,2011年);及2006至2008年全国肠道普查计划数据(NHS肠癌筛查计划,2011年).这些数据集使用唯一的NHS编号进行链接,该编号分配给英国的每个患者,并且出现在每个数据集的几乎每个患者级别的记录中(所有数据集的完整性大于98.5%,门诊HES数据除外,不能直接评估)。NCDR记录的妇科筛查状况提供了宫颈肿瘤的筛查鉴定。使用欧洲癌症登记网络(ENCR)标准(帕金等人,1994年),移除7.0%的个案。
诊断路径算法首先使用HES数据对每个肿瘤的路径进行单独分类。通过NHS编号与癌症登记记录相关联的国家筛查计划和CWT数据随后被检查,分配的路线可能会改变为“筛查”或“TWW”路线。
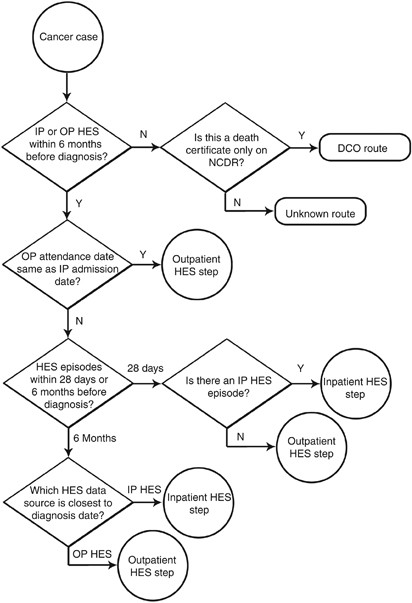
图1显示使用HES数据将每个案例分类为一条路线。在HES中,特定的住院患者或门诊患者发作被确定为路径的“终点”,其接近诊断日期(由使用ENCR标准的标准注册规则定义)。Tyczynski等人,2003年))。终点被假定为最直接导致诊断的临床护理事件。在定义了终点之后,算法寻找路由的起点。通过从终点向后计算来确定起点,如图所示图1,2,3.在护理环境和诊断前的时间长短上都有所不同。这一起点的特点导致了路线的分类。
如果住院和门诊活动都发生在诊断日期,住院发作被定义为路线的终点。否则,如果在诊断日期前28天内有一次发作,则将其指定为路线的终点,住院发作优先于门诊发作,如果有多次发作,则最近的发作优先。如果在诊断后28天内没有HES活动,则将6个月内最近的一次发作(住院或门诊)作为该路线的终点。对于在诊断前6个月没有HES活动的病例,该路径被归类为未知,或对于在NCDR上记录的由癌症登记处指定为DCO状态的病例,该路径被归类为DCO。
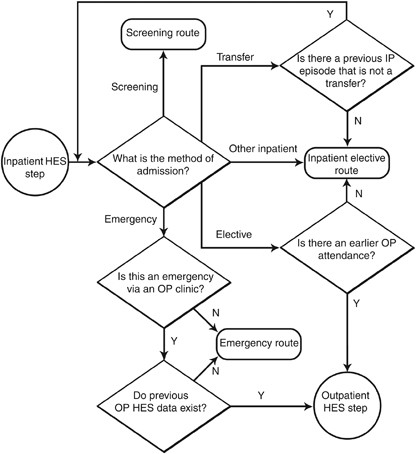
图2显示了当终点是住院时寻求路线起点所采取的步骤。检查终点的进入方法,以确定路线中的前一步。如果入院方法是紧急性质的,则此事件被定义为路线的起点(以及终点),路线被归类为紧急介绍。如果入院方法是转院,则以迭代方式检查入院前6个月内最近的住院活动。如果入院方法表明以前的门诊就诊,确定入院前6个月内最近的门诊活动,并检查该门诊就诊的转诊来源,如下所述,但如果在住院前6个月内没有门诊活动,则该路线被归类为住院选择性。否则,根据所列的代码,该路线被分类为未知或住院病人选择性表1.
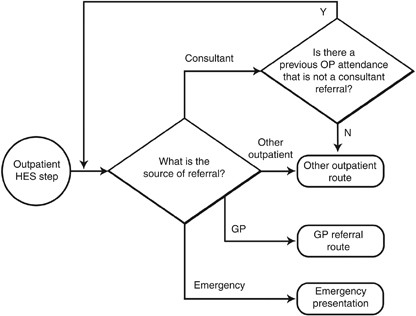
图3显示了当路线的终点是门诊就诊时的门诊转诊源的检查。如果门诊出席不是门诊发作的第一次预约,则检查该发作的第一次预约。如果转诊来源表明从以前的门诊发作转诊,则检查最近6个月内的第一次门诊就诊。另外,根据中代码将该路分为急诊介绍、屏幕检测或其他门诊表1.
从HES数据中为每个病例分配路径后,检查筛选和CWT数据。如果病例可能与疑似癌症的CWT紧急转诊有关,则将其归类为TWW路线,除非使用HES数据分类的路线是在决定治疗日期前28天内入院的紧急介绍。如果该病例可能与筛选事件有关,则该路线被归类为筛选。如果两者都是可能的,那么屏幕检测路由的优先级高于TWW路由(路由优先级汇总在表1).
一个病例与CWT转诊有关,其中TWW在诊断前62天或诊断后31天内决定治疗日期。一例与乳腺筛查事件有关,其中乳腺筛查评估日期在诊断日期前91天或诊断日期后31天内。对于结直肠癌和子宫颈筛查数据,该病例已被筛查检测NHS肠癌筛查计划(2011年)或区域癌症登记处,分别没有进行日期匹配。
该算法是在Microsoft Server 2005数据库环境中用SQL编写的。比例的置信区间计算使用威尔逊评分区间(纽康比,1998).相对生存期的点估计和置信区间的计算是在STATA版本10的统计包中使用strel计划及年龄-性别-区域-剥夺-年寿命表(英国癌症研究中心癌症生存小组,2006年).如果性别、出生日期或诊断日期缺失,或者患者在诊断时年龄超过99岁,则排除在分析之外。没有进一步的年龄分层或病例审查。
结果
所分类的739667个肿瘤中按路径诊断的比例显示在表2.大多数癌症是通过急诊(24%)、TWW(26%)或全科医生转诊(21%)中的一种诊断出来的,其他五种途径占29%。这些比例因癌症类型的不同而有很大差异。
急诊比例随年龄增长而增加,而TWW和GP转诊途径则随年龄下降。未知路径在50岁以下年龄组中最高,而dco在85岁以上年龄组中最高。筛查比例显示了乳房筛查年龄范围的影响。在所有TWW比例低的肿瘤中,儿童(0-14岁)急诊就诊的比例为54%(总体为2%,数据未显示)。青少年和年轻人(15-24岁)的比例更能反映整个队列,24%的肿瘤表现为紧急呈示,某些部位的比例更高(例如,结直肠为57%,数据未显示)。
在2006-2008年的3年中,航线的比例变化不大(数据未显示)。在所有癌症中,TWW途径的比例从25%增加到27%。2006年和2007年归类为紧急呈递的比例为24%,2008年为23%。筛检出的结直肠病例的比例从2006年的0.1%增加到2008年的5%,反映了该方案的分阶段推出NHS肠癌筛查计划(2011年).
相对较小,但有统计学意义(P< 0.001,z2006年至2008年间,通过TWW途径诊断的膀胱癌(5%)、口咽癌(10%)、喉癌(7%)、黑色素瘤(6%)、前列腺癌(5%)和子宫癌(4%)的肿瘤比例有所增加。
一年的相对生存估计是按路线提出的表3,虽然不计算DCO路线的生存期(帕金和哈库利宁,1991).在所有癌症类型中,被归类为紧急呈递的病例的1年相对生存率明显低于通过其他途径呈递的病例。未知路径与其他非紧急呈现路径具有相当的生存期。在目前情况下,屏幕检测路线的相对存活估计最高。
敏感性分析
该算法寻找诊断前28天内的住院患者发作,然后,在诊断前6个月内的任何HES发作作为路线的终点。85%的病例可以从HES数据中分配到一条路线。在这些病例中,74%是在诊断日期前一个月内开始的。在诊断前3个月内有起点的患者增加到84%,在诊断前6个月内有起点的患者增加到98%。
总体而言,94%的诊断路径来自非HES数据(39%)或终点在诊断日期前28天内的HES数据(56%),只有4%的诊断路径来自终点在诊断日期前28天至6个月的HES数据。
诊断前一个月(住院患者)的入院频率比诊断前一年同期(在整个患者队列中)高19倍。对于85岁以上的人,这个比例是14:1。
2006年至2008年间,在患有一种以上侵袭性癌症的患者中诊断出肿瘤(6.2%),不包括非黑素瘤皮肤癌(ICD-10 C00-C97除C44)。如果排除这些多发性肿瘤,那么紧急路线的总体比例增加了不到0.1%,未知路线的总体比例增加了0.2%,其他路线的比例变化不到0.5%。包括多发性肿瘤在内的所有路径和癌症类型组合的最大变化为1.7%,平均绝对变化为0.2%。
如果紧急陈述路线优先级最高,其次是tww路线、筛查路线和其他路线,那么紧急陈述路线上升0.6%,tww路线下降0.4%,筛查路线下降0.2%。如果屏幕检测到的路线优先级最高,其次是tww路线、紧急情况介绍和其他路线,则紧急情况介绍下降1.2%,tww路线上升1.2%,筛查保持不变。
筛查数据和CWT数据专门与癌症记录相关,而不是像HES数据那样与患者相关。因此,这些数据被视为更可靠的,因此,由它们生成的路线取代了由医院入院记录生成的路线,但在决定治疗日期前28天内收治的紧急情况报告除外。如果“屏幕检测到的路线”没有优先于“紧急情况介绍”,则影响不到0.2%。
如果决定治疗日期在诊断日期前31天至诊断日期后62天的3个月内,则使用TWW记录对路线进行分类。如果筛查日期在诊断日期前91天到诊断日期后31天的4个月内,则使用筛查记录对路线进行分类。选择这些时间段是为了与这些患者路径的典型时间尺度相对应,并考虑到癌症登记规则,该规则优先从病理确认中定义诊断日期。敏感性分析显示,一个月的筛选日期周期变化对路径故障影响不大;如果TWW匹配期从诊断日前1个月缩短到诊断后1个月,TWW路径的比例会降低4%。将所有TWW路线优先于紧急情况呈报,可使观察到的紧急情况呈报比例降低约1%。
讨论
诊断算法的路由
该算法的一个核心假设是,合理地假设住院和门诊医院长达6个月的活动,特别是诊断前28天的活动与癌症的诊断有关。这种活动不一定是由癌症本身直接引起的,因为可以通过其他临床调查进行诊断,例如,对不相关疾病的放射检查。
与一年前相比,诊断前一个月的活动频率较高,表明诊断前28天的大部分医院活动与癌症诊断有关。保守的假设是,“背景”事件与与诊断相关的事件被算法提取的几率相同,而进一步的保守假设是,它们将给出不正确的聚合路线,这使得我们可以估计出由于“背景”入院导致的算法错误率的总体上限为10%。由此产生的癌症诊断比例的不确定性,即25%的癌症,总体上约为2.5%,对于85岁以上的人来说略高。对于老年人来说,非紧急情况介绍可能会有一个小的偏见,因为事实上,他们较高的“背景”录取率大多数是选择性录取。同样,在已有共病的特定患者组中也会存在小的系统性影响,其结果的偏倚取决于共病入院的典型性质。
该算法并不试图将诊断出的癌症与特定癌症住院患者或门诊患者的HES记录相匹配。大多数门诊记录没有诊断编码,即使在门诊或住院记录中存在诊断编码,感兴趣的发作(诊断前)也可能不包括癌症特异性编码。该算法仅依赖于存在的出勤和发病记录,相关的管理字段记录转诊来源和入院方法,使得计算出的路径对临床编码的变化不敏感。
所提出的方法有几个可调参数。包含多个肿瘤并没有实质性地影响路径之间的频率变化的大小,因此它们被包括在分析中(Brenner和Hakulinen, 2007;Rosso等人,2009年).稍微改变关于筛查和TWW路线的紧急情况介绍的优先级(大约1%或更少)会改变分类为每种路线的病例的比例。紧急示诊和屏幕检测的路径之间没有重叠,这是令人放心的,因为大多数屏幕检测到的病例是早期肿瘤,不太可能导致紧急示诊。
虽然该方法允许指定诊断路径,但它并不打算确定可能导致癌症诊断的癌症或其他疾病的表现症状。需要进一步的特定部位研究,以了解导致患者遵循每种肿瘤的诊断路径的复杂性质。
航路频率和对生存的影响
在每一种检查的肿瘤类型中,急诊就诊的1年相对生存率明显低于任何其他途径。紧急路线和非紧急路线之间的生存差异通常在20-40%的范围内。有紧急情况报告的老年人比例较高,这可能在一定程度上解释了这种生存差异。对于几种癌症部位,包括中枢神经系统癌、肝癌和下消化道癌,TWW途径的一年相对生存期低于其他非紧急途径。考虑到TWW的转介速度相对较快,这可能是等待时间悖论的一个例子(Crawford等人,2002年).这与其他研究结果一致(Tørring等,2011)表明,最紧急的转诊病例的结果更糟。
分配到未知路径的病例有癌症登记(不仅仅基于死亡证明),但在诊断前6个月的HES中没有数据,在CWT或筛查来源中也没有数据。50岁以下人群和社会经济较富裕人群(未显示数据)中未知路线所占比例较高,可能表明这一群体中私人转诊的比例较高。年龄的影响也见于国家初级保健癌症诊断审计(鲁宾等,2011年),这表明私人转诊在70岁以上的人群中不太常见。相对较大比例(18%)的肿瘤被分配到未知途径的黑色素瘤可能是由于肿瘤在初级保健中被切除,而没有怀疑黑色素瘤。在所有癌症类型中,未知路径的生存率与其他非紧急路径的生存率相当,这表明通过非紧急设置提供护理。
与其他研究的比较
这项研究使用国家定义的数据集计算人口水平上的路线比例。当将这些比例与以前的研究进行比较时,应考虑患者队列的性质。来自初级保健的患者队列可能未记录筛查发现的病例、在医院护理期间作出的偶然诊断以及在诊断后不久导致死亡的紧急情况。如果病例发现依赖于组织病理学数据库,来自二级护理的患者队列可能会漏报临床诊断。此外,在单一中心进行的研究中,观察到的比例可能出现统计波动,因为在研究期间,每种肿瘤类型的诊断病例数量相对较低。
来自其他研究的比较结果在表4.在我们的研究中,通过TWW诊断的病例比例与大多数在二级护理中发现病例的研究之间通常有很好的一致性(尼尔等人,2007年;索恩等,2009年;Blick等人,2010年).本研究中所见的急诊报告比例也与通过二级护理或癌症登记发现病例的研究中所见的比例相当(巴雷特和汉密尔顿,2005年;Blick等人,2010年).
通过全科医生转诊的病例总比例在被检查的研究中高于本研究。这可能是由于本研究将筛选检测的、未知的、其他门诊和住院患者选择的途径单独分类。特别是,其他门诊和住院患者选择性路线中的大多数病例最初可能是由全科医生转诊发起的。为了探索这一假设,需要进一步将路由与诊断结果连接到GP数据集。
虽然这8条路线中有一些是英国医疗保健系统所特有的;该方法可用于其他有数据集的国家,详细介绍医院护理的事件。TWW、全科医生转诊、住院病人择期和其他门诊病人的路径都可以被认为起源于全科医生转诊。因此,只使用5条不同的路线就可以进行更普遍的国际比较,这4条路线形成了一个整体的“GP-Initiated”路线。
总之,我们已经展示了一种方法,用于对所有注册肿瘤的诊断路径进行分类,使用大量常规可用的卫生服务数据集。这可以以一种自动的方式应用于英国癌症登记处记录的所有被诊断为癌症的患者,并使研究能够进行,以了解这些群体之间的差异。在癌症诊断中遵循这些途径的频率与以前的临床研究合理一致,并显示出癌症类型和年龄的合理变化。该路径与1年相对生存率有显著相关性。特别是,与非急诊路线相比,急诊路线的相对生存率大大降低,这表明这种区别具有很高的临床意义。
改变历史
二零一二年十月四日
本文在首次发表12个月后进行了修改,以切换到创作共用许可条款,如发表时所述
参考文献
Abdel-Rahman M, Stockton D, Rachet B, Hakulinen T, Coleman MP(2009)如果英国的癌症生存率与欧洲相同:有多少死亡是可以避免的?Br J癌101(补充2):S115-S124
乳房外科协会(2011年)筛查发现癌症的审计,http://www.cancerscreening.nhs.uk/breastscreen/publications/archived-baso-reports.html(2012年8月2日访问)
巴雷特J,汉密尔顿W(2005)英国一个城市前列腺癌的诊断途径。基于人群的研究。扫描J尿肾素39: 267 - 270
巴雷特J,汉密尔顿W(2008)英国肺癌诊断途径:一项队列研究。BMC Fam实践9: 31
Blick C, Bailey D, Haldar N, Bdesha A, Kelleher J, Muneer A(2010)两周等待规则对英国单一机构膀胱癌诊断和管理的影响。Ann R Coll外科英语92: 46-50
Brenner H, Hakulinen T(2007)在国际比较癌症生存研究中不应排除既往患有癌症的患者。肿瘤121: 2274 - 2278
英国癌症研究中心癌症生存小组(2006年)strel计算机程序,版本1.2.7和癌症生存分析的生命表。下载www.lshtm.ac.uk ncde cancersurvival /工具2010年2月8日;英国伦敦卫生与热带医学院非传染性疾病流行病学系
Crawford SC, Davis JA, Siddiqui NA, de Caestecker L, Gillis CR, Hole D(2002)等待时间悖论:苏格兰子宫内膜癌女性治疗延迟和生存的基于人群的回顾性研究。BMJ325: 196
卫生署(2007年)癌症改革策略.卫生部:英国伦敦
卫生署(2011年)改善预后:癌症的策略.卫生部:英国伦敦
Holmberg L, Sandin F, Richards M, Spicer J, Lambe M, Klint A, Peake M, Strand TE, Linklater K, Robinson D, Møller H(2010) 2001-2004年英格兰、挪威和瑞典肺癌生存期的国家比较:差异出现在随访早期。胸腔65(5): 436 - 441
信息标准委员会(2002)DSC公告:22/2002/ dscn / dscn2002/222002.pdf www.isb.nhs.uk文件(2012年8月2日访问)
Morris EJ, Sandin F, Lambert PC, Bray F, Klint A, Linklater KM, Robinson D, Pahlman L, Holmberg L, Møller H(2011) 1996 - 2004年英国、挪威和瑞典结直肠癌患者基于人群的生存比较。肠道60(8): 1087 - 1093
Møller H, Sandin F, Bray F, Klint A, Linklater KM, Purushotham A, Robinson D, Holmberg L(2010)英国、挪威和瑞典乳腺癌生存率:基于人群的比较。肿瘤127(11): 2630 - 2638
Neal R, Allgar V, Nasreen A, Leese B, Heywood P, Proctor G, Evans J(2007)肺癌、结直肠癌、前列腺癌和卵巢癌的分期、生存期和延迟:诊断途径的比较。Br J Gen Pract57: 212 - 219
纽科姆R(1998)单比例的双侧置信区间:七种方法的比较。地中海统计17: 857 - 872
国家癌症情报网络(2010)国家癌症数据库,http://www.ncin.org.uk/collecting_and_using_data/national_cancer_data_repository/default.aspx(2012年8月2日访问)
NHS肠癌筛查计划(2011年)http://www.cancerscreening.nhs.uk/bowel/index.html(2012年8月2日访问)
国民保健制度卫生和社会保健信息中心(2011年)住院事件统计(HES),http://www.hesonline.nhs.uk(2012年8月2日访问)
黄建平,黄建平,黄建平(1991)。进:Jensen OM, Parkin DM, MacLennan R, Muir CS, Skeet RG,(编辑)癌症登记,原则和方法。IARC科学出版物第95号.IARC出版社:里昂,159-176页
Parkin DM, Chen VW, Ferlay J, Galceran J, Storm HH, Whelan SL (1994)癌症登记的可比性和质量控制.IARC技术报告第19号。里昂研究:
Richards M(2009)英国癌症早期诊断奖的规模。Br J癌101: S125-S129
Rosso S, De Angelis R, Ciccolallo L, Carrani E, Soerjomatarum I, Grande E, Zigon G, Brenner H EUROCARE工作组(2009)多发性肿瘤的生存估计。欧元癌症45: 1080 - 1094
鲁宾G,麦克菲尔S,埃利奥特K (2011)国家初级保健癌症诊断审计.皇家全科医师学院:伦敦,英国
Thomson C, Forman D(2009)英国癌症生存和早期诊断的影响:我们可以从最近的EUROCARE结果中学到什么?Br J癌101(补充2):S102-S109
Thorne K, Hutchings H, Elwyn G (2009) NHS胃肠道癌症转诊的两周规则:诊断有效性的系统回顾。开放性结直肠癌J2:即
Tørring ML, Frydenberg M, Hansen RP, Olesen F, Hamilton W, Vedsted P(2011)结肠直肠癌的诊断时间与死亡率:初级护理中的队列研究。Br J癌104: 934 - 940
Tyczynski J, Démaret E, Parkin D (eds)(2003)欧洲癌症注册标准和指南。IARC技术出版物40: 69 - 73
确认
我们感谢Chris Carrigan,已故的Brian Cottier, Tariq Malik, Jodie Moffat, Eva Morris, Andy Pring, James Thomas, Catherine Thomson, Julia Verne以及国家癌症情报网、英国癌症登记处、英国癌症研究中心和国家癌症服务分析小组的其他工作人员。
作者信息
作者及隶属关系
相应的作者
额外的信息
本作品在标准许可发布协议下发布。12个月后,该作品将免费提供,许可条款将切换到创作共用署名-非商业性类似共享3.0未移植许可。
权利和权限
自最初发布12个月后,本作品按照创作共用署名-非商业性相同方式共享3.0未移植许可协议授权使用。要查看此许可证的副本,请访问http://creativecommons.org/licenses/by-nc-sa/3.0/
关于本文
引用本文
埃利斯-布鲁克斯,L.,麦克菲尔,S.,艾夫斯,A.。et al。癌症诊断路线-使用多个常规数据集确定患者的旅程。Br J癌107, 1220-1226(2012)。https://doi.org/10.1038/bjc.2012.408
收到了:
修改后的:
接受:
发表:
发行日期:
DOI:https://doi.org/10.1038/bjc.2012.408
关键字
- 诊断
- 通路
- 推荐
- 生存
- 紧急
- 路线
这篇文章被引用
症状性结直肠癌患者发病至诊断时间与预后的关系
BMC癌症(2022)
评估诊断途径如何因癌症患者的年龄而变化:丹麦一项全国性的基于登记的队列研究
BMC癌症(2022)
COVID-19大流行对英国一个地区急诊医院癌症入院人数的影响
BMC癌症(2022)
已有精神障碍患者的癌症诊断途径:一项全国性的基于登记的队列研究
BMC癌症(2022)
增加对肺癌筛查计划的接受:通过共同设计与社区建立联系
BMC公共卫生(2022)