摘要gydF4y2Ba
人类结肠菌群中优势种的种群可能被饮食摄入改变,从而对健康产生影响。在这里,我们检查了精确控制饮食对14名超重男性的影响。志愿者先后被提供对照饮食,高抗性淀粉(RS)或非淀粉多糖(NSPs)的饮食和减少碳水化合物减肥(WL)饮食,超过10周。对6名志愿者粪便样本中的16S rRNA序列进行分析,发现320种系统型(识别度为>98%),其中26种,包括19种培养物种,各占>1%的序列。尽管样本在个体上的聚集比在饮食上的聚集更强烈,但通过靶向qPCR获得的时间过程显示,在饮食改变后,特定细菌群中的“大量繁殖”迅速发生。随后的饮食迅速扭转了这一状况。的亲属gydF4y2Ba瘤胃球菌属bromiigydF4y2Ba(r -瘤胃球菌)在RS饮食的大多数志愿者中增加,占细菌总数的平均17%,而NSP饮食的比例为3.8%gydF4y2BaOscillibactergydF4y2Ba组在RS和WL饲粮中均增加。的亲属gydF4y2Ba真细菌rectalegydF4y2BaRS增加(平均为10.1%),但随着gydF4y2BaCollinsella aerofaciensgydF4y2Ba,在WL。然而,个体间差异显著,两名食用RS饮食的志愿者中有60%的RS未发酵,而其他12名志愿者的这一比例<4%;这两个个体也显示出低数量的r -瘤胃球菌(<1%)。饮食中不可消化的碳水化合物可以使肠道菌群发生显著变化,但这取决于个人肠道菌群的初始组成。gydF4y2Ba
简介gydF4y2Ba
基于16S rrna的分析显示,人类结肠菌群在细菌种类和系统型水平上的显著多样性。从给定的粪便样本中,不仅通常估计存在于人类结肠微生物群中的数百种系统类型(gydF4y2BaSuau et al., 1999gydF4y2Ba;gydF4y2BaEckburg等人,2005年gydF4y2Ba),但据报道,不同个体的样本显示存在有限的系统型重叠(gydF4y2BaLey等人,2006年gydF4y2Ba;gydF4y2BaTurnbaugh et al., 2008gydF4y2Ba).最近一项研究(gydF4y2BaTap等人,2009年gydF4y2Ba)的研究表明,在不同个体的优势粪便细菌中,某些系统型比其他系统型更常见。确定定植大肠的优势细菌种类及其受饮食和宿主因素影响的程度,对于揭示结肠微生物群对人类健康的影响至关重要(gydF4y2BaFlint et al., 2007gydF4y2Ba;gydF4y2Ba索科尔等人,2008年gydF4y2Ba).gydF4y2Ba
迄今为止,一些研究已经检查了时间上的变化,这些研究表明,正常饮食的个体结肠菌群具有一定程度的稳定性(gydF4y2Ba弗兰克斯等人,1998年gydF4y2Ba;gydF4y2BaZoetendal等,1998gydF4y2Ba;gydF4y2Ba科斯特洛等人,2009gydF4y2Ba).相比之下,人们对饮食变化对微生物群落组成的影响知之甚少。有证据表明,膳食中补充低聚果糖和菊粉等益生元可以促进特定细菌群的生长,包括双歧杆菌(gydF4y2BaBouhnik等人,2004年gydF4y2Ba;gydF4y2BaRamirez-Farias等人,2009gydF4y2Ba).研究还表明,在肥胖受试者的减肥(WL)饮食中,总碳水化合物含量的减少,对结肠中细菌群落的组成和代谢输出有重大影响(gydF4y2Ba邓肯等人,2007年gydF4y2Ba,gydF4y2Ba2008gydF4y2Ba;gydF4y2Ba布林克沃斯等人,2009gydF4y2Ba).这些变化被认为反映了到达大肠的不可消化(ND)碳水化合物成分(主要是非淀粉多糖(NSPs)、抗性淀粉(RS)和某些低聚糖)的发酵。然而,饮食中通常存在的主要类型的ND碳水化合物(RS和NSP)的控制变化对结肠微生物群的影响尚未得到任何详细的研究。人类饮食中的ND碳水化合物含量被认为会影响健康。例如,高RS饮食已被证明有利于胰岛素敏感性,这可能是由结肠中的细菌发酵活动介导的(gydF4y2Ba罗伯逊等,2005年gydF4y2Ba).含有RS和NSP的饮食通过将发酵酸,特别是丁酸酸输送到远端结肠,为预防结直肠癌提供了潜在的好处(gydF4y2BaMcIntyre等人,1993年gydF4y2Ba;gydF4y2Ba邓肯等人,2007年gydF4y2Ba).NSP的微生物分解也会将结合的植物化学物质释放到结肠(gydF4y2Ba吉尔和罗兰,2002年gydF4y2Ba).这些健康益处对肥胖和超重的受试者尤其重要,因为他们罹患大肠癌和糖尿病的风险较高(gydF4y2BaPolednak 2003gydF4y2Ba;gydF4y2BaCani等人,2007年gydF4y2Ba).gydF4y2Ba
这项研究的问题是,饮食中主要类型的ND碳水化合物的变化在多大程度上影响个体中存在的主要细菌系统类型。它还通过使用详细的时间过程和交叉设计,首次探索了这些变化的动态,包括它们的可逆性。一个必要的补充问题是,相同的饮食变化是否会引起不同个体肠道菌群的相似变化。我们的研究结果显示,一组超重志愿者在摄入主要类型的可发酵碳水化合物(RS或NSP)后,结肠微生物群发生了快速而显著的变化。我们还发现,这些变化对个体具有高度特异性,对设计富含纤维的饮食具有潜在的重要意义。gydF4y2Ba
材料与方法gydF4y2Ba
志愿者招募gydF4y2Ba
志愿者最初是通过报纸广告招募的。男性纳入标准为体重指数>27 kg mgydF4y2Ba−2gydF4y2Ba腰围>102 cm,空腹血糖浓度>6.0 mmol lgydF4y2Ba−1gydF4y2Ba,表示代谢综合征。他们接受了体检,并联系了他们的全科医生以确认病史和用药史。在研究前6个月或研究期间,所有受试者均无胃肠道疾病或紊乱史,也未服用抗生素。最初的16名受试者中有两人因为与方案无关的原因离开了研究。其余14名志愿者平均年龄为54岁(27-73岁),平均体重指数(kg mgydF4y2Ba−2gydF4y2Ba)(范围27.9-51.3)(gydF4y2Ba补充表S1gydF4y2Ba).这项研究得到了苏格兰北部研究伦理服务机构的批准,所有志愿者都提供了知情的书面同意。gydF4y2Ba
实验设计和饮食制度gydF4y2Ba
志愿者在进入试验前体重稳定(过去4个月变化<3公斤)。在前7周,在能量维持时为每个人提供1.4-1.5 ×测量的静息代谢率。最后的干预期包括高蛋白WL饮食,持续3周(gydF4y2Ba补充表S2gydF4y2Ba,gydF4y2Ba补充图S1gydF4y2Ba).初始维持日粮(M日粮)中蛋白质/碳水化合物/脂肪的代谢能比例为13:52:35,NSP为27.7 g / d,连续饲喂7天。然后受试者被提供两种饮食的固定摄入量,其中包括高RS饮食或高NSP饮食,每种饮食在随机交叉设计中供应3周(gydF4y2Ba补充图S1gydF4y2Ba).RS饲粮中添加了III型RS,而NSP饲粮中添加了麦麸。所有餐食都具有相同的能量密度(5.5 MJ kggydF4y2Ba−1gydF4y2Ba)及每顿饭后的体重(gydF4y2Ba补充表S2gydF4y2Ba).每日宏量营养素摄入量使用Windiet软件程序(罗伯特戈登大学,阿伯丁,英国)计算,基于每种食材的类型和数量以及公布的食物成分表(gydF4y2Ba2002年食品标准局gydF4y2Ba).平均每周收集两次粪便样本。此外,从每个饲粮期的最后一周收集一个24小时用于消化率的化学分析。gydF4y2Ba
饲料成分和消化率的化学分析gydF4y2Ba
分析饲粮总能、RS、不溶性和可溶性NSPs (gydF4y2Ba补充表S2gydF4y2Ba).对饲粮和24 h粪便样本中RS含量的估计由gydF4y2Ba英格斯特等人(1992)gydF4y2Ba而NSPs的定量描述为gydF4y2Ba英格利斯特和卡明斯(1988)gydF4y2Ba.gydF4y2Ba
从粪便样本中提取DNAgydF4y2Ba
粪便样本保存在4°C,并在收集后5小时内处理。这种短时间的储存预计不会影响微生物群落组成的分子估计(gydF4y2BaLauber等人,2010年gydF4y2Ba).每个样品混合,5克分散(3500 r.p.m.。使用Dispomix Drive, Medic Tools, Lussiwag, Switzerland),在10ml无菌磷酸盐缓冲盐水缓冲液中浸泡1分钟,然后进行混合。根据制造商(Qbiogene, MP Biomedicals, Illkirch, France)的说明,使用FastDNA Spin for soil试剂盒立即用于DNA提取。gydF4y2Ba
16S rRNA克隆文库序列的系统发育分析gydF4y2Ba
从提取的DNA中PCR扩增16S rRNA基因,在94℃下初始变性5 min;变性(95°C 30秒),退火(52°C 30秒),72°C延伸2分钟,最后在72°C循环8分钟。Taq1聚合酶来自Promega (Southampton, UK),浓度为0.025 U μlgydF4y2Ba−1gydF4y2Ba在2.5米的存在gydF4y2Ba米gydF4y2BaMgClgydF4y2Ba2gydF4y2Ba.正向引物由7f, 27fChl, 27fBor, 27fBif和27fAto的4:1:1:1:1的混合物组成,反向引物为1510r (gydF4y2Ba补充表S3gydF4y2Ba).PCR产物使用Wizard PCR产物纯化试剂盒(Promega)清洗,然后按照描述进行克隆和测序(gydF4y2Ba劳利等人,2009年gydF4y2Ba).序列(跨越可变区域V2-V5)使用母软件包(gydF4y2BaSchloss et al., 2009gydF4y2Ba),并由Mallard (gydF4y2BaAshelford等人,2006年gydF4y2Ba),针尾(gydF4y2BaAshelford等人,2005年gydF4y2Ba)及BLAST (gydF4y2Ba约翰逊等人,2008年gydF4y2Ba).去除嵌合序列后,使用ARB包中的编辑器功能进行大量的手动管理(gydF4y2Ba路德维希等人,2004年gydF4y2Ba).使用策画对齐,使用ARB创建带有Felsenstein校正的距离矩阵。然后将此矩阵用作DOTUR (gydF4y2Ba施洛斯和汉德尔斯曼,2005gydF4y2Ba),在默认的最近邻设置下,使用98%的身份截断。系统发育相似性为>98%的序列可认为属于同一系统发育型。这产生了320个系统类型(gydF4y2Ba补充表S4gydF4y2Ba),由RDP分类器(gydF4y2Ba科尔等人,2009年gydF4y2Ba),并在NCBI数据库中使用MegaBLAST (gydF4y2Ba约翰逊等人,2008年gydF4y2Ba).稀疏性分析、Shannon和Simpson多样性指数计算、群落结构与∫-Libshuff比较、简约和加权版本UniFrac、Jaccard和Yue和Clayton θ树聚类分析均使用母本软件包(gydF4y2BaSchloss et al., 2009gydF4y2Ba).gydF4y2Ba
最终的16S rRNA克隆文库数据集来自6名志愿者(v16、v19、v20、v22、v23和v24),包含5915个序列(中位数长度为678个碱基)(GenBank登录号)gydF4y2BaGU238434-GU244348gydF4y2Ba).这些序列来自四种饲料中的每一种饲料中的每个个体的一个粪便样本,除了志愿者v16,其中两个样本来自M和NSP饲料(见gydF4y2Ba补充表S4gydF4y2Ba).随后,仅从v14和v25的RS和NSP日粮中又获得了768个序列(gydF4y2Ba补充表S5gydF4y2Ba) (GenBank登录号gydF4y2BaHM191774-HM192541gydF4y2Ba).gydF4y2Ba
16S rRNA基因qPCR和DGGE分析gydF4y2Ba
对所有14名志愿者的所有可用样本进行实时定量PCR (qPCR)。引物序列和条件在gydF4y2Ba补充表S3gydF4y2Ba的研究主要基于gydF4y2BaRamirez-Farias et al. (2009)gydF4y2Ba.引物对gydF4y2BaOscillibactergydF4y2Ba本研究设计了相关细菌。gydF4y2Ba
在变性梯度凝胶电泳(DGGE)中,用16S基因V3高可变区引物PCR扩增细菌DNA (gydF4y2Ba补充表S3gydF4y2Ba).反应混合物含1.5 mgydF4y2Ba米gydF4y2BaMgClgydF4y2Ba2gydF4y2Ba每μl含有0.025 U Taq1聚合酶。产品在含有尿素和甲酰胺(梯度35-60%)的8%丙烯酰胺变性梯度凝胶中分离,在80 V下,60°C下,16小时,并用SybrGold染料(Invitrogen, Paisley, UK)染色。gydF4y2Ba
统计分析gydF4y2Ba
对于丰度较大的系型(超过1%,在6个志愿者中有5或6个存在,320个系型中有8个存在),桑格序列(克隆计数)使用具有逻辑链接和估计过度分散的二项模型作为层次广义线性模型进行分析。这是一次对一个系型进行,以每个样品的克隆总数作为总计数。志愿者和饮食分别被视为随机(正态分布)和固定效应。粪便样本之间的相似性通过主坐标分析以图形方式显示,其中堪培拉距离矩阵应用于每个粪便样本分配给每个系统类型的克隆数量(基于所有320个系统类型)。主坐标分析还用于获得320个系统发育类型之间的系统发育距离(从DOTUR软件包获得)的图形表示。gydF4y2Ba
采用方差分析的方法检验饮食的效果,志愿者为随机,饮食为固定效应。当饮食效果显著时,比较饮食均数gydF4y2Ba事后处理gydF4y2Ba以及。包含许多零(即低于检测极限)的数据用Friedman的非参数方差分析代替。在所有的分析中,顺序的影响最初被作为固定效应,但它及其与饮食的相互作用被发现不显著,并从后续的分析中删除。所有统计分析均使用Genstat第11版11.1版(VSN国际有限公司,Hemel Hempstead,赫特福德郡,英国)进行。重要性被设定为gydF4y2BaPgydF4y2Ba-value <0.05。gydF4y2Ba
结果gydF4y2Ba
研究设计gydF4y2Ba
14名超重男性志愿者完成了这项研究(见材料和方法部分)(gydF4y2Ba补充表S1gydF4y2Ba).在10周的研究期间,每天提供完整的饮食,从而精确控制所有的饮食摄入量(gydF4y2Ba补充表S2gydF4y2Ba).每个志愿者在第一周接受体重控制(M)饮食,然后分别接受三周的高III型抗性淀粉(RS饮食)或高麦麸(NSP)饮食,以及减少碳水化合物但富含蛋白质的WL饮食(WL饮食)。前三种饮食以维持能量为主,并且碳水化合物、蛋白质和脂肪的总含量非常匹配;一半志愿者的RS和NSP饮食顺序颠倒了(gydF4y2Ba补充图S1gydF4y2Ba,gydF4y2Ba补充表S2gydF4y2Ba).收集粪便样本后应尽快处理,不进行预先冷冻,以提取核酸(见材料和方法部分)。gydF4y2Ba
肠道细菌群落中的显性细菌类群gydF4y2Ba
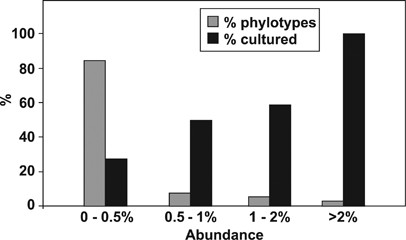
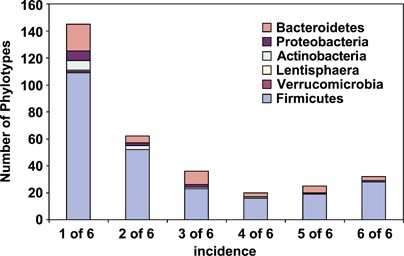
首先使用DGGE分析了所有可用粪便样本的16S rRNA谱,结果显示,在特定饮食的个体中,随着时间的推移,谱是一致的(gydF4y2Ba补充图S2gydF4y2Ba).然而,在RS和NSP饮食之间的切换,极大地改变了分布,表明细菌群落组成发生了变化。对14名志愿者中的6人(每个饮食顺序3人)的16S rRNA基因扩增序列进行了分析,使用的样本来自每种饮食制度的最后一周。这产生了5915个非嵌合序列(平均每个样本227个序列)。系统发育分析使用98%的序列识别截断,在所有样本中显示320个系统发育型(gydF4y2Ba补充表S4gydF4y2Ba).培养菌株的比例随着系统型丰度的增加而增加,所有系统型均出现在>,占总数的2% (gydF4y2Ba图1gydF4y2Ba).在每个样本中都没有检测到320种系统型,但在所有6个志愿者中都存在32种系统型,占所有序列的47.1%,而在6个个体中至少有4个个体中出现了77种系统型(gydF4y2Ba图2gydF4y2Ba,gydF4y2Ba补充图S3gydF4y2Ba).gydF4y2Ba图2gydF4y2Ba提示系统型发生的双峰频率分布,表明在人类肠道菌群中可能存在一组广泛且高度丰富的系统型(gydF4y2BaTap等人,2009年gydF4y2Ba).最丰富的系型为gydF4y2Ba真细菌rectalegydF4y2Ba虽然三个系型对应于三个不同的品系gydF4y2BaFaecalibacterium prausnitziigydF4y2Ba共占总序列的8.0% (gydF4y2Ba表1gydF4y2Ba).gydF4y2Ba
16S rRNA系统型的可培养性与其丰度相关。从六名志愿者(四种饮食)的粪便样本中获得的16S rRNA序列(5915)被分为320个系统型(在>98%的序列一致性中定义)(gydF4y2Ba补充表S4gydF4y2Ba).与培养的细菌显示>98%序列相同的系分型百分比随着系分型丰度的增加而增加。系统型频率分布以百分比表示;实际系统型数分别为9(>占所有序列的2%)、17(>1%<2%)、24(>0.5%<1%)和270(<0.5%)(共320)。数据为16、20、22(饮食顺序为RS-NSP)和19、23、24(饮食顺序为NSP-RS)志愿者。gydF4y2Ba
不同个体的系统型发生率。所有320个16S rRNA系统型的分布在六名志愿者中被确定(见gydF4y2Ba图1gydF4y2Ba,gydF4y2Ba补充表S4gydF4y2Ba);根据细菌门,在所有六个个体(32)和五个(25),四个(20),三个(36),两个(62)或一个(145)中发现的系统型的数量在这里显示。gydF4y2Ba
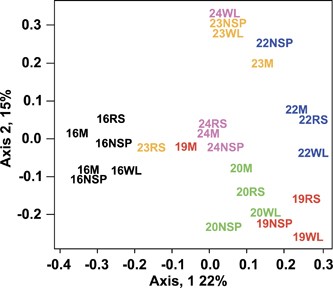
使用母体软件包(gydF4y2BaSchloss et al., 2009gydF4y2Ba).∫-Libshuff、精简法和UniFrac(加权和非加权)分析显示,个体之间存在高度的差异,每个样本与其他样本之间存在显著差异。利用Jaccard、Yue和Clayton theta相似系数(gydF4y2BaYue和Clayton, 2005gydF4y2Ba) (gydF4y2Ba补充图S4gydF4y2Ba).这些结果与主坐标分析结果(gydF4y2Ba图3gydF4y2Ba)表明样本主要由志愿者聚集,这表明对饮食变化的反应受到个体结肠微生物群初始物种组成的影响。稀少度分析显示,四种饲料的物种丰富度相似(gydF4y2Ba补充图S5gydF4y2Ba).RS和NSP饲粮的Simpson (1/D)和Shannon多样性指数略低于M和WL饲粮,但差异不显著(p < 0.05)。gydF4y2Ba补充图S5;gydF4y2Ba另请参阅gydF4y2Ba补充表S4gydF4y2Ba对于个别值)。gydF4y2Ba
饮食和个体变异对粪便菌群组成的影响。基于26份粪便样本的16S rRNA克隆文库的主坐标分析(使用堪培拉距离矩阵)(从六名捐赠者在四种饮食条件下获得)(gydF4y2Ba补充表S4gydF4y2Ba).颜色代码基于供体(v16, v19, v20, v22, v23和v24)。饮食用M表示,维持;非淀粉多糖NSP;RS,抗性淀粉;WL,减肥。对来自M和NSP饲料的两个样品进行了v16分析。gydF4y2Ba
结肠微生物群落对饮食变化的反应gydF4y2Ba
在门水平上,饲粮对粪便菌群中拟杆菌门(平均21.5%)、厚壁菌门(平均70.6%)、放线菌门(平均4.9%)和变形菌门(平均3.0%)的比例无显著影响。然而,在更精细的分类学水平上,gydF4y2Ba大肠rectalegydF4y2Ba而且gydF4y2Ba瘤胃球菌属bromiigydF4y2Ba,在RS饮食中比例增加,而gydF4y2BaCollinsella aerofaciensgydF4y2Ba在WL饮食中的比例下降(gydF4y2BaPgydF4y2Ba< 0.001) (gydF4y2Ba表1gydF4y2Ba).由于序列数据也提示相关系型组可能受到饮食的影响,我们决定使用qPCR进行进一步分析。gydF4y2Ba
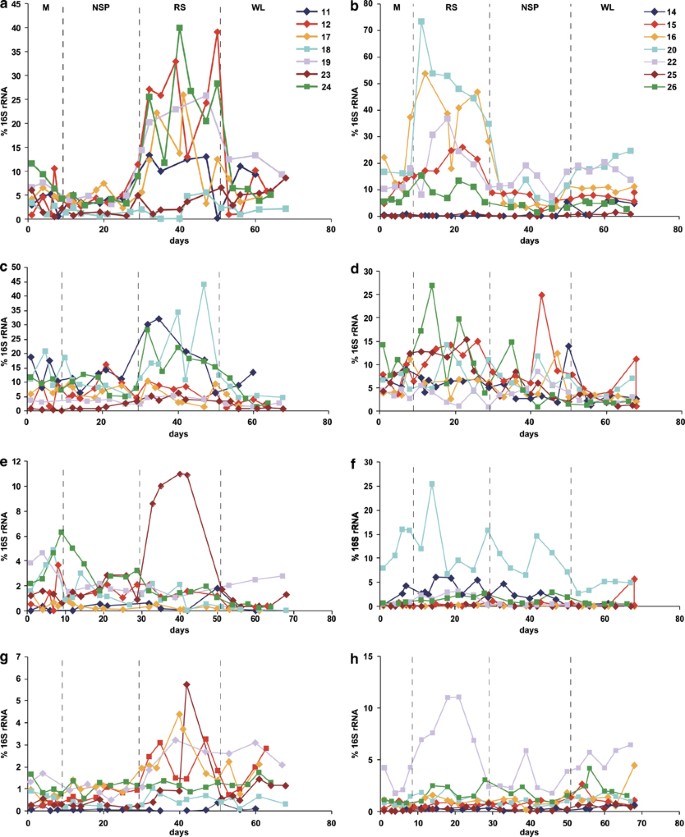
PCR引物组(gydF4y2Ba补充表S3gydF4y2Ba),用于序列分析表明对RS饮食(朗姆酒,Ros, Osc)有反应的目标组,或用于先前gydF4y2Ba在体外gydF4y2Ba有证据表明,利用淀粉(Bac, Bif, Fprau)的能力(gydF4y2Ba表2gydF4y2Ba).产甲烷菌也被监测,因为它们对多糖利用群落的潜在影响(gydF4y2BaRobert和bernnier - donadille, 2003gydF4y2Ba).分析了所有可用的时间点。目标群体的平均数据显示在gydF4y2Ba表2gydF4y2Ba全部14门课程的全部时间课程见gydF4y2Ba图4gydF4y2Ba那些对RS饮食有反应的细菌群。朗姆酒集团包括gydF4y2Bar . bromiigydF4y2Ba,gydF4y2Bar . flavefaciensgydF4y2Ba而且gydF4y2Bar·阿不思·gydF4y2Ba它们属于瘤胃球菌科,在这里被称为“r -瘤胃球菌”。显著增加了约4.5倍(gydF4y2BaPgydF4y2Ba<0.001),与NSP饮食相比(gydF4y2Ba表2gydF4y2Ba,gydF4y2Ba图4gydF4y2Ba).设计了一套新的引物来识别瘤胃球菌科的另一组,与gydF4y2BaOscillibacter valericigenesgydF4y2Ba(gydF4y2BaIino等人,2007年gydF4y2Ba)这种细菌不是从人体肠道中培养出来的。与M和NSP饲粮相比,该组的RS和WL平均显著增加(gydF4y2BaPgydF4y2Ba< 0.001) (gydF4y2Ba表2gydF4y2Ba,gydF4y2Ba图4gydF4y2Ba).先前报道的引物集(gydF4y2BaMackie等人,2003年gydF4y2Ba)针对瘤胃中该组的亲戚也被使用,但检测到<0.1%的人类粪便细菌(结果未显示)。第三个丰富的瘤胃球菌群,gydF4y2Baf . prausnitziigydF4y2Ba,对饮食变化无明显反应(gydF4y2Ba表2gydF4y2Ba).gydF4y2Ba
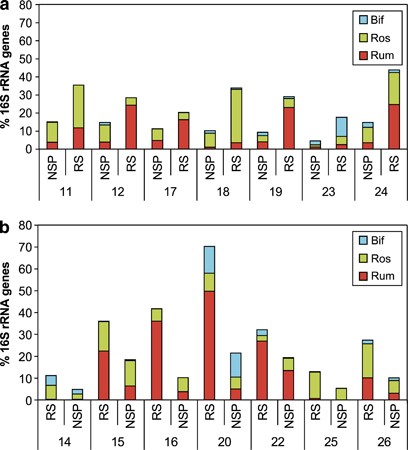
qPCR检测四组人结肠细菌的饮食驱动变化。每个目标组的丰度表示为用一般细菌引物集获得的信号的百分比(见gydF4y2Ba补充表S3gydF4y2Ba用于引物和使用的条件)。显示了14名志愿者的所有可用时间点:左边的面板显示饮食顺序M-NSP-RS-WL,右边的面板显示M-RS-NSP-WL, (gydF4y2Ba一个gydF4y2Ba而且gydF4y2BabgydF4y2BaR-ruminococci (R-ruminococci的亲戚)gydF4y2Bar . bromiigydF4y2Ba);(gydF4y2BacgydF4y2Ba而且gydF4y2BadgydF4y2Ba)亲戚gydF4y2Ba大肠rectalegydF4y2Ba而且gydF4y2BaRoseburiagydF4y2Baspp。(gydF4y2BaegydF4y2Ba而且gydF4y2BafgydF4y2Ba)gydF4y2Ba双歧杆菌属gydF4y2Baspp。(gydF4y2BaggydF4y2Ba而且gydF4y2BahgydF4y2Ba)亲戚gydF4y2Bao . valericigenesgydF4y2Ba.gydF4y2Ba
厚壁菌门有关的细菌gydF4y2BaRoseburiagydF4y2Ba而且gydF4y2Ba大肠rectalegydF4y2Ba亦大幅增加(gydF4y2BaPgydF4y2Ba<0.048),降低(约为RS的三倍)(gydF4y2BaPgydF4y2Ba<0.029)。(Ros,gydF4y2Ba表2gydF4y2Ba).所有组间的个体差异都很明显gydF4y2Ba图4gydF4y2Ba.值得注意的是,gydF4y2Ba双歧杆菌属gydF4y2Basp .对RS没有表现出显著的平均反应,但在一名志愿者中,他们的人口在RS上显著增加(v23) (gydF4y2Ba图4gydF4y2Ba而且gydF4y2Ba5gydF4y2Ba).双歧杆菌通常在16S rRNA克隆文库中表现不佳(gydF4y2BaEckburg等人,2005年gydF4y2Ba;gydF4y2BaHold等,2002年gydF4y2Ba),在我们的分析中也是如此,尽管使用了广泛的细菌引物集,据报道包括该组(gydF4y2Ba弗兰克等人,2008年gydF4y2Ba).%无明显变化gydF4y2Ba拟杆菌gydF4y2Ba因应饮食(gydF4y2Ba表2gydF4y2Ba).gydF4y2Ba
在RS(高抗性淀粉)和NSP(低抗性淀粉)饲粮中,研究了三组具有潜在淀粉溶解能力的细菌种群。通过qPCR估计r -瘤胃球菌的种群,gydF4y2Ba大肠rectale / RoseburiagydF4y2Ba种虫害和gydF4y2Ba双歧杆菌属gydF4y2Ba对所有14名志愿者按饮食顺序进行计数。数据是每个志愿者在RS和NSP饮食的第二周和第三周的平均值(总平均值在gydF4y2Ba表2gydF4y2Ba).gydF4y2Ba
9名志愿者的>中90%的样本被qPCR检测到产甲烷古菌,而v11、14、17、24和25的样本中检测到的古菌不到10%。对照组无显著影响(gydF4y2Ba表2gydF4y2Ba).gydF4y2Ba
RS和NSP的消化率gydF4y2Ba
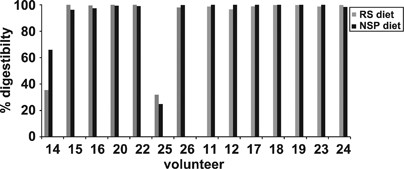
通过对饲粮和24 h粪便收集的化学分析,估计RS和NSP的全消化道消化率。在14名志愿者中,有12人在所有四种饮食的粪便样本中回收了<4%的摄入RS,反映了几乎完全的微生物发酵。然而,对于两个个体(v14和v25), RS饮食中的粪便RS回收率分别为69%和65%(消化率为31%和35%)(gydF4y2Ba图6gydF4y2Ba).通过qPCR评估,这两个个体都具有低r -瘤胃球菌数量,尽管其中一个显示r -瘤胃球菌数量增加gydF4y2BaRoseburiagydF4y2Ba而且gydF4y2Ba大肠rectalegydF4y2BaRS饮食组(gydF4y2Ba图4gydF4y2Ba而且gydF4y2Ba5gydF4y2Ba).随后对这两只个体RS和NSP饮食期的最终样本进行了额外的克隆文库分析。未检出r -瘤胃球菌,36%和46.5%的克隆属于r -瘤胃球菌gydF4y2Ba拟杆菌门gydF4y2Ba在对v14和v25进行分析的381和387个克隆中(gydF4y2Ba补充表S5gydF4y2Ba).gydF4y2Ba
淀粉消化率。在估算饲粮和24小时粪便样本中抗性淀粉的含量后,确定抗性淀粉的全肠道消化率%(见材料和方法部分)。结果仅显示在NSP和RS饮食期。v14和v25中抗性淀粉消化率的显著降低与这些个体中r -瘤胃球菌数量的低相对应(见正文和gydF4y2Ba补充表S5gydF4y2Ba).gydF4y2Ba
可溶性NSP消化率平均为90%,略低(gydF4y2BaPgydF4y2BaRS和WL饲粮(88%)均<0.05),M饲粮(92%)均<0.05。不溶性NSP消化率平均为66%,各组间无差异(平均范围为58-71%)。gydF4y2Ba
讨论gydF4y2Ba
这是第一个将精确控制和监测人类饮食摄入量和消化率与详细分析粪便微生物群在细菌系统分型水平上的变化相结合的研究。因此,有可能揭示饮食和影响人类结肠群落的个体差异之间的相互作用。对扩增的16S rRNA序列的分析表明,来自6名超重男性志愿者的样本在个体上比在饮食上聚集得更强。这与先前报道的粪便微生物群个体间差异的证据一致(gydF4y2Ba弗兰克斯等人,1998年gydF4y2Ba;gydF4y2BaLey等人,2006年gydF4y2Ba).相比之下,通过克隆文库和对279份粪便样本的大量qPCR分析,饮食成分对特定细菌群有非常显著的影响。时间进程表明,大多数饮食驱动的变化发生得很快,在3-4天内可检测到,并且同样迅速地逆转。这些动力学似乎与膳食残渣对结肠中相对细菌生长速率的直接影响一致,随后在粪便样本中反映为结肠内容物的周转,假设平均结肠过境时间约为60小时(gydF4y2BaStephen等人,1987年gydF4y2Ba).gydF4y2Ba
厚壁菌门gydF4y2Ba与此相关的细菌gydF4y2Bar . bromiigydF4y2Ba(R-ruminococci)和gydF4y2Ba大肠rectalegydF4y2Ba通常会受到RS饮食的刺激在大多数个体中,qPCR分析显示R-ruminococci的数量激增,在一些样本中超过细菌总数的25%。R-ruminococci是之前发现的唯一一组优先与人类粪便样本中的颗粒物质相关的人类肠道细菌(gydF4y2Ba沃克等人,2008年gydF4y2Ba),表明它们在颗粒基质的分解中起着重要作用。gydF4y2Bar . bromiigydF4y2Ba分离株具有溶淀粉活性(gydF4y2BaSalyers等人,1977年gydF4y2Ba)但我们的研究结果表明,许多相关但未培养的细菌也可能具有这种活性。之前的一项研究,使用非定量DGGE分析,报告说gydF4y2Bar . bromiigydF4y2Ba饮食中含有大量RS和NSP的人的粪便样本中相关细菌显著(gydF4y2BaAbell等人,2008年gydF4y2Ba).的gydF4y2Ba大肠rectalegydF4y2Ba而且gydF4y2BaRoseburiagydF4y2Ba组中也含有淀粉溶解的种类(gydF4y2BaRamsay等人,2006年gydF4y2Ba),但以前没有显示对RS有反应gydF4y2Ba在活的有机体内gydF4y2Ba.早期的一项研究未能发现特异性的增加gydF4y2Ba真细菌gydF4y2Ba在高RS III型饮食的人类受试者中,spp.,但重要的是,检测方法没有gydF4y2Ba大肠rectalegydF4y2Ba(gydF4y2BaSchwiertz等人,2002年gydF4y2Ba).在这项工作中,我们还检测到一组未培养的瘤胃球菌相关的饮食反应gydF4y2BaOscillibacter。gydF4y2Ba目前尚不清楚这些细菌是否是淀粉降解者,而RS和WL饮食中细菌数量的增加表明,它们对饮食的反应一定与其他因素有关。gydF4y2Ba
早期研究表明,在培养的人类肠道细菌中,淀粉酶活性分布广泛,其中50%的菌株,包括许多gydF4y2Ba拟杆菌gydF4y2Ba,可在直链淀粉或支链淀粉上生长(gydF4y2BaSalyers等人,1977年gydF4y2Ba).的潜在作用gydF4y2Ba双歧杆菌属gydF4y2Ba在高直链淀粉RS (gydF4y2Ba麦克法兰和英格利斯特,1986gydF4y2Ba;gydF4y2Ba王等,1999gydF4y2Ba).在本研究中,双歧杆菌数量仅在一个个体(v23)中显示出对RS的强烈反应,而没有证据表明对RS的反应gydF4y2Ba拟杆菌gydF4y2Ba组到RS。gydF4y2Ba拟杆菌gydF4y2Basp .可能更适合使用可溶性淀粉分子(gydF4y2Ba弗林特等人,2008gydF4y2Ba).这些发现gydF4y2Ba在活的有机体内gydF4y2Ba不过,与最近的研究比较吻合gydF4y2Ba在体外gydF4y2Ba确认gydF4y2Bar . bromiigydF4y2Ba,gydF4y2Ba大肠rectalegydF4y2Ba而且gydF4y2Ba双歧杆菌属gydF4y2Ba在人类粪便中以淀粉颗粒为定植物的主要种类(gydF4y2BaLeitch等人,2007年gydF4y2Ba)和使用gydF4y2Ba13gydF4y2Bac标记淀粉(gydF4y2BaKovatcheva-Datchary等人,2009gydF4y2Ba).gydF4y2Ba
不同种类的淀粉溶解细菌在其代谢产物和潜在的宿主相互作用方面有显著差异。gydF4y2Ba双歧杆菌属gydF4y2Ba产乳酸和醋酸盐的菌,被广泛用作益生菌和益生元的靶点(gydF4y2BaFurrie等人,2005年gydF4y2Ba).委员会成员gydF4y2Ba大肠rectalegydF4y2Ba属鞭毛细菌,它们是大肠内丁酸盐的主要产生者,因此可能是RS产生丁酸盐的原因之一(gydF4y2BaAminov等人,2006gydF4y2Ba;gydF4y2Ba邓肯等人,2007年gydF4y2Ba;gydF4y2Ba路易斯等人,2010年gydF4y2Ba).gydF4y2Bar . bromiigydF4y2Ba是醋酸酯、乙醇和氢的生产者,可能有助于产生气体,但目前很少知道这个基团对宿主的影响。鉴于不同类型的RS对发酵和宿主反应的不同影响,未来建立不同类型的RS是否选择不同的淀粉菌群将是重要的(gydF4y2BaLe Leu等人,2009年gydF4y2Ba).gydF4y2Ba
淀粉被认为在整个胃肠道中具有较高的消化率,大多数RSs在大肠中完全发酵(gydF4y2BaBird等人,2000年gydF4y2Ba).然而,值得注意的是,在这里研究的14个人中,有2个人的粪便中有大量的淀粉在发酵中幸存下来。这种发酵的差异不能归因于饮食摄入,这对所有14名受试者都是标准化的,而且似乎可能与每个人的结肠微生物群的菌株组成有关。这两个个体的R-ruminococci数量非常低,群落组成与淀粉发酵之间的关系显然值得进一步研究。虽然这两个个体也非产甲烷菌,但产甲烷菌和r -瘤胃球菌之间没有明显的简单关系。已知甲烷菌种群在个体之间有所不同,并受多种因素的影响(gydF4y2BaFlorin等人,2000年gydF4y2Ba).gydF4y2Ba
与这些对RS的反应相反,几乎没有证据表明高NSP饮食导致粪便微生物群组成的重大变化。然而,在某种程度上,这可能反映了这样一个事实:与M饮食相比,NSP摄入量(1.5倍)比RS摄入量(4.8倍)增加得更小。正如RS所观察到的,特定NSP成分的较大变化可能会影响特定结肠细菌群的种群gydF4y2Bac . aerofaciensgydF4y2Ba对于gydF4y2Ba大肠rectalegydF4y2BaWL饮食组WL的变化并没有显示出与RS和NSP摄入量的简单关系,而且这种饮食中蛋白质含量的增加可能在改变微生物群组成方面发挥了作用。gydF4y2Ba
这里观察到的主要细菌门的分布与非肥胖受试者的分布没有显著差异(gydF4y2BaEckburg等人,2005年gydF4y2Ba;gydF4y2Ba沃克等人,2008年gydF4y2Ba).我们通过qPCR和克隆文库分析得到的数据与最近使用荧光技术对肥胖受试者的报道一致gydF4y2Ba原位gydF4y2Ba杂交显微镜(gydF4y2Ba邓肯等人,2007年gydF4y2Ba,gydF4y2Ba2008gydF4y2Ba;gydF4y2BaSchwiertz等人,2010gydF4y2Ba)或16S rRNA测序(gydF4y2BaZhang et al., 2008gydF4y2Ba)虽然较低%gydF4y2Ba拟杆菌gydF4y2Ba已在另一项研究中报告(gydF4y2BaLey等人,2006年gydF4y2Ba).肥胖者和非肥胖者的肠道菌群在物种水平上可能存在更细微的差异,而这里报告的饮食反应确实使这种情况有可能发生。然而,在这个研究小组中确定的10个最丰富的系型中,有5个也在10个最丰富的系型中gydF4y2BaTap et al. (2009)gydF4y2Ba在非肥胖志愿者中。gydF4y2Ba
我们在这里检测到的最丰富的16S rRNA系统型中,与培养细菌相对应的比例很高,占> - 0.5%序列的50个系统型中有66%具有密切的培养亲缘关系。这表明,人类肠道菌群通过培养的覆盖范围有限可能是由于厌氧隔离工作不足,而不是由于人类结肠细菌固有的不可培养性。这里检测到的五个最丰富的系统型中的四个(gydF4y2Ba大肠rectalegydF4y2Ba,gydF4y2Baf . prausnitziigydF4y2Ba,gydF4y2Bac . aerofaciensgydF4y2Ba而且gydF4y2Bab . vulgatusgydF4y2Ba)与日本-夏威夷人、北美白种人和息肉患者的厌氧培养中所报告的最丰富的物种(gydF4y2Ba摩尔和摩尔,1995年gydF4y2Ba).但总体而言,本研究中33.4%的系统型与培养菌的一致性<98%,反映出培养菌株对较少丰度的菌群的覆盖率相对较低。许多丰富的系统型被发现是广泛存在的,在所有6个被调查的个体中检测到的320种系统型中有32种存在,占所有序列的近一半(47%)。gydF4y2Ba
总之,我们发现,在人类饮食中增加RS(一种重要的ND碳水化合物)的摄入量可以极大地改变结肠微生物群的物种组成。这种反应也可能发生在其他可发酵的ND膳食成分上。由此可见,结肠微生物群落通常必须处于一种持续变化的状态,这是由饮食摄入的短期变化所驱动的。因此,在不同的采样时间和不同的个体中,只有最成功和最多才多艺的生物才会在优势微生物群中普遍发现。此外,然而,我们的证据表明,结肠菌群的菌株组成受到个体间变异的影响。此外,我们还表明,这可能与微生物群落对饮食变化的反应以及结肠中饮食基质的微生物发酵的深刻个体差异有关。这表明,未来关于ND碳水化合物摄入的饮食建议可能需要个性化。gydF4y2Ba
加入代码gydF4y2Ba
参考文献gydF4y2Ba
Abell GCJ, Cooke CM, Bennett CN, Conlon MA, McOrist AL。(2008)。与。相关的系统型gydF4y2Ba瘤胃球菌属bromiigydF4y2Ba在人类的大肠中大量存在,并对高抗性淀粉的饮食做出反应。gydF4y2BaFEMS微生物生态gydF4y2Ba66gydF4y2Ba: 505 - 515。gydF4y2Ba
阿米诺夫RI,沃克AW,邓肯SH,哈森HJM,韦林GW,弗林特HJ。(2006)。分子多样性、培养和改进FISH检测与人类肠道细菌的优势群有关gydF4y2BaRoseburiagydF4y2Ba种虫害或gydF4y2Ba真细菌gydF4y2BarectalegydF4y2Ba.gydF4y2Ba应用环境微生物gydF4y2Ba72gydF4y2Ba: 6371 - 6376。gydF4y2Ba
Ashelford KE, Chuzhanova NA, Fry JC, Jones AJ, Weightman AJ。(2005)。据估计,目前在公共存储库中保存的20个序列记录中至少有1个包含大量异常。gydF4y2Ba应用环境微生物gydF4y2Ba71gydF4y2Ba: 7724 - 7736。gydF4y2Ba
Ashelford KE, Chuzhanova NA, Fry JC, Jones AJ, Weightman AJ。(2006)。新的筛选软件显示,最近的大型16S rRNA基因克隆文库包含嵌合体。gydF4y2Ba应用环境微生物gydF4y2Ba72gydF4y2Ba: 5734 - 5741。gydF4y2Ba
鸟AR,棕色IL,顶DL。(2000)。淀粉,抗性淀粉,肠道菌群和人类健康。gydF4y2Ba当前问题的细菌gydF4y2Ba1gydF4y2Ba: 25-37。gydF4y2Ba
博尼克Y,拉斯金L,西蒙诺G,维考E,纽特C,弗洛里BgydF4y2Ba等gydF4y2Ba.(2004)。不可消化碳水化合物刺激健康人粪便双歧杆菌的能力:一项双盲、随机、安慰剂对照、平行组、剂量反应关系研究gydF4y2BaJ是clinin Nutr吗gydF4y2Ba80gydF4y2Ba: 1658 - 1664。gydF4y2Ba
Brinkworth GD, Noakes M, Clifton PM, Bird AR。(2009)。极低碳水化合物、高脂肪和高碳水化合物、低脂减肥饮食对排便习惯、粪便短链脂肪酸和细菌数量的比较影响gydF4y2Ba英国人J纳特gydF4y2Ba101gydF4y2Ba: 1493 - 1502。gydF4y2Ba
Cani PD, Amar J, Iglesias MA, Poggi M,可耐福C, Bastelica DgydF4y2Ba等gydF4y2Ba.(2007)。代谢性内毒素血症引起肥胖和胰岛素抵抗。gydF4y2Ba糖尿病gydF4y2Ba56gydF4y2Ba: 1761 - 1772。gydF4y2Ba
Cole JR, Wang Q, Cardenas E, Fish J, Chai B, Farris RJgydF4y2Ba等gydF4y2Ba.(2009)。核糖体数据库项目:改进的比对和rRNA分析的新工具。gydF4y2Ba核酸测定gydF4y2Ba37gydF4y2Ba: D141-D145。gydF4y2Ba
科斯特洛EK, Lauber CL, Hamady M, Fierer N, Gordon JI, Knight R。(2009)。人体栖息地细菌群落在时间和空间上的变化。gydF4y2Ba科学gydF4y2Ba326gydF4y2Ba: 1694 - 1697。gydF4y2Ba
Duncan SH, Belenguer A, Holtrop G, Johnstone AM, Flint HJ, Lobley GE。(2007)。肥胖受试者饮食中碳水化合物摄入量的减少导致粪便中丁酸盐和产生丁酸盐的细菌浓度的降低。gydF4y2Ba应用环境微生物gydF4y2Ba73gydF4y2Ba: 1073 - 1078。gydF4y2Ba
Duncan SH, Lobley GE, Holtrop G, Ince J, Johnstone AM, Louis PgydF4y2Ba等gydF4y2Ba.(2008)。人类结肠菌群与饮食、肥胖和体重减轻有关。gydF4y2Ba肥胖症gydF4y2Ba32gydF4y2Ba: 1720 - 1724。gydF4y2Ba
Eckburg PB, Bernstein CN, Purdom E, Dethlefsen L, Sargent M, Gill SRgydF4y2Ba等gydF4y2Ba.(2005)。人体肠道微生物菌群的多样性。gydF4y2Ba科学gydF4y2Ba308gydF4y2Ba: 1635 - 1638。gydF4y2Ba
英伦斯,卡明斯。(1988)。植物性食品中膳食纤维非淀粉多糖含量测定的改进方法。gydF4y2BaJ协会的肛门化学gydF4y2Ba1gydF4y2Ba: 247 - 286。gydF4y2Ba
英格利斯特HN,金曼SM,卡明斯JE。(1992)。营养重要淀粉组分的分类与测定。gydF4y2BaEur J clinin NutrgydF4y2Ba46gydF4y2Ba(补充2):S33-S50。gydF4y2Ba
食品标准局(2002年)。gydF4y2BaMcCance和Widdowson的《食物的组成gydF4y2Ba,第六次总结。皇家化学学会:剑桥。gydF4y2Ba
Flint HJ, Bayer EA, Rincon MT, Lamed R, White BA。(2008)。肠道细菌多糖的利用:从基因组分析中获得新见解的潜力。gydF4y2BaNat Rev微生物gydF4y2Ba6gydF4y2Ba: 121 - 131。gydF4y2Ba
李志强,李志强,李志强,李志强。(2007)。人类结肠微生物群落内的相互作用和竞争:饮食与健康之间的联系。gydF4y2Ba环境MicrobiolgydF4y2Ba9gydF4y2Ba: 1101 - 1111。gydF4y2Ba
吴国强,朱国强,吴国强。(2000)。共同和独特的环境因素决定了人类和大鼠体内产甲烷菌的生态。gydF4y2Ba是胃肠醇吗gydF4y2Ba95gydF4y2Ba: 2872 - 2879。gydF4y2Ba
Frank JA, Reich CI, Sharma S, Weisbaum JS, Wilson BA, Olsen GJ。(2008)。两种常用的细菌16S rRNA基因扩增引物的关键评价。gydF4y2Ba应用环境微生物gydF4y2Ba74gydF4y2Ba: 2461 - 2470。gydF4y2Ba
弗兰克斯AH,哈森HJM, Raangs GC,詹森GJ,舒特F,韦林GW。(1998)。荧光法测定人类粪便中细菌种群的变化gydF4y2Ba原位gydF4y2Ba与群体特异性16S rrna靶向寡核苷酸探针杂交。gydF4y2Ba应用环境微生物gydF4y2Ba64gydF4y2Ba: 3336 - 3345。gydF4y2Ba
弗瑞E,麦克法兰S,肯尼迪A,卡明斯JH,沃尔什SV,奥尼尔DAgydF4y2Ba等gydF4y2Ba.(2005)。共生疗法(gydF4y2Ba双歧杆菌longumgydF4y2Ba1)启动活动性溃疡性结肠炎患者炎症的缓解:一项随机对照试点试验。gydF4y2Ba肠道gydF4y2Ba54gydF4y2Ba: 242 - 249。gydF4y2Ba
吉尔CIR,罗兰IR。(2002)。饮食和癌症:评估风险。gydF4y2BaBr J NutrgydF4y2Ba88gydF4y2Ba(补充1):S73-S87。gydF4y2Ba
Hold GL, Pryde SE, Russell VJ, Furrie E, Flint HJ。(2002)。用16S rDNA序列分析评估人类结肠样品中的微生物多样性。gydF4y2BaFEMS微生物生态gydF4y2Ba39gydF4y2Ba: 33-39。gydF4y2Ba
Johnson M, Zaretskaya I, Raytselis Y, Merezhuk Y, McGinnis S, Madden TL。(2008)。NCBI BLAST:一个更好的网页界面。gydF4y2Ba核酸测定gydF4y2Ba36gydF4y2Ba: W5-W9。gydF4y2Ba
科瓦切瓦-达查里P,埃格特M,马图伊斯A,拉吉里奇-斯托亚诺维奇M,德格拉夫AA,史密特HgydF4y2Ba等gydF4y2Ba.(2009)。淀粉发酵与细菌系统发育关系的研究gydF4y2Ba在体外gydF4y2Ba以rna为基础的稳定同位素探测大肠模型。gydF4y2Ba环境MicrobiolgydF4y2Ba11gydF4y2Ba: 914 - 926。gydF4y2Ba
井野T,森K,田中K,铃木K- i,原山S。(2007)。gydF4y2BaOscillibacter valericigenesgydF4y2Ba一种产戊酸的厌氧细菌,从日本蛤的消化道中分离出来。gydF4y2BaInt J系统进化微生物gydF4y2Ba57gydF4y2Ba: 1840 - 1845。gydF4y2Ba
劳伯CL,周N,纪高登,奈特R,菲勒N。(2010)。储存条件对土壤和人类相关样品中细菌群落结构评估的影响。gydF4y2BaFEMS微生物莱特gydF4y2Ba307gydF4y2Ba: 80 - 85。gydF4y2Ba
劳利TD,克莱尔S,沃克AW,古尔丁D,斯塔布勒RA,裘槎NgydF4y2Ba等gydF4y2Ba.(2009)。抗生素治疗gydF4y2Ba艰难梭状芽胞杆菌gydF4y2Ba携带小鼠在免疫功能低下的宿主中引发超级脱落状态、孢子介导的传播和严重疾病。gydF4y2Ba感染ImmungydF4y2Ba77gydF4y2Ba: 3661 - 3669。gydF4y2Ba
Leitch ECM, Walker AW, Duncan SH, Holtrop G, Flint HJ。(2007)。人类结肠细菌对不溶性底物的选择性定植。gydF4y2Ba环境MicrobiolgydF4y2Ba72gydF4y2Ba: 667 - 679。gydF4y2Ba
黎璐RK,胡勇,Brown IL, Young GP。(2009)。高直链淀粉对大鼠结肠发酵及dna损伤凋亡反应的影响。gydF4y2BaBMC Nutr MetabgydF4y2Ba6gydF4y2Ba: 11-19。gydF4y2Ba
李雷,滕宝PJ,克莱因S,高登JI。(2006)。微生物生态学——与肥胖相关的人类肠道微生物。gydF4y2Ba自然gydF4y2Ba444gydF4y2Ba: 1022 - 1023。gydF4y2Ba
李志强,杨永平,李志强,李志强。(2010)。丁基辅酶a:乙酸辅酶a转移酶基因分析揭示了人结肠产生丁酸盐细菌的多样性。gydF4y2Ba环境MicrobiolgydF4y2Ba12gydF4y2Ba: 304 - 314。gydF4y2Ba
路德维希W,斯特伦克O,韦斯特拉姆R,里希特L,迈耶H,亚胡库玛尔gydF4y2Ba等gydF4y2Ba.(2004)。ARB:序列数据的软件环境。gydF4y2Ba核酸测定gydF4y2Ba32gydF4y2Ba: 1363 - 1371。gydF4y2Ba
麦克法兰GT,英国人HN。(1986)。人类大肠菌群对淀粉的利用。gydF4y2BaJ应用抗菌gydF4y2Ba60gydF4y2Ba: 195 - 201。gydF4y2Ba
麦凯·李,阿米诺夫·李,胡·W,克利夫·AV,欧韦克·D,桑德西特·马gydF4y2Ba等gydF4y2Ba.(2003)。未开垦生态gydF4y2BaOscillospiragydF4y2Ba牛、羊和驯鹿瘤胃中的物种用显微镜和分子方法评估。gydF4y2Ba应用环境微生物gydF4y2Ba69gydF4y2Ba: 6808 - 6815。gydF4y2Ba
麦金太尔AP,吉布森P,杨GP。(1993)。在肠道模型中膳食纤维产生丁酸盐和预防大肠癌。gydF4y2Ba肠道gydF4y2Ba34gydF4y2Ba: 386 - 391。gydF4y2Ba
摩尔WEC,摩尔LH。(1995)。结肠癌高危人群的肠道菌群。gydF4y2Ba应用环境微生物gydF4y2Ba61gydF4y2Ba: 3202 - 3207。gydF4y2Ba
Polednak美联社报道。(2003)。美国肥胖相关癌症的发病率趋势gydF4y2Ba癌症检测gydF4y2Ba27gydF4y2Ba: 415 - 421。gydF4y2Ba
Ramirez-Farias C, Slezak K, Fuller Z, Duncan A, Holtrop G, Louis P。(2009)。菊粉对人体肠道菌群的影响:刺激gydF4y2Ba双歧杆菌adolescentisgydF4y2Ba而且gydF4y2BaFaecalibacterium prausnitziigydF4y2Ba.gydF4y2BaBr J NutrgydF4y2Ba101gydF4y2Ba: 541 - 550。gydF4y2Ba
Ramsay AG, Scott KP, Martin CJ, Rincon MT, Flint HJ。(2006)。来自人类结肠的产丁酸厚壁菌的细胞相关α-淀粉酶。gydF4y2Ba微生物学gydF4y2Ba152gydF4y2Ba: 3281 - 3290。gydF4y2Ba
罗伯特C,伯纳利-多纳迪尔A。(2003)。人体结肠的纤维素分解菌群:甲烷排泄对象中微晶纤维素降解细菌的证据。gydF4y2BaFEMS微生物生态gydF4y2Ba46gydF4y2Ba: 81 - 89。gydF4y2Ba
Robertson MD, Bickerton AS, Dennis AL, Vidal H, Frayn KN。(2005)。膳食抗性淀粉的胰岛素增敏作用及对骨骼肌和脂肪组织代谢的影响。gydF4y2BaJ是clinin Nutr吗gydF4y2Ba82gydF4y2Ba: 559 - 567。gydF4y2Ba
Salyers AA, West SEH, Vercellotti JR, Wilkins TD。(1977)。人体结肠厌氧细菌发酵粘蛋白和植物多糖。gydF4y2Ba应用环境微生物gydF4y2Ba34gydF4y2Ba: 529 - 533。gydF4y2Ba
施洛斯PD, Handelsman J。(2005)。介绍DOTUR,一个定义操作分类单位和估计物种丰富度的计算机程序。gydF4y2Ba应用环境微生物gydF4y2Ba71gydF4y2Ba: 1501 - 1506。gydF4y2Ba
施洛斯PD,韦斯科特SL,里亚宾T,霍尔JR,哈特曼M,霍利斯特EBgydF4y2Ba等gydF4y2Ba.(2009)。介绍mother:开源、平台独立、社区支持的软件,用于描述和比较微生物群落。gydF4y2Ba应用环境微生物gydF4y2Ba75gydF4y2Ba: 7537 - 7541。gydF4y2Ba
许维兹,李志强,李志强,李志强。(2002)。抗性淀粉对短链脂肪酸产量及丁酸生成细胞计数的影响gydF4y2Ba真细菌gydF4y2Ba在人的肠道里。gydF4y2Ba应用微生物gydF4y2Ba93gydF4y2Ba: 157 - 162。gydF4y2Ba
Schwiertz A, Tara D, Schafer K, Beijer S, Bos NA, Donus CgydF4y2Ba等gydF4y2Ba.(2010)。瘦和超重健康受试者的微生物区系和短链脂肪酸。gydF4y2Ba肥胖gydF4y2Ba18gydF4y2Ba: 190 - 195。gydF4y2Ba
Sokol H, Pigneur B, Watterlot L, Lakhdari O, Bermúdez-Humarán LG, Gratadoux JgydF4y2Ba等gydF4y2Ba.(2008)。gydF4y2BaFaecalibacterium prausnitziigydF4y2Ba是一种抗炎共生细菌,通过克罗恩病患者肠道菌群分析确定。gydF4y2Ba美国国家科学研究院gydF4y2Ba105gydF4y2Ba: 16731 - 16736。gydF4y2Ba
Stephen AM, Wiggins HS, Cummings JH。(1987)。改变转运时间对人体结肠微生物代谢的影响。gydF4y2Ba肠道gydF4y2Ba28gydF4y2Ba: 601 - 609。gydF4y2Ba
Suau A, Bonnet R, Sutren M, Godon JJ, Gibson GR, Collins MDgydF4y2Ba等gydF4y2Ba.(1999)。对来自复杂群体的编码16S rRNA的基因的直接分析揭示了人类肠道内许多新的分子物种。gydF4y2Ba应用环境微生物gydF4y2Ba24gydF4y2Ba: 4799 - 4807。gydF4y2Ba
点击J, Mondot S, Levenez F, Pelletier E, Caron C, Furet JPgydF4y2Ba等gydF4y2Ba.(2009)。朝着人类肠道菌群系统发育核心。gydF4y2Ba环境MicrobiolgydF4y2Ba11gydF4y2Ba: 2574 - 2584。gydF4y2Ba
特恩堡PJ,巴克德F,富尔顿L,戈登JI。(2008)。饮食引起的肥胖与小鼠远端肠道微生物群显著但可逆的改变有关。gydF4y2Ba细胞宿主微生物gydF4y2Ba3.gydF4y2Ba: 213 - 223。gydF4y2Ba
沃克AW,邓肯SH,哈德森HJM,霍特罗普G,韦林GW,弗林特HJ。(2008)。人类肠道微生物群的物种组成在颗粒相关和液相群落之间有所不同。gydF4y2Ba环境MicrobiolgydF4y2Ba10gydF4y2Ba: 3275 - 3283。gydF4y2Ba
王x, Conway PL, Brown IL, Evans AJ。(1999)。gydF4y2Ba在体外gydF4y2Ba人类结肠细菌对支链淀粉和高直链玉米淀粉粒的利用。gydF4y2Ba应用环境微生物gydF4y2Ba65gydF4y2Ba: 4848 - 4854。gydF4y2Ba
余捷,克莱顿MK。(2005)。一种基于物种比例的相似性度量。gydF4y2Ba公共统计Theo方法gydF4y2Ba34gydF4y2Ba: 2123 - 2131。gydF4y2Ba
Zoetendal EG, Akkermans ADL, de Vos WM。(1998)。从人类粪便样本中提取16S rRNA的温度梯度凝胶电泳分析揭示了稳定的和宿主特异性的活性细菌群落。gydF4y2Ba应用环境微生物gydF4y2Ba64gydF4y2Ba: 3854 - 3859。gydF4y2Ba
张华,DiBaise JK, Zuccolo A, Kudma D, Braidotti M, Yu YgydF4y2Ba等gydF4y2Ba.(2008)。肥胖及胃分流术后人体肠道菌群。gydF4y2Ba美国国家科学研究院gydF4y2Ba106gydF4y2Ba: 2365 - 2370。gydF4y2Ba
确认gydF4y2Ba
我们感谢世界癌症研究基金会对该项目的支持。罗维特营养与健康研究所(阿伯丁大学)和苏格兰生物数学与统计研究所得到了苏格兰政府农村环境研究与分析理事会的支持。我们感谢Claire Fyfe和RINH人类研究单位。我们也感谢David Harris和他在Wellcome Trust Sanger研究所的团队的其他成员,他们生成了16S rRNA基因序列。资助AWW、MDS、PS、JP和测序的是The Wellcome Trust(批准号:no。WT 76964)。gydF4y2Ba
作者信息gydF4y2Ba
作者及隶属关系gydF4y2Ba
相应的作者gydF4y2Ba
额外的信息gydF4y2Ba
补充信息gydF4y2Ba这篇论文发表在ISME期刊网站上gydF4y2Ba
权利和权限gydF4y2Ba
关于本文gydF4y2Ba
引用本文gydF4y2Ba
沃克,A,因斯,J,邓肯,S。gydF4y2Baet al。gydF4y2Ba人类结肠菌群中的优势菌群和饮食反应菌群。gydF4y2BaISME JgydF4y2Ba5gydF4y2Ba, 220-230(2011)。https://doi.org/10.1038/ismej.2010.118gydF4y2Ba
收到了gydF4y2Ba:gydF4y2Ba
修改后的gydF4y2Ba:gydF4y2Ba
接受gydF4y2Ba:gydF4y2Ba
发表gydF4y2Ba:gydF4y2Ba
发行日期gydF4y2Ba:gydF4y2Ba
DOIgydF4y2Ba:gydF4y2Bahttps://doi.org/10.1038/ismej.2010.118gydF4y2Ba
关键字gydF4y2Ba
- 人类结肠gydF4y2Ba
- 抗性淀粉gydF4y2Ba
- 16 s rRNAgydF4y2Ba
- phylotypesgydF4y2Ba
- 瘤胃球菌属gydF4y2Ba
- 时间改变gydF4y2Ba
这篇文章被引用gydF4y2Ba
肥胖和周围神经病变小鼠模型中的肠道微生物群与血浆和神经脂质组学和神经转录组学相关gydF4y2Ba
微生物组gydF4y2Ba(2023)gydF4y2Ba
心脏代谢健康,饮食和肠道微生物组:元组学的观点gydF4y2Ba
自然医学gydF4y2Ba(2023)gydF4y2Ba
利用地热球菌淀粉酶酶修饰大米淀粉对肠道菌群的调节gydF4y2Ba
食品科学与生物技术gydF4y2Ba(2023)gydF4y2Ba
无谷蛋白饮食干预后肠道菌群的变化并不介导β细胞的保存gydF4y2Ba
DiabetologiagydF4y2Ba(2023)gydF4y2Ba
饮食,肠道菌群和代谢物gydF4y2Ba
PhenomicsgydF4y2Ba(2023)gydF4y2Ba