文摘gydF4y2Ba
脂多糖内毒素是唯一已知的细菌的产品,当皮下注入到老鼠在其纯净的形式,能引起肥胖和胰岛素抵抗通过inflammation-mediated通路。在这里,我们表明,endotoxin-producing细菌隔绝一个病态肥胖人的肠道引起肥胖和胰岛素抵抗在无菌的老鼠。的endotoxin-producinggydF4y2Ba肠杆菌属gydF4y2Ba降低相对丰度从志愿者的肠道细菌降到35%,在此期间志愿者失去了51.4公斤174.8公斤初始重量和恢复从23周后高血糖和高血压饮食的全谷类,中国传统药用食品和益生元。大量减少肠道内毒素生物合成基因的志愿者与循环内毒素降低负载和缓解炎症。Mono-association的无菌的C57BL / 6 j小鼠与压力gydF4y2Ba肠杆菌属下水道gydF4y2BaB29孤立于志愿者的肠道诱导发育完全了肥胖和胰岛素抵抗在高脂饮食而不是正常食物的饮食,而无菌的控制小鼠高脂饮食也表现出不同的疾病表型。的gydF4y2Ba肠杆菌属gydF4y2Ba全身肥胖的老鼠显示增加血清内毒素负载和加重炎症条件。obesity-inducing能力的人为内毒素生产商无菌老鼠表明它可能病因导致的人类宿主肥胖的发展。gydF4y2Ba
主要gydF4y2Ba
肠道微生物群的作用在肥胖的发病机制出现了一个重要的研究领域(gydF4y2BaBackhed et al ., 2004gydF4y2Ba)。肠道革兰氏阴性机会病原体可能是肥胖的关键(gydF4y2Ba舒曼et al ., 1990gydF4y2Ba;gydF4y2BaZhang et al ., 2010gydF4y2Ba,gydF4y2Ba2012年gydF4y2Ba)。脂多糖(LPS)内毒素纯化gydF4y2Ba大肠杆菌gydF4y2Ba诱导肥胖和胰岛素抵抗表型浓度与皮下注入到老鼠时可以发现高脂肪饮食的小鼠模型(HFD)全身肥胖(gydF4y2BaCani et al ., 2007gydF4y2Ba)。Endotoxin-induced炎症的发展似乎是必不可少的肥胖和胰岛素抵抗的表型小鼠模型包括有限合伙人输液,CD14-knockout老鼠注入内毒素后没有开发这些表型(gydF4y2BaCani et al ., 2007gydF4y2Ba)。流行病学研究表明增加人口内毒素生产者和高架内毒素负载在不同的肥胖人群(gydF4y2Ba莱佩尔et al ., 2007gydF4y2Ba;gydF4y2BaRuiz et al ., 2007gydF4y2Ba;gydF4y2BaMoreno-Navarrete et al ., 2011gydF4y2Ba),但实验证据的内毒素生产商有决定性作用在人类肥胖是缺乏。gydF4y2Ba
在我们的临床研究,我们发现gydF4y2Ba肠杆菌属gydF4y2Ba、一种机会,endotoxin-producing病原体(gydF4y2Ba桑德斯和桑德斯,1997年gydF4y2Ba),由35%的肠道细菌在病态肥胖志愿者(体重174.8公斤,体重指数58.8公斤米gydF4y2Ba−2gydF4y2Ba)患有糖尿病、高血压和其他严重代谢恶化(gydF4y2Ba表1gydF4y2Ba)。9周后志愿者失去了30.1公斤,51.4公斤23周后,节食组成的全谷类,中国传统药用食品和益生元(WTP的饮食,gydF4y2Ba补充信息gydF4y2Ba;gydF4y2Ba补充图1gydF4y2Ba),与持续改善高胰岛素血症、高血糖和高血压,直到大部分代谢参数提高到正常范围(gydF4y2Ba表1gydF4y2Ba)。9周后WTP的饮食,这一点gydF4y2Ba肠杆菌属gydF4y2Ba人口志愿者肠道减少至1.8%,并成为察觉到年底23-week试验,如克隆库所示分析(gydF4y2Ba表1gydF4y2Ba;gydF4y2Ba补充图2和图3gydF4y2Ba)。serum-endotoxin负载,测量LPS-binding蛋白(gydF4y2Ba舒曼et al ., 1990gydF4y2Ba),减肥期间显著下降,随着大量改善炎症,降低白细胞介素- 6和增加脂联素水平(gydF4y2Ba表1gydF4y2Ba)。宏基因组测序的志愿者粪便样本(0)9日和23周WTP饮食证实,在减肥期间,gydF4y2Ba肠杆菌科gydF4y2Ba家庭是最显著降低人口(gydF4y2Ba补充图4gydF4y2Ba)。丰富的25 KEGG Orthologies有限合伙人参与生物合成途径大幅减少,在一起表示显著减少endotoxin-producing能力的志愿者的干预后肠道微生物群(gydF4y2Ba补充数据5 - 7gydF4y2Ba)。根据以前报道的关键作用,木糖醇代谢疾病的老鼠(gydF4y2BaCani et al ., 2007gydF4y2Ba),我们假设这endotoxin-producinggydF4y2Ba肠杆菌属gydF4y2Ba人口可能有决定性作用在人类宿主的代谢恶化。确认致病作用可能在肥胖的开发中,我们证实科赫的假设在一个实验主机与一个孤立的应变gydF4y2Ba肠杆菌属gydF4y2Ba人口(gydF4y2Ba埃文斯,1976gydF4y2Ba)。然后我们获得一个临床分离(B29)志愿者粪便样本通过“sequence-guided隔离”计划(gydF4y2Ba灵巧的et al ., 2002gydF4y2Ba;gydF4y2Ba补充图8gydF4y2Ba),并确认gydF4y2Ba肠杆菌属下水道gydF4y2Ba通过生化测试和16 s rrna基因测序(gydF4y2Ba补充表1gydF4y2Ba)。我们进行全基因组测序B29,和系统发育分析使用CVTree (gydF4y2BaQi et al ., 2004gydF4y2Ba),确定其最近邻gydF4y2Ba大肠下水道gydF4y2Ba无性系种群。gydF4y2Ba下水道gydF4y2Ba写明ATCC 13047 (gydF4y2Ba补充信息gydF4y2Ba)。一个鲎变形细胞溶解产物试验表明,B29有限合伙人有很强的内毒素活动(gydF4y2Ba补充图9gydF4y2Ba有限合伙人)和基因组序列草案显示生物合成基因类似metagenome从第0天粪便样本(gydF4y2Ba补充图10gydF4y2Ba)。gydF4y2Ba
先前的研究表明,无菌的老鼠是抵抗HFD-induced肥胖(gydF4y2BaBackhed et al ., 2007gydF4y2Ba;gydF4y2Ba丁et al ., 2010gydF4y2Ba;gydF4y2BaRabot et al ., 2010gydF4y2Ba)。测试是否B29可以克服这种阻力与肥胖通过殖民无菌的小鼠的肠道(gydF4y2Ba补充图11gydF4y2Ba),我们接种10gydF4y2Ba10gydF4y2Ba细胞B29第一周每天都到6 - 10周大无菌的C57BL / 6 j小鼠(gydF4y2BangydF4y2Ba每组= 7)在正常饮食(非传染性疾病)或HFD。我们观察到轻微的体重减少小鼠接种时期(gydF4y2Ba补充数据11 - 14gydF4y2Ba)。每组一个老鼠死于接种的易位B29成各种器官(gydF4y2Ba桑德斯和桑德斯,1997年gydF4y2Ba;gydF4y2Ba补充表2gydF4y2Ba)。第一周后,HFD-fed无菌老鼠接种B29 (HFD + B29)显示稳定的体重增加,直到最终达到一个肥胖的状态与HFD-fed常规老鼠(gydF4y2BangydF4y2Ba每组= 8;gydF4y2BaFigures1a-cgydF4y2Ba;gydF4y2Ba补充数据14 - 17gydF4y2Ba)。过多的脂肪堆积在HFD + B29无菌老鼠与脂肪代谢的改变包括leptin-resistant表型,回肠fasting-induced脂肪因子的表达,减少和乙酰辅酶a羧化酶1的表达增加,脂肪酸合酶和过氧物酶体proliferator-activated receptor-gamma基因在肝脏(gydF4y2Ba补充数据18日至19日gydF4y2Ba;gydF4y2BaBackhed et al ., 2004gydF4y2Ba,gydF4y2Ba2007年gydF4y2Ba)。HFD + B29无菌老鼠开发最重要的胰岛素抗性表型所示的口服葡萄糖耐量试验和2 h后负载胰岛素水平的试验(gydF4y2Ba图1 d和egydF4y2Ba)。这组也有最大的增加肝脏和脾脏重量和最大的减少盲肠体重(gydF4y2Ba补充表3gydF4y2Ba)。NCD-fed小鼠接种B29(非传染性疾病+ B29)或Luria-Bertani(磅)中(非传染性疾病+磅)保持精益在整个试验(gydF4y2Ba图1 a - cgydF4y2Ba)。的HFD-fed无菌的小鼠接种磅(HFD +磅)经历了显著的体重在前9周但最终成为没有不同,根据肥胖参数测试,从年底NCD-fed组16周的试验中,除了适度增加附睾的脂肪垫和一个低水平的胰岛素抵抗(gydF4y2Ba补充图14gydF4y2Ba;gydF4y2Ba图1 b和dgydF4y2Ba)。我们重复的动物测试HFD-fed无菌老鼠mono-associated B29证实单个内毒素生产商如B29函数在整个微生物群的能力诱导肥胖和胰岛素抵抗表型(gydF4y2Ba补充图20gydF4y2Ba)。接种6 - 10周大无菌的老鼠(gydF4y2BangydF4y2Ba每组)= 4 - 6株gydF4y2Ba动物双歧杆菌gydF4y2Ba通过交替的非传染性疾病和HFD喂养没有诱导肥胖表现型相同(gydF4y2Ba补充图21gydF4y2Ba),这表明肥胖不能引入任何细菌引起的无菌的老鼠在HFD喂食。gydF4y2Ba
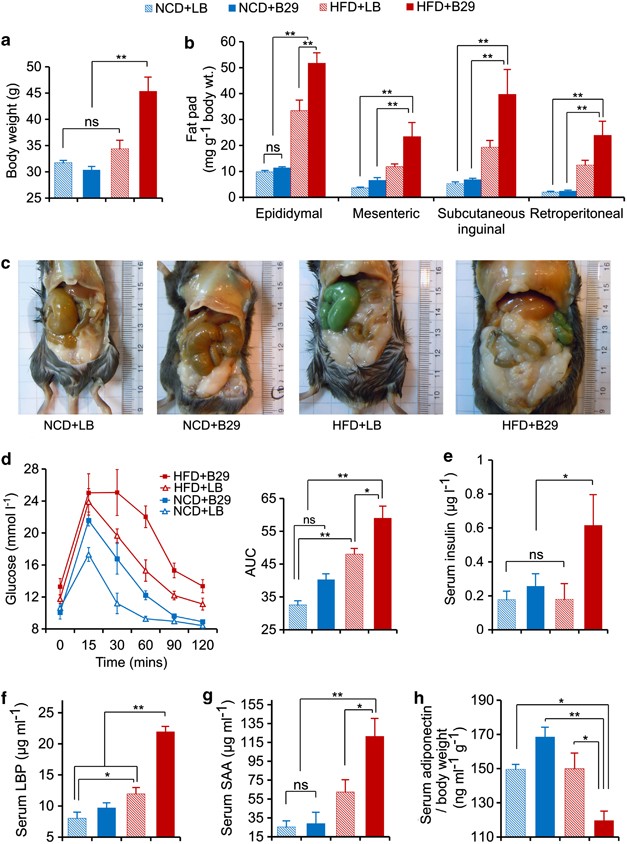
无菌老鼠mono-associated与gydF4y2Ba大肠下水道gydF4y2BaB29变得肥胖和胰岛素抵抗与内毒素增加负载和HFD喂养下引发系统性炎症(接种后16周结束时收集的数据)。(gydF4y2Ba一个gydF4y2Ba)体重;(gydF4y2BabgydF4y2Ba)附睾的质量、肠系膜皮下腹股沟和腹膜后脂肪垫;(gydF4y2BacgydF4y2Ba)腹部照片;(gydF4y2BadgydF4y2Ba)口服葡萄糖耐量试验(OGTT)和曲线下的面积(AUC)血浆葡萄糖;(gydF4y2BaegydF4y2Ba)血清2 h后负载胰岛素;(gydF4y2BafgydF4y2Ba酶联免疫吸附试验(ELISA)分析血清LPS-binding蛋白质(LBP);(gydF4y2BaggydF4y2Ba)血清淀粉样蛋白A (SAA);和(gydF4y2BahgydF4y2Ba)脂联素纠正体重。双向方差分析(方差分析)发现了一个显著的影响,gydF4y2BaPgydF4y2BaB29(< 0.01),显著的影响gydF4y2BaPgydF4y2Ba< 0.01)和一个重要的饮食×B29交互效应(gydF4y2BaPgydF4y2Ba< 0.01)体重,附睾的质量,肠系膜,皮下腹股沟和腹膜后脂肪垫,血清枸杞多糖;一个重要的影响饮食(gydF4y2BaPgydF4y2BaB29(< 0.01)和一个显著的影响gydF4y2BaPgydF4y2BaOGTT < 0.01);显著影响B29 (gydF4y2BaPgydF4y2Ba< 0.05)在血清2 h后负载胰岛素。数据显示为意味着±s.e.m。(gydF4y2BangydF4y2Ba= 6)。NS,无显著差异;*gydF4y2BaPgydF4y2Ba< 0.05;* *gydF4y2BaPgydF4y2Ba< 0.01。颜色代码动物组:非传染性疾病+磅,蓝色削减;非传染性疾病+ B29,蓝色;HFD +磅,红色斜线;HFD + B29,红色。磅,Luria-Bertani媒介。gydF4y2Ba
稍微增加了内毒素负载可以诱导低级,慢性炎症作为胰岛素抵抗的驱动力和改变小鼠的脂肪代谢(gydF4y2Ba格et al ., 1996gydF4y2Ba;gydF4y2BaCani et al ., 2007gydF4y2Ba)。血清LPS-binding蛋白显著高于在HFD + B29无菌老鼠比非传染性疾病+ B29无菌老鼠(gydF4y2Ba图1 fgydF4y2Ba),尽管B29达到显著更大的人口规模的肠道NCD-fed无菌老鼠(gydF4y2Ba补充图13gydF4y2Ba)。B29是唯一有限合伙人生产商在小鼠肠道(gydF4y2Ba补充图22gydF4y2Ba),增加serum-endotoxin载入HFD + B29无菌老鼠只能来自B29。的基因表达水平两个紧密连接蛋白occludin和ZO-1 (gydF4y2BaCani et al ., 2008gydF4y2Ba在回肠各组之间没有显著差异(gydF4y2Ba补充图23gydF4y2Ba),从肠道内毒素易位的高数量的血清HFD + B29无菌老鼠可以促进HFD乳糜微粒引起的长链脂肪酸(gydF4y2BaCani et al ., 2007gydF4y2Ba;gydF4y2BaGhoshal et al ., 2009gydF4y2Ba),而不是通过肠道屏障功能受损(gydF4y2BaCani et al ., 2007gydF4y2Ba;gydF4y2BaZhang et al ., 2010gydF4y2Ba,gydF4y2Ba2012年gydF4y2Ba)。依照内毒素增加负载,HFD + B29无菌的最伟大的增加小鼠血清淀粉样蛋白水平和最大的脂联素的分泌减少,这也暗示了这些老鼠全身炎症(数量增加最多的gydF4y2Ba图1 g和hgydF4y2Ba)。interleukin-1β,肿瘤坏死因子-α的表达白细胞介素- 6,我κB激酶ε和toll样受体4炎性基因显著增加在肝脏和附睾脂肪垫回肠的但不是HFD + B29无菌老鼠(gydF4y2Ba补充图24gydF4y2Ba),表明诱导炎症在前两个组织,但不是在肠道,相比以前的报告(gydF4y2Ba丁et al ., 2010gydF4y2Ba)。HFD +磅无菌的老鼠适度更高水平的血清血清淀粉样蛋白A和肝脏肿瘤坏死因子-α的表达比NCD-fed组,这表明HFD诱导宿主炎症(gydF4y2BaTripathy et al ., 2003gydF4y2Ba然而,),这是远低于B29引起的。综上所述,我们的研究结果表明,endotoxin-induced炎症可能引起肥胖的关键作用gydF4y2Ba大肠下水道gydF4y2BaB29,支持一个假定的因果关系链的存在从肠道内毒素生产商肥胖端点。gydF4y2Ba
无菌的老鼠被广泛用于肥胖的研究。例如,戈登gydF4y2Baet al。gydF4y2Ba显示,与植物polysaccharide-fermenting co-inoculation无菌的老鼠gydF4y2Ba叫多形拟杆菌gydF4y2Ba和产甲烷gydF4y2BaMethanobrevibacter smithiigydF4y2Ba显著提高附睾脂肪垫而不是总体重(gydF4y2Ba撒母耳和戈登,2006gydF4y2Ba)。一步,我们研究了程序修改从科赫法则(gydF4y2Ba埃文斯,1976gydF4y2Ba),首次建立了小鼠肥胖模型结合HFD human-originated内毒素生产国。这项工作表明,endotoxin-producing肠道细菌的生长是一个因素,而不是一个结果,在人类宿主代谢恶化。事实上,这一毒株B29是人类肥胖可能不是唯一的因素gydF4y2Ba在活的有机体内gydF4y2Ba,它的相对贡献需要评估。然而,按照协议建立在这项研究中,我们希望确定更多这样obesity-inducing细菌从各种人群,更好地了解相互作用的分子机制与其他肠道微生物群的成员,饮食和宿主肥胖,和开发新的策略减少毁灭性的代谢疾病的流行。gydF4y2Ba
引用gydF4y2Ba
王Backhed F,丁H, T, Hooper LV, Koh GY,纳吉gydF4y2Ba等gydF4y2Ba。(2004)。肠道微生物群作为一个环境因素调节脂肪存储。gydF4y2Ba《美国国家科学院刊gydF4y2Ba101年gydF4y2Ba:15718 - 15723。gydF4y2Ba
Backhed F,曼彻斯特JK Semenkovich CF,戈登霁。(2007)。机制在无菌鼠抗食源性肥胖。gydF4y2Ba《美国国家科学院刊gydF4y2Ba104年gydF4y2Ba:979 - 984。gydF4y2Ba
马Cani PD, Amar J·伊格莱西亚斯,Poggi M,可耐福C, Bastelica DgydF4y2Ba等gydF4y2Ba。(2007)。代谢内毒素发起肥胖和胰岛素抵抗。gydF4y2Ba糖尿病gydF4y2Ba56gydF4y2Ba:1761 - 1772。gydF4y2Ba
Cani PD,米罗•R,可耐福C, Waget, Neyrinck, Delzenne NMgydF4y2Ba等gydF4y2Ba。(2008)。改变肠道微生物群控制代谢endotoxemia-induced炎症在老鼠的脂肪食源性肥胖和糖尿病。gydF4y2Ba糖尿病gydF4y2Ba57gydF4y2Ba:1470 - 1481。gydF4y2Ba
丁,x毫米,短桨BP Rigby R, Schwerbrock NM,格尼斯年代gydF4y2Ba等gydF4y2Ba。(2010)。高脂肪饮食:细菌相互作用促进肠道炎症之前和与肥胖和胰岛素抵抗在鼠标。gydF4y2Ba《公共科学图书馆•综合》gydF4y2Ba5gydF4y2Ba:e12191。gydF4y2Ba
埃文斯。(1976)。因果关系和疾病:Henle-Koch假设再现。gydF4y2Ba耶鲁J杂志gydF4y2Ba49gydF4y2Ba:175 - 195。gydF4y2Ba
Ghoshal SJ, Witta J,钟J, de Villiers W,堪称" E。(2009)。乳糜微粒促进肠道吸收的脂多糖。gydF4y2BaJ脂质物gydF4y2Ba50gydF4y2Ba:90 - 97。gydF4y2Ba
格GS, Peraldi P Budavari,埃利斯R,白色的MF, Spiegelman BMgydF4y2Ba等gydF4y2Ba。(1996)。IRS-1-mediated抑制胰岛素受体酪氨酸激酶活动在tnf -和obesity-induced胰岛素抵抗。gydF4y2Ba科学gydF4y2Ba271年gydF4y2Ba:665 - 668。gydF4y2Ba
莱佩尔点,舒曼C, Triantafilou K, Rasche调频,舒斯特尔T,弗兰克·HgydF4y2Ba等gydF4y2Ba。(2007)。协会lipopolysaccharide-binding蛋白质和男性冠状动脉疾病。gydF4y2BaJ是科尔心功能杂志gydF4y2Ba50gydF4y2Ba:25-31。gydF4y2Ba
Moreno-Navarrete JM,奥尔特加F, Serino M, Luche E, Waget, Pardo GgydF4y2Ba等gydF4y2Ba。(2011)。循环lipopolysaccharide-binding蛋白质(LBP)是一个与肥胖相关胰岛素抵抗的标志。gydF4y2BaInt J ob (Lond)gydF4y2Ba36gydF4y2Ba:1442 - 1449。gydF4y2Ba
罗七J, H,郝B。(2004)。CVTree:基于全基因组的种系发生树重建工具。gydF4y2Ba核酸ResgydF4y2Ba32gydF4y2Ba:45-47。gydF4y2Ba
Rabot年代,Membrez M, Bruneau,杰拉德P, Harach T,莫泽MgydF4y2Ba等gydF4y2Ba。(2010)。无菌C57BL / 6 j小鼠对high-fat-diet-induced胰岛素抵抗和改变胆固醇代谢。gydF4y2Ba美国实验生物学学会联合会JgydF4y2Ba24gydF4y2Ba:4948 - 4959。gydF4y2Ba
灵巧的女士,Connon SA Vergin KL, Giovannoni SJ。(2002)。无处不在的SAR 11培养海洋bacterioplankton进化枝。gydF4y2Ba自然gydF4y2Ba418年gydF4y2Ba:630 - 633。gydF4y2Ba
Ruiz AG) Casafont F,克雷斯波J, Cayon,马约加米,EstebanezgydF4y2Ba等gydF4y2Ba。(2007)。Lipopolysaccharide-binding蛋白血浆和肝脏tnf基因表达水平在肥胖病人:潜在作用的证据内毒素在非酒精性脂肪肝的发病机制。gydF4y2Baob杂志gydF4y2Ba17gydF4y2Ba:1374 - 1380。gydF4y2Ba
塞缪尔·b,戈登霁。(2006)。人源化小鼠模型的host-archaeal-bacterial互利共生。gydF4y2Ba《美国国家科学院刊gydF4y2Ba103年gydF4y2Ba:10011 - 10016。gydF4y2Ba
桑德斯j .我们桑德斯CC。(1997)。gydF4y2Ba肠杆菌属gydF4y2Baspp。病原体将蓬勃发展的世纪。gydF4y2Ba中国Microbiol牧师gydF4y2Ba10gydF4y2Ba:220 - 241。gydF4y2Ba
老梁,舒曼RR兴吉瓦,灰色PW,赖特SD, Mathison JCgydF4y2Ba等gydF4y2Ba。(1990)。脂多糖结合蛋白的结构和功能。gydF4y2Ba科学gydF4y2Ba249年gydF4y2Ba:1429 - 1431。gydF4y2Ba
莫汉蒂Tripathy D, P, Dhindsa年代,赛义德·T, Ghanim H, AljadagydF4y2Ba等gydF4y2Ba。(2003)。海拔的游离脂肪酸诱导炎症和健康受试者的损害血管反应性。gydF4y2Ba糖尿病gydF4y2Ba52gydF4y2Ba:2882 - 2887。gydF4y2Ba
张赵张C, Y, M,彭日成X,赵王L, L。(2012)。肠道微生物群的结构弹性在成年小鼠高脂饮食扰动。gydF4y2BaISME JgydF4y2Ba6gydF4y2Ba:1848 - 1857。gydF4y2Ba
韩张张C、M,王年代,R,曹Y,华WgydF4y2Ba等gydF4y2Ba。(2010)。肠道微生物群之间的相互作用,宿主基因和代谢综合征小鼠饮食相关发展。gydF4y2BaISME JgydF4y2Ba4gydF4y2Ba:232 - 241。gydF4y2Ba
确认gydF4y2Ba
我们感谢教授r . Losick L纽豪斯,M Obin和M流行的批判阅读手稿和建议。我们也感谢以下个人援助在研究:肖,J沈,X彭日成,M, XJ, Y赵,L小王,小王,Y, G, G, H Ou, J气,JJ Wang X张,王,M的歌,J徐,H, T, Q, N赵,C, Y风扇,刘,YZ粉丝,T, Z, R Xi, XY, C, H, X, X,赵G Ning,杨和G。gydF4y2Ba
这项工作得到了国家自然科学基金的项目30730005中国(国家自然科学基金委),2008 aa02z315和2009 aa02z310 863项目,重点项目2007 dfc30450和075407001国际合作项目的资助和项目在全国科技2006 bai11b08支柱项目。gydF4y2Ba
作者信息gydF4y2Ba
作者和联系gydF4y2Ba
相应的作者gydF4y2Ba
额外的信息gydF4y2Ba
补充信息gydF4y2Ba伴随着ISME期刊上的论文网站gydF4y2Ba
补充信息gydF4y2Ba
权利和权限gydF4y2Ba
这个工作许可适用创作共用署名下衍生著作3.0 Unported许可证。查看本许可证的副本,请访问http://creativecommons.org/licenses/by-nc-nd/3.0/gydF4y2Ba
关于这篇文章gydF4y2Ba
引用这篇文章gydF4y2Ba
范,N。,Zhao, L. An opportunistic pathogen isolated from the gut of an obese human causes obesity in germfree mice.ISME JgydF4y2Ba7gydF4y2Ba,880 - 884 (2013)。https://doi.org/10.1038/ismej.2012.153gydF4y2Ba
收到了gydF4y2Ba:gydF4y2Ba
修改后的gydF4y2Ba:gydF4y2Ba
接受gydF4y2Ba:gydF4y2Ba
发表gydF4y2Ba:gydF4y2Ba
发行日期gydF4y2Ba:gydF4y2Ba
DOIgydF4y2Ba:gydF4y2Bahttps://doi.org/10.1038/ismej.2012.153gydF4y2Ba
关键字gydF4y2Ba
- 肠道微生物群gydF4y2Ba
- 无菌的老鼠gydF4y2Ba
- endotoxin-producing细菌gydF4y2Ba
- 肥胖gydF4y2Ba
- 胰岛素抵抗gydF4y2Ba
- 高脂肪饮食gydF4y2Ba
本文引用的gydF4y2Ba
葡萄籽和皮肤中提取,一个潜在的生命起源以前的反肥胖通过肠道微生物群的调制效果gydF4y2Ba
肠道病原体gydF4y2Ba(2022)gydF4y2Ba
受伤是一个独立的决定因素水平在慢性脊髓损伤患者肠道失调:横断面研究gydF4y2Ba
脊髓gydF4y2Ba(2022)gydF4y2Ba
Host-microbial交互在代谢性疾病:从饮食到免疫力gydF4y2Ba
微生物学杂志gydF4y2Ba(2022)gydF4y2Ba
胰岛素抵抗与进步增加NOD1高脂肪饮食的老鼠gydF4y2Ba
内分泌gydF4y2Ba(2022)gydF4y2Ba
审查的影响肠道微生物群对代谢疾病gydF4y2Ba
档案的微生物学gydF4y2Ba(2022)gydF4y2Ba