摘要
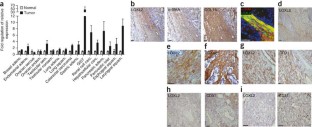
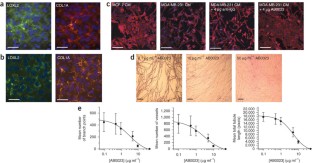
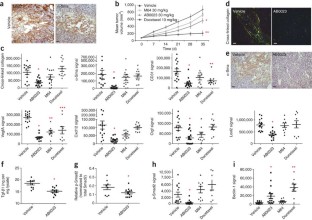
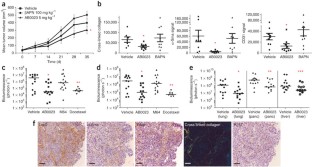
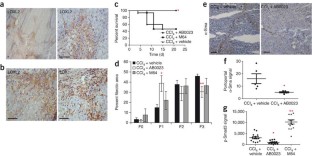
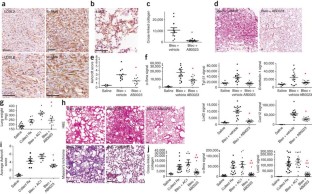
我们已经确定了基质酶赖氨酸氧化酶样2 (LOXL2)在癌症和纤维化疾病的病理微环境的产生和维持中的新作用。我们对人类肿瘤、纤维化肺和肝组织的活检分析显示,LOXL2在疾病相关间质中表达增加,在健康组织中表达有限。用抑制性单克隆抗体(AB0023)靶向LOXL2在原发性和转移性癌症异种移植模型以及肝和肺纤维化模型中都是有效的。抑制LOXL2导致激活的成纤维细胞、粘连增生和内皮细胞显著减少,生长因子和细胞因子的产生减少,转化生长因子-β (TGF-β)通路信号减弱。AB0023的性能优于小分子赖氨酸氧化酶抑制剂β-氨基固有腈。loxl2特异性AB0023的有效性和安全性代表了一种新的治疗方法,在肿瘤和纤维化疾病中具有广泛的适用性。
这是订阅内容的预览,通过你所在的机构访问
相关的文章
引用本文的开放获取文章。
靶向递送装载ZNF416 sirna的脂质体可减轻实验性肺纤维化
转化医学杂志开放获取11月12日
一个积极的机械生物学反馈回路控制心脏成纤维细胞表型的双稳态开关
细胞的发现开放获取2022年9月6日
从ECM降解角度对纤维化的新见解:巨噬细胞- mmp -ECM相互作用
细胞与生物科学开放获取2022年7月27日
访问选项
订阅这本杂志
收到12个印刷问题和在线访问
每年189.00美元
每期只要15.75美元
租或购买这篇文章
只要这篇文章,只要你需要它
39.95美元
价格可能受当地税收的影响,在结账时计算
参考文献
照射乳腺基质促进未照射上皮细胞致瘤潜能的表达。癌症Res。60, 1254-1260(2000)。
Bhowmick, n.a., Neilson, E.G., Moses, H.L.肿瘤起始和进展中的基质成纤维细胞。自然432, 332-337(2004)。
库森斯,L.M. & Werb, Z.炎症与癌症。自然420, 860-867(2002)。
库哈,g.r.,海沃德,S.W.,王永哲,和Ricke, W.A.间质微环境在前列腺癌发生中的作用。Int。j .癌症107, 1-10(2003)。
雅各布斯,t.w., Byrne, C., Colditz, G., Connolly, J.L. & Schnitt, S.J.良性乳腺活检标本中的放射状疤痕与乳腺癌的风险。心血管病。j .地中海。340, 430-436(1999)。
奥鲁米,A.F.等人。癌相关成纤维细胞直接启动人前列腺上皮的肿瘤进展。癌症Res。59, 5002-5011(1999)。
Orimo, A.等。癌症相关肌成纤维细胞具有多种促进子宫内膜肿瘤进展的因素。中国。癌症Res。7, 3097-3105(2001)。
克莱夫,J.等人。胰腺癌微环境。Int。j .癌症121, 699-705(2007)。
Cardone, A., Tolino, A., Zarcone, R., Borruto Caracciolo, G. & Tartaglia, E.促结扎反应和淋巴细胞浸润在乳腺癌治疗中的预后价值。Panminerva地中海。39, 174-177(1997)。
朱,g.c., Kimmelman, a.c., Hezel, A.F. & DePinho, R.A.胰腺癌的基质生物学。j .细胞。物化学。101, 887-907(2007)。
Conti, J.A.等人。肝结直肠腺癌转移灶周围的结缔组织形成反应通过- v整合素结扎帮助肿瘤生长和存活。中国。癌症Res。14, 6405-6413(2008)。
Maeshima, A.M.,等。改良瘢痕分级:小周围肺腺癌的预后指标。癌症95, 2546-2554(2002)。
Sappino, a.p., Skalli, O., Jackson, B., Schurch, W. & Gabbiani, G.恶性和非恶性乳腺组织间质细胞中的平滑肌分化。Int。j .癌症41, 707-712(1988)。
董,J.等。vegf缺失细胞需要PDGFRα信号介导的间质成纤维细胞募集来发生肿瘤。EMBO J。23, 2800-2810(2004)。
Hinz, B.等人。肌成纤维细胞:一个功能,多个来源。点。j .分册。170, 1807-1816(2007)。
Hlatky, L., Tsionou, C., Hahnfeldt, P. & Coleman, C.N.乳腺成纤维细胞可能通过缺氧诱导的血管内皮生长因子上调和蛋白表达影响乳腺肿瘤血管生成。癌症Res。54, 6083-6086(1994)。
Orimo, A.等。浸润性人乳腺癌中存在的基质成纤维细胞通过提高SDF-1/CXCL12分泌促进肿瘤生长和血管生成。细胞121, 335-348(2005)。
布彻,d.t.,阿利斯顿,T. &韦弗,V.M.紧张的情况:迫使肿瘤进展。Nat. Rev. Cancer9, 108-122(2009)。
乔治,P.C.等人。大鼠肝脏硬度增加先于基质沉积:纤维化的意义。点。j .杂志。Gastrointest。肝脏杂志。293, g1147-g1154(2007)。
Levental, K.R.等。基质交联通过增强整合素信号通路促进肿瘤进展。细胞139, 891-906(2009)。
Wipff, p.j., Rifkin, d.b., Meister, J.J. & Hinz, B.肌成纤维细胞收缩从细胞外基质激活潜伏的TGF-β1。J.细胞生物学。179, 1311-1323(2007)。
Suki, B., Ito, S., Stamenovic, D., Lutchen, K.R. & Ingenito, E.P.肺实质的生物力学:胶原蛋白和机械力的关键作用。j:。杂志。98, 1892-1899(2005)。
Kagan, H.M.和Li, W.赖氨酸氧化酶:性质,特异性,和细胞内外的生物学作用。j .细胞。物化学。88, 660-672(2003)。
佩恩,s.l.,亨德里克斯,M.J.和Kirschmann, D.A.赖氨酸氧化酶在癌症中的矛盾作用——一种前景。j .细胞。物化学。101, 1338-1354(2007)。
Vadasz, Z.等。肝细胞周围胶原蛋白异常沉积与肝细胞赖氨酸氧化酶和赖氨酸氧化酶样蛋白-2特异性表达有关。j .乙醇。43, 499-507(2005)。
Erler, J.T.等人。赖氨酸氧化酶是缺氧诱导转移的必要条件。自然440, 1222-1226(2006)。
Akiri, G.等人。赖氨酸氧化酶相关蛋白-1在体内促进肿瘤纤维化和肿瘤进展。癌症Res。63, 1657-1666(2003)。
方,S.F.等。赖氨酸氧化酶样2在结肠和食道肿瘤中表达增加,并与低分化的结肠肿瘤相关。Chromosom基因。癌症46, 644-655(2007)。
Hollosi, P., Yakushiji, j.k., Fong, k.s., Csiszar, K. & Fong, S.F.赖氨酸氧化酶样2促进非侵袭性乳腺癌细胞的迁移,但不促进正常乳腺上皮细胞的迁移。Int。j .癌症125, 318-327(2009)。
Kirschmann, D.A.等人。赖氨酸氧化酶在乳腺癌侵袭中的分子作用。癌症Res。62, 4478-4483(2002)。
彭,L.等。分泌的LOXL2是一种新的治疗靶点,通过Src/FAK途径促进胃癌转移。致癌作用30., 1660-1669(2009)。
罗德里格斯,H.M.等人。变构抗体抑制剂对赖氨酸氧化酶样2酶活性的调节。生物。化学。285, 20964-20974(2010)。
Peinado, H.等人。赖氨酸氧化酶样2酶在蜗牛调节和肿瘤进展中的分子作用。EMBO J。24, 3446-3458(2005)。
Lelièvre, E.等。ve -他汀/egfl7通过与赖氨酸氧化酶相互作用调节血管弹性发生。EMBO J。27, 1658-1670(2008)。
钱伯斯,A.F. MDA-MB-435和M14细胞系:相同但不是M14黑色素瘤?癌症Res。69, 5292-5293(2009)。
杨,F.等。结缔组织生长因子的间质表达促进血管生成和前列腺癌肿瘤发生。癌症Res。65, 8887-8895(2005)。
自噬在细胞死亡和肿瘤抑制机制中的作用。致癌基因23, 2891-2906(2004)。
唐,s.s., Trackman, P.C.和Kagan, H.M.主动脉赖氨酸氧化酶与β -氨基丙腈的反应。生物。化学。258, 4331-4338(1983)。
Trackman, P.C.和Kagan, H.M.非肽基胺抑制剂是赖氨酸氧化酶的底物。生物。化学。254, 7831-7836(1979)。
Jenkins, d.e., Hornig, y.s., Oei, Y., Dusich, J. & Purchio, T.允许在免疫缺陷小鼠中快速和敏感地检测乳腺肿瘤和多重转移的生物发光人乳腺癌细胞系。乳腺癌研究。7, r444-r454(2005)。
法国METAVIR合作研究小组。慢性丙型肝炎患者肝活检解释的观察者内和观察者间差异。肝脏病学20., 15-20(1994)。
Tahashi, Y.等人。大鼠急性和慢性肝损伤中肝星状细胞TGF-β信号的差异调节。肝脏病学35, 49-61(2002)。
Inagaki, Y.等。Smad3的组成性磷酸化和核定位与激活的肝星状细胞中胶原蛋白基因转录的增加相关。j .细胞。杂志。187, 117-123(2001)。
Khalil, N. & O'Connor, R.特发性肺纤维化:目前对发病机制和治疗现状的认识。医疗协会171, 153-160(2004)。
Moeller, A., Ask, K., Warburton, D., Gauldie, J. & Kolb, M.博莱霉素动物模型:研究特发性肺纤维化治疗方案的有用工具?Int。学生物化学j。细胞生物。40, 362-382(2008)。
Ashcroft, T., Simpson, J.M.和Timbrell, V.在数值尺度上估计肺纤维化严重程度的简单方法。j .中国。病理学研究。41, 467-470(1988)。
莫勒,A.等人。循环纤维细胞是特发性肺纤维化预后不良的一个指标。点。j .和。暴击。保健医疗。179, 588-594(2009)。
Park, s.h., Saleh, D., Giaid, A. & Michel, R.P.在博莱霉素诱导的肺纤维化中内皮素-1的增加和内皮素受体拮抗剂的作用。点。j .和。暴击。保健医疗。156, 600-608(1997)。
普利奇诺,A.M.等。转化生长因子β - 1驱动急性肺纤维化遗传程序的鉴定。点。j .和。细胞分子生物学39, 324-336(2008)。
徐杰,等。SDF-1/CXCR4轴在肺损伤和纤维化发病机制中的作用点。j .和。细胞分子生物学37, 291-299(2007)。
Dornhöfer, N.等。结缔组织生长因子特异性单克隆抗体治疗抑制胰腺肿瘤的生长和转移。癌症Res。66, 5816-5827(2006)。
古冷,B.等。阻断基质细胞衍生因子-1/CXCR4轴减弱在活的有机体内肿瘤生长以不依赖血管内皮生长因子的方式抑制血管生成。癌症Res。65, 5864-5871(2005)。
贝利,J.M.等人。Sonic hedgehog基因促进胰腺癌粘连增生。中国。癌症Res。14, 5995-6004(2008)。
Van Aarsen,洛杉矶等。抗体介导的整合素αvβ6阻断抑制肿瘤进展在活的有机体内通过转化生长因子β调控机制。癌症Res。68, 561-570(2008)。
葛,R.等。转化生长因子-β I型受体激酶选择性抑制剂对小鼠乳腺癌生长和转移的抑制作用在活的有机体内.中国。癌症Res。12, 4315-4330(2006)。
南,J.S.等。一种抗转化生长因子β抗体通过对多个细胞区室的协同作用抑制转移。癌症Res。68, 3835-3843(2008)。
邱,W.等。在人类乳腺癌和卵巢癌的癌症相关成纤维细胞中没有克隆性体细胞遗传改变的证据。Nat,麝猫。40, 650-655(2008)。
Constandinou, C., Henderson, N. & Iredale, J.P.啮齿动物肝纤维化建模。方法:分子医学。117, 237-250(2005)。
确认
我们感谢S. Lyle对组织病理学的指导和解释,也感谢J. Adamkewicz、S. Lyle、M. Longaker和F. McCormick对本手稿的审阅。我们感谢G. Rosen和J. Belperio对博莱霉素诱导肺纤维化研究的指导,以及G. Gurtner对伤口愈合研究设计的帮助。我们感谢J. Tambaoan对项目的支持。
作者信息
作者及隶属关系
贡献
V.B.-H。和R.S.用V.B.-H对人和小鼠组织进行免疫组化和组织学检查,并进行所有相关分析。带领免疫组化组,共同参与稿件准备工作。V.B.-H。D.M.进行转录本分析,组织采集,创面愈合模型设计并参与稿件准备,S.M.进行克隆表达并参与EMT实验和稿件准备,H.M.R.进行数据分析,IC50M.O.在肝纤维化研究中进行免疫组化分析,A.M.和M.V.进行张力实验和抗体表征,A.M.参与稿件制备,H.G.在SKOV3研究中进行免疫组化分析并参与稿件制备,C.W.进行转录本分析,C.A.G、A.C.V、b.j.、D.B.和D.T.生成,在C.A.G, J.G.的领导下,对所有抗体和蛋白质进行了定性和质量控制,进行了组织ELISA, S.Z.-E。A.H.监督MDA-MB-435小鼠研究,S.O.协助管理合同研究小组,D.T.参与毒理学研究和手稿准备,G.N.开发Y698F突变体并参与肿瘤学研究和手稿准备,P.V.V.参与实验设计和手稿准备,V.S.设计转移,纤维化和毒理学动物研究和分析,指导实验工作并撰写论文。
相应的作者
道德声明
相互竞争的利益
作为阿雷斯托生物科学公司的现任或前任员工。,R.S., D.M., S.M., H.M.R., M.O., A.M., M.V., H.G., C.W., C.A.G., A.C.V., B.J., D.B., D.T., A.H., S.O., D.T., P.V.V. & V.S. have an equity stake in the company.
补充信息
补充文字及图表
补充数据、方法及图1-7 (PDF 3481kb)
权利和权限
关于本文
引用本文
巴瑞-汉密尔顿,V.,斯潘格勒,R.,马歇尔,D.。et al。赖氨酸氧化酶样2的变构抑制阻碍病理微环境的发展。Nat地中海16, 1009-1017(2010)。https://doi.org/10.1038/nm.2208
收到了:
接受:
发表:
发行日期:
DOI:https://doi.org/10.1038/nm.2208
这篇文章被引用
从ECM降解角度对纤维化的新见解:巨噬细胞- mmp -ECM相互作用
细胞与生物科学(2022)
硅法制备酚类衍生物作为潜在的抗赖氨酸氧化酶样2酶血管生成剂
未来药学杂志(2022)
靶向递送装载ZNF416 sirna的脂质体可减轻实验性肺纤维化
转化医学杂志(2022)
染色质和转录的机械调节
自然评论遗传学(2022)
一个积极的机械生物学反馈回路控制心脏成纤维细胞表型的双稳态开关
细胞的发现(2022)
