文摘gydF4y2Ba
溶瘤细胞的病毒和主动免疫治疗作用机制互补(农业部)都是自我放大肿瘤,但剂量对主题的影响的结果还不清楚。jx - 594 (Pexa-Vec)是一种溶瘤细胞的免疫治疗牛痘病毒。确定最优jx - 594剂量的受试者晚期肝细胞癌(HCC),我们进行了一项随机2期药物剂量摸索试验(gydF4y2BangydF4y2Ba= 30)。放射科医生注入低或高剂量jx - 594肝肿瘤(天1,15 - 29);注入导致急性检测血管内jx - 594的基因组。目的肝内修改响应评估标准在实体肿瘤(mRECIST)(15%)和崔(62%)响应率和肝内疾病控制(50%)等效注入和遥远的noninjected肿瘤剂量。jx - 594复制和集落刺激因子(gm - csf)表达式之前抗癌免疫力的感应。相比肿瘤反应率和免疫端点,主体生存时间显著相关剂量(平均生存14.1个月与6.7个月的高、低剂量,分别;风险比0.39;gydF4y2BaPgydF4y2Ba= 0.020)。jx - 594证明溶瘤细胞的免疫疗法恐鸟,肿瘤反应和剂量相关肝癌患者的生存。gydF4y2Ba
主要gydF4y2Ba
尽管先进的癌症治疗与化疗和生物制剂在过去30年里,大多数实体肿瘤仍无法治愈的一旦转移。真正的新药剂与多个互补农业部要求超越适度的好处。广泛的研究领域的主动免疫疗法最近sipuleucel-t最终以批准(Provenge;Dendreon公司)和ipilimumab (Yervoy;百时美施贵宝)。尽管这些代理组成第一个批准一个新的治疗类,他们有限的长期受益权证发展主动免疫疗法更有效。溶瘤细胞的和免疫治疗单纯疱疹病毒T-Vec (Amgen),最近表达gm - csf当地瘤内注射后,证明抗癌免疫诱导和持久的客观的反应一个黑色素瘤瘤内第二阶段研究gydF4y2Ba1gydF4y2Ba。gydF4y2Ba
溶瘤细胞的免疫疗法是为了内选择性地复制,随后溶解,癌细胞gydF4y2Ba2gydF4y2Ba,gydF4y2Ba3gydF4y2Ba,gydF4y2Ba4gydF4y2Ba,gydF4y2Ba5gydF4y2Ba而诱导肿瘤特异性免疫。jx - 594(也称为Pexa-Vec;Jennerex Inc .)是一种牛痘病毒(惠氏疫苗株)病毒胸苷激酶基因的中断(gydF4y2BaTKgydF4y2Ba)对癌症的选择性和插入人类集落刺激因子(hGM-CSF)和β-galactosidase转基因免疫刺激和复制的评估,分别gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba,gydF4y2Ba8gydF4y2Ba。jx - 594的目的是诱导两种病毒replication-dependent瘤细胞溶解和肿瘤特异性免疫gydF4y2Ba6gydF4y2Ba,gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba。牛痘病毒的优势包括静脉(注射)稳定和交付gydF4y2Ba11gydF4y2Ba、增强力量gydF4y2Ba12gydF4y2Ba,丰富的安全经验作为活疫苗,演示了诱导有效的免疫反应的能力和一个大transgene-encoding能力gydF4y2Ba6gydF4y2Ba。溶瘤细胞的免疫疗法jx - 594 (Pexa-Vec) T-VEC (Amgen)gydF4y2Ba13gydF4y2Ba和一个adenoviral构建表达gm - csf (Ad-GM-CSF)gydF4y2Ba3gydF4y2Ba组成一个新的平台,优势目前批准的肿瘤免疫治疗的直接溶菌作用,诱导肿瘤特异性免疫和使用现成的产品。gydF4y2Ba
与其他代理在这个类中,jx - 594显示完整的笨重的肿瘤反应和系统性的功效在第一阶段的研究gydF4y2Ba14gydF4y2Ba,gydF4y2Ba15gydF4y2Ba。1期临床试验的瘤内jx - 594 (ref。gydF4y2Ba14gydF4y2Ba),可以预计self-amplifying剂,注射部位反应在所有剂量;然而,系统性的肿瘤反应和交付通过遥远的肿瘤的血液需要高剂量。jx - 594也需要大剂量静脉输液交付和疗效剂量输液第一阶段试验gydF4y2Ba15gydF4y2Ba。然而,到目前为止,没有随机研究试验报告这些self-amplifying主动免疫疗法。此外,证明主动免疫疗法感应与缺乏这些代理对象。这个随机试验的目标与低剂量(10比较结果gydF4y2Ba8gydF4y2Ba空斑形成单位)和高剂量(10gydF4y2Ba9gydF4y2Ba空斑形成单位)jx - 594在一个统一的先进实体瘤人口(HCC),包括安全、肝内肿瘤反应,诱导癌细胞和牛痘免疫,和整体的生存。gydF4y2Ba
结果gydF4y2Ba
主题登记和基线和治疗特点gydF4y2Ba
2008年12月至2011年5月,我们为入学筛选49科目。早期研究招生停止由一个独立的数据安全监督委员会,因为一个重要的生存支持高剂量组中获益。我们招收30主题和分层(病毒或病毒的肿瘤病因)和随机(16大剂量的胳膊,14低剂量的手臂;试验配置文件所示gydF4y2Ba补充图1gydF4y2Ba)。基线主题特征和预后因素两组之间的平衡(gydF4y2Ba表1gydF4y2Ba)。我们注意到组织之间的预后因素没有明显的统计学差异。然而,高剂量的受试者更有可能没有先前的系统性疗法,这是一种消极的预后因子(六大剂量的受试者相比,低剂量的主题没有以前的系统性治疗;gydF4y2BaPgydF4y2Ba= 0.09,确切概率法),包括以前的索拉非尼治疗(四个科目与先前的索拉非尼治疗高剂量组肿瘤恶化而在这个疗法)。gydF4y2Ba
29个话题收到了所有三个剂量;一个主题只收到了两剂,因为一个不相关的不良事件。所有受试者可评价的安全(因为他们都收到至少一剂),只有一个(由于严重的非法协议偏差,活检确诊胆管癌)可评价的生存。28受试者认为可评价的射线照相端点;这包括两位受试者临床疾病进展和死了没有扫描在第八周(以及被认为有发展)。治疗后给予jx - 594治疗和协议,根据主要调查人员报告,在两组相似;其中包括索拉非尼治疗剂量索拉非尼≥8周的两个大剂量对象和一个低剂量主题)和局部姑息疗法(两个大剂量对象和一个低剂量的主题)。gydF4y2Ba
安全性和毒性gydF4y2Ba
jx - 594在两个剂量一般耐受性良好。没有治疗相关的死亡报告。一个治疗相关的严重不良事件被报道在高剂量组(需长期住院的恶心和呕吐)。十non-treatment-related严重不良事件报告(八个主题,四大剂量和四个低剂量)。治疗相关的不良事件的等级和治疗手臂进行了总结gydF4y2Ba补充表1gydF4y2Ba。频率和年级(根据美国国家癌症研究所共同术语标准不良事件)之间的不良事件是相同的两个剂量组。流感样症状(1 - 2年级)发生在所有受试者在第一次治疗后12 - 24小时,包括发热、寒颤、恶心或呕吐。受试者治疗高剂量显示更大的温度升高后第一个jx - 594治疗相比,低剂量的受试者(gydF4y2BaPgydF4y2Ba= 0.0023,gydF4y2BatgydF4y2Ba测试)和厌食症有更高的发生率(31%比0%;gydF4y2BaPgydF4y2Ba= 0.04)。一个可能相关的4级事件的淋巴球减少症(2周时间)在一个大剂量的话题。增加血清转氨酶浓度被报道在六个科目(四个低剂量和两个高剂量)。gydF4y2Ba
一个高剂量主题开发8到10年级皮肤脓疱测量< 1厘米直径每个四肢,额头和鼻子。治疗后病变发展大约4 d和解决大约6周内完全没有疤痕形成。这个话题收到两个后续剂jx - 594没有延迟。gydF4y2Ba
疾病控制和mRECIST肝内和崔响应gydF4y2Ba
我们进行连续动态磁共振成像(MRI)扫描肝脏和腹部,而这些随后被阅读专家独立的中央读者对治疗手臂也不清楚。我们应用mRECIST响应标准开发的肝癌患者gydF4y2Ba16gydF4y2Ba评估jx - 594治疗肝脏的影响。此外,jx - 594可以破坏肿瘤血流量和诱导肿瘤坏死gydF4y2Ba17gydF4y2Ba肿瘤,我们进行对比度增强测量根据修改后的彩标准gydF4y2Ba18gydF4y2Ba评估影响灌注和肿瘤坏死的发展。gydF4y2Ba
在一项研究表明gydF4y2Ba14gydF4y2Ba,两个剂量与肝内抗肿瘤活性有关。8周后肝内mRECIST疾病控制利率总体为46%(28可评价的对象,控制利率47%和46%的高剂量和低剂量组,分别),在任何时间点为50%(8周后意义或任何其他时间,哪个是更好的)。作为主要影像学端点在第八周,我们没有持续进行后续的扫描结果没有评估肿瘤进展时间。gydF4y2Ba
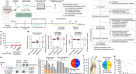
我们发现客观mRECIST反应和减少肿瘤灌注和对比度增强注射和noninjected肿瘤内两个剂量组(gydF4y2Ba图1模拟gydF4y2Ba和gydF4y2Ba补充图2gydF4y2Ba)。在某些情况下,肿瘤与降低对比度增强显示肿胀和水肿(gydF4y2Ba图1 egydF4y2Ba)。修改后的崔整体回应率为62%(26可评价的主题,与57%和67%的反应率高剂量和低剂量组,分别)。崔均值的变化参数和−−35.6%和28.8%的高剂量和低剂量组,分别为(gydF4y2BaPgydF4y2Ba= 0.73)。四个目标mRECIST反应(一个完整的和三个部分;gydF4y2Ba图1 fgydF4y2Ba)和报告了10例稳定的疾病;剂量不与肝内响应(gydF4y2Ba图1模拟gydF4y2Ba)。最长的意思是改变肿瘤直径(mRECIST)可能反映剂量水肿的形成(变化23.8%,−8.7%的高剂量和低剂量组,分别;gydF4y2BaPgydF4y2Ba= 0.11)。我们发现类似的身体影响肿瘤血管肿瘤高剂量治疗后(gydF4y2Ba图1克gydF4y2Ba),包括小质量(< 1厘米),基线可视化水平较差。gydF4y2Ba
(gydF4y2Ba一个gydF4y2Ba)最大减少最长直径之和(LD)的目标从基线(mRECIST标准)在肝脏肿瘤患者个体jx - 594治疗。gydF4y2BangydF4y2Ba= 22患者在基线和至少一个可测量的和可评价的肿瘤随访时间点。肿瘤增加> 100%表示+以上的酒吧。(gydF4y2BabgydF4y2Ba)最大的肿瘤对比度增强或减少最长直径从基线(Choi标准)在目标在肝脏肿瘤患者个体jx - 594治疗。gydF4y2BangydF4y2Ba= 24患者在基线和至少一个可测量的和可评价的肿瘤随访时间点。肿瘤增加> 100%表示+以上的酒吧。(gydF4y2BacgydF4y2Ba)之和最长最大的减少肿瘤直径在noninjected基线(RECIST标准)后肝肿瘤患者个体jx - 594治疗。gydF4y2BangydF4y2Ba= 8可评价的。(gydF4y2BadgydF4y2Ba)最大的肿瘤对比度增强或减少noninjected最长的直径从基线(Choi标准)后肝肿瘤患者个体jx - 594治疗。gydF4y2BangydF4y2Ba= 8可评价的。(gydF4y2BaegydF4y2Ba)的影响的例子jx - 594在对比度增强和灌注在一个注射肿瘤(jx7 - 1401;高剂量)。(gydF4y2BafgydF4y2Ba)的影响的例子jx - 594的最长直径注射肿瘤(完成mRECIST反应)(jx7 - 1715;低剂量)。(gydF4y2BaggydF4y2Ba)的影响的例子jx - 594在对比度增强和灌注noninjected(遥远)肿瘤(jx7 - 1403;高剂量)。红圈(gydF4y2BaegydF4y2Ba- - - - - -gydF4y2BaggydF4y2Ba)显示相同的肿瘤(回应)。gydF4y2Ba
药物动力学、复制和转基因表达gydF4y2Ba
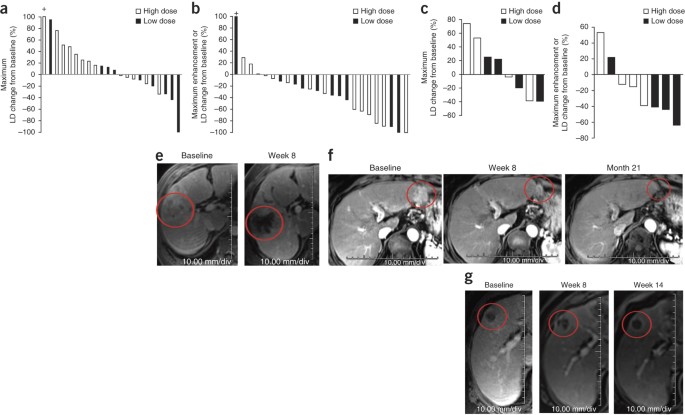
jx - 594注入肿瘤导致急性扩散jx - 594基因组进入血液,从而导致系统分布。我们监测血液中jx - 594的浓度随着时间在15分钟,3 h, 5 - 7 d和14 d后完成每个喷射过程。药代动力学资料是每个主题类似的所有三个注射(gydF4y2Ba图2一个gydF4y2Ba)。最高浓度在注射后15分钟;基因组在血液检测在这个时间点在双臂上的所有对象。jx - 594的峰值浓度显著更大剂量的受试者手臂(gydF4y2Ba图2一个gydF4y2Ba);平均浓度(±s.e.m)。所有周期是273700±55650毫升基因组gydF4y2Ba−1gydF4y2Ba高剂量组和基因组31650±5317毫升gydF4y2Ba−1gydF4y2Ba低剂量组(gydF4y2BaPgydF4y2Ba= 0.0002,gydF4y2BatgydF4y2Ba测试)。急性血药浓度在15分钟后注入符合输入剂量相当大一部分敏锐地进入血液中或后立即注射过程(半衰期gydF4y2Ba∼gydF4y2Ba60分钟)。这些受试者的峰值浓度类似于受试者输液后注入浓度峰值在第一阶段试验类似的剂量gydF4y2Ba15gydF4y2Ba;峰值浓度高剂量组在这个实验中高于阈值对静脉输液交付肿瘤(第一阶段临床静脉输液中定义的),而低剂量组的浓度。jx - 594的频率和浓度检测血液中基因组也明显更大剂量的受试者在注射后3小时以内(78%的受试者可检测jx - 594相比,45%的高剂量和低剂量组,分别为所有治疗周期;意味着基因组10450±2090毫升的浓度gydF4y2Ba−1gydF4y2Ba基因组和2098±488毫升gydF4y2Ba−1gydF4y2Ba高剂量和低剂量组,分别为所有治疗周期;gydF4y2BaPgydF4y2Ba= 0.0006,gydF4y2BatgydF4y2Ba测试)。gydF4y2Ba
(gydF4y2Ba一个gydF4y2Ba)均值(±s.e.m) jx - 594的浓度峰值(基因组以定量PCR (qPCR))在每次治疗后血液循环(使用血液获得15分钟完成后治疗)的剂量组(gydF4y2BatgydF4y2Ba测试)。瘤内。(gydF4y2BabgydF4y2Ba)患者的百分比的证据β-gal转基因表达(+ 95%可信区间(CI)) jx - 594治疗后(代抗体(Ab)β-gal转基因产品在29 d治疗表明jx - 594复制,像β-gal蛋白表达与病毒复制)(确切概率法)。(gydF4y2BacgydF4y2Ba)患者的百分比的证据hGM-CSF转基因表达(+ 95% CI) jx - 594治疗后5天(确切概率法)。(gydF4y2BadgydF4y2Ba)最大诱导中性粒细胞浓度在治疗后血液循环1中剂量组(使用血液获得治疗后在5和15天)。黑条,低剂量jx - 594;白色的酒吧,大剂量jx - 594。gydF4y2Ba
我们评估jx - 594使用三种方法复制和双重转基因表达。我们首先评估抗体开发β-galactosidase(β-gal)蛋白质(gydF4y2BalacZgydF4y2Ba转基因产品),这取决于病毒复制和相关蛋白表达。第二,jx - 594表达hGM-CSF转基因早期的后期合成启动子的控制下,高层表达会发生在复制产品的癌细胞gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba,gydF4y2Ba8gydF4y2Ba。而增长值jx - 594能强烈刺激多种细胞因子的生产,推迟hGM-CSF表达5或更多天输液后(当其他细胞因子浓度回到基线水平)是表明hGM-CSF表达式从jx - 594在复制的背景下gydF4y2Ba14gydF4y2Ba,gydF4y2Ba15gydF4y2Ba。第三,我们评估了延迟重新jx - 594血液中基因组5天,15日,22日,29日,第三十六条、第四十三条、57。jx - 594的基因组检测的血液在任何的时间点后jx - 594建议瘤内注射复制和随后的泄漏进入体循环。我们能够检测jx - 594血液中基因组的三个主题(两个高剂量和低剂量)在后期时间点(天15-36)。gydF4y2Ba
可以预期,因为复制jx - 594剂量,β-gal-specific抗体开发的大部分的受试者在治疗阶段:高剂量的75%和62%的低剂量的受试者发达这些抗体(gydF4y2Ba图2 bgydF4y2Ba)。痘苗病毒中和抗体滴度(jx - 594),因此,在基线检测(从儿童期疫苗接种)在50%的受试者;所有科目开发可检测浓度白天29。gydF4y2Ba
hGM-CSF蛋白质可量化的等离子体在第五天高剂量的69%和46%的低剂量的受试者(gydF4y2BaPgydF4y2Ba= 0.27,确切概率法;所有基线样本- hGM-CSF) (gydF4y2Ba图2 cgydF4y2Ba)。探索性的数据的一个子集受试者接受同样的制造大量的临床试验资料表明,hGM-CSF浓度(第五天)在高剂量的受试者高于低剂量的受试者(高剂量的受试者中位数为47.6 pg毫升gydF4y2Ba−1gydF4y2Ba而1.5 pg mlgydF4y2Ba−1gydF4y2Ba低剂量的受试者;gydF4y2BaPgydF4y2Ba< 0.001,gydF4y2BatgydF4y2Ba测试)。中性粒细胞和嗜酸性粒细胞是白细胞的GM-CSF-responsive子集。绝对中性粒细胞和嗜酸性粒细胞浓度为5 - 14 d之间的大幅增加治疗后65%的受试者血液中可量化的hGM-CSF (gydF4y2Ba图2 dgydF4y2Ba)。gydF4y2Ba
诱导体液和细胞抗癌免疫力gydF4y2Ba
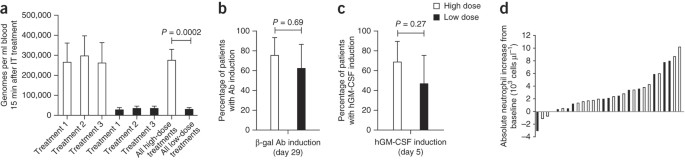
我们分析了血液,肿瘤组织和影像学成像评估感应抗癌免疫(gydF4y2Ba图3gydF4y2Ba)。作为衡量antitumoral免疫诱导,我们评估抗体介入补体依赖细胞毒性(CDC)受试者的血清治疗后随着时间的推移。十一16例(69%)受试者评估发达国家疾病预防控制中心对至少一个四肝癌细胞系(六大剂量和五低剂量的受试者)(gydF4y2Ba图3 a, bgydF4y2Ba);CDC血清稀释到5%后尤为明显。所有肝癌细胞系含有乙型肝炎病毒DNA测试除了HepG2(这不是病毒相关);六个科目与CDC感应肝炎B-associated HCC,两人肝炎C-associated HCC和三个病毒性肝细胞癌。gydF4y2Ba
(gydF4y2Ba一个gydF4y2Ba)抗体介入补体依赖细胞毒性诱导后jx - 594治疗肝细胞癌(gydF4y2BangydF4y2Ba= 4)正常(gydF4y2BangydF4y2Ba= 2;HUVEC和MRC-5)和non-HCC (RCC,gydF4y2BangydF4y2Ba= 3;黑色素瘤,gydF4y2BangydF4y2Ba= 4)细胞系。每个图显示了比例意味着细胞生存能力南达科他州(+)与每个孵化后病人的血清(稀释至5%)收集43天的起始治疗后与基线相比。jx7 - 1704和jx7 - 1702,两大剂量的病人。(gydF4y2BabgydF4y2Ba)抗体介入中心感应在个别病人对肝癌细胞株后随着时间的推移jx - 594治疗(血清稀释至5%;意思是南达科他州±)。数据显示从病人的血清诱导≤50%细胞生存能力细胞死亡(> 50%)在至少一个随访时间点。(gydF4y2BacgydF4y2Ba)的影像学证据渐进性坏死和边缘增强noninjected肿瘤(jx7 - 0307;低剂量)。(gydF4y2BadgydF4y2Ba))染色的活检样本收集的肿瘤病人jx7 - 0301(低剂量)1.5年后jx - 594的起始治疗。规模的酒吧,100μm(低放大);50μm(高倍率插图)。(gydF4y2BaegydF4y2Ba)的影像学证据渐进性坏死和边缘增强noninjected肿瘤(jx7 - 0301;低剂量)。红圈(gydF4y2BacgydF4y2Ba,gydF4y2BaegydF4y2Ba)显示相同的肿瘤(回应)。(gydF4y2BafgydF4y2Ba有关酶联免疫斑点分析检测T细胞)生产interferon-γ回应刺激β-gal肽在基线和jx - 594治疗后;数据表示为spot-forming细胞的平均数(证监会)10gydF4y2Ba5gydF4y2Ba南达科他州细胞(+)(jx7 - 0310,低剂量;jx7 - 0311,高剂量)。(−),负控制肽。的gydF4y2BaPgydF4y2Ba值gydF4y2Ba一个gydF4y2Ba和gydF4y2BafgydF4y2Ba被计算gydF4y2BatgydF4y2Ba测试。gydF4y2Ba
肿瘤影像学证据包括进步几乎完全hypovascularity和坏死明显增强边缘noninjected肿瘤发展中在四个主题(3 - 4个月gydF4y2Ba图3gydF4y2Ba);这些发现被认为是极不寻常的肝癌肿瘤恶化,但我们不能完全排除过程。我们检查这些群众1.5年后最后jx - 594治疗(gydF4y2Ba图3 egydF4y2Ba);活检显示弥漫性淋巴细胞浸润(gydF4y2Ba图3 dgydF4y2Ba)。gydF4y2Ba
我们也评估细胞免疫。细胞毒性T细胞诱导牛痘肽(数据未显示)和jx - 594转基因产品β-gal(酶联免疫吸附点有关酶联免疫斑点)(分析)(gydF4y2Ba图3 fgydF4y2Ba);β-gal细胞毒性T细胞活动出现在高剂量主题1.5年治疗后初始化(gydF4y2Ba补充图3gydF4y2Ba)。相比之下,T细胞来自健康的捐赠者不暴露于jx - 594没有反应到β-gal (gydF4y2Ba补充图3gydF4y2Ba)。gydF4y2Ba
总生存期gydF4y2Ba
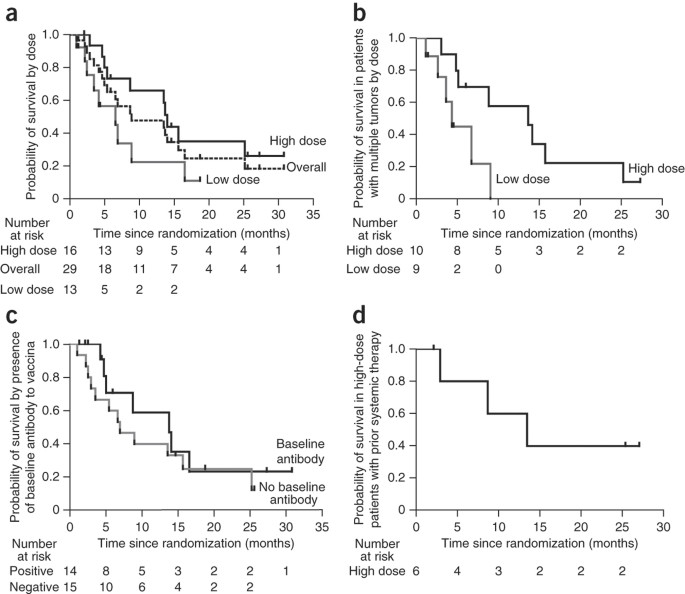
中位总生存期是9.0个月整个人口研究。我们评估了不同的基线变量之间的相关性和总生存期(gydF4y2Ba表2gydF4y2Ba)。只有剂量队列和jx - 594年达到峰值血药浓度与总体存活率显著相关。总体存活率大大延长了高剂量的手臂相比,低剂量的手臂(风险比0.39,gydF4y2BaPgydF4y2Ba= 0.020,Gehan-Breslow-Wilcoxon测试,单侧检验的优势高剂量)。中位总生存期是14.1个月的大剂量组相比,低剂量组6.7个月(gydF4y2Ba图4gydF4y2Ba)。kaplan meier生存估计高剂量和低剂量组在1年分别为66%和23%,分别在18个月分别为35%和11%,分别。生存没有与肿瘤病因(病毒或病毒)。在主题与多个肿瘤在基线(十大剂量和9低剂量的受试者),高剂量jx - 594与一个重要的生存受益;中位总生存期是13.6个月高剂量组与低剂量组的4.3个月(危险比为0.19,gydF4y2BaPgydF4y2Ba= 0.018,Gehan-Breslow-Wilcoxon测试,单侧检验的优势高剂量)(gydF4y2Ba图4 bgydF4y2Ba)。主题与多个肿瘤(gydF4y2BangydF4y2Ba= 19)有一个生存中值与单一肿瘤(科目的一半gydF4y2BangydF4y2Ba= 10)在这个实验中(分别为8.8个月和16.6个月)。检测到中和抗体的存在与否对牛痘基线不与生存时间(风险比0.68,偏向于基线相比,抗体阳性antibody-negative科目;gydF4y2BaPgydF4y2Ba= 0.24,Gehan-Breslow-Wilcoxon测试)(gydF4y2Ba图4摄氏度gydF4y2Ba)。我们进行了探索性的多元逐步回归分析,以评估剂量和基因组峰值浓度,中性粒细胞诱导和抗体诱导jx - 594β-gal转基因;因为只有24受试者可评价的所有变量,这只是一个存活率存在分析。这个多变量分析证实剂量组是最好的预测总生存期(gydF4y2BaχgydF4y2Ba2gydF4y2Ba= 2.0085,风险比为0.358);其他变量没有添加额外的剂量后整体生存预测价值。gydF4y2Ba
六大剂量的受试者之前失败的系统性治疗研究招生的时候,如上所述;这组四个没有之前用索拉非尼治疗。中位数生存的人口估计为主题gydF4y2Ba∼gydF4y2Ba2 - 4个月的基础上随机三期试验的数据与索拉非尼gydF4y2Ba19gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba。高剂量的受试者在这个系统性治疗失败子群的平均生存13.6个月,和两个这样的科目还活着后2年以上(gydF4y2Ba图4 dgydF4y2Ba)。gydF4y2Ba
讨论gydF4y2Ba
我们报告在这里第一次,据我们所知,几个重要发现jx - 594和溶瘤细胞的免疫疗法的领域。首先,我们证明了jx - 594剂量是一个重要的决定因素的总体生存时间在学科高级癌;鉴于溶瘤病毒在肿瘤细胞复制,它已经预言最大化剂量的主题将是更重要比与其他癌症的疗法。第二,据我们所知,这是第一个随机临床试验显示,溶瘤病毒或基因疗法代理与显著提高总生存时间。值得注意的是,这个试验的低剂量有明显的抗癌功效,因此,表现出显著的生存影响高剂量组与低剂量的活性控制可能是更高的障碍相比安慰剂。第三,我们展示了积极的感应功能抗肿瘤免疫的溶瘤细胞的病毒在多个学科内的同质人口。jx - 594治疗诱导多克隆体液免疫反应导致锁定疾控中心。黑色素瘤临床试验中单纯疱疹病毒(HSV) hGM-CSF (T-Vec;安进公司),T细胞来源于肿瘤样本的表型分析建议从外周血T细胞明显的差异。T细胞来源于参与控制的患者相比,有一个与黑素瘤相关抗原被增加T细胞(MART-1)特殊T细胞肿瘤疫苗接种后进行回归; functional antitumoral immunity, however, was not assessed1gydF4y2Ba。gydF4y2Ba
这些试验结果解决关键问题,但其他人仍悬而未决。尽管不同得到了农业部的数据,包括jx - 594复制和免疫刺激,每个恐鸟的相对重要性还有待确定。唯一的变量与总体生存时间,除了剂量组,是急性峰值jx - 594血液中的浓度;值得注意的是,高剂量组的血药浓度高于静脉输液交付所需的阈值浓度在阶段1 (ref。gydF4y2Ba15gydF4y2Ba),而低剂量浓度。因此,这些数据表明,系统性肿瘤控制和改善生存可能通过jx - 594通过大剂量静脉输液管理。预测这一假设的基础上,高剂量的生存受益jx - 594是最广泛的肿瘤患者最为明显的负担。复制和hGM-CSF转基因表达与三个农业部:有关急性血管破坏肿瘤,肿瘤瘤细胞溶解、坏死和抗肿瘤免疫力。高剂量的长期生存患者(gydF4y2Ba∼gydF4y2Ba在2年35%)剂量/只有4周后显示一个潜在的持久的系统性受益。虽然不是证明,这种持久的功效可以反映慢性病毒瘤细胞溶解或免疫介导的效果,证明tumor-lysing抗体生成和淋巴细胞浸润成肿瘤。还需要进一步的研究来评估每个恐鸟的相对重要性在特定的患者群体。同样,虽然辅助T细胞参与了免疫球蛋白类切换和诱导T细胞特定β-gal转基因,进一步诱导肿瘤特异性T淋巴细胞上的数据需要在今后的试验中获得的。此外,较大的试验将允许探索免疫和病毒复制端点之间的相关性和患者生存。崔响应标准包括肿瘤密度和最大直径的变化。mRECIST和崔标准在肝癌中的应用试验越来越多,和初步的数据显示,这些标准可能预测HCC的整体存活率比标准RECIST标准gydF4y2Ba21gydF4y2Ba,gydF4y2Ba22gydF4y2Ba。然而,需要更多的数据来知道如何解释这些mRECIST和崔的反应。gydF4y2Ba
这个分层的生存分析和随机临床试验表现出明显的剂量依赖性延长生存。然而,这些发现应该扩展在较大的随机试验与安慰剂控制臂包括在内。我们选择的样本大小30例给予足够的权力在双臂毒性分析。尽管样本量相对较小,一个活跃的控制组治疗,一个显著的生存受益了,因为大的效果。预后因素平衡在两臂之间,除了穷人更大剂量的患者先前未能系统性治疗的预后因子,包括索拉非尼治疗;这群大剂量治疗的生存时间是类似于系统性首次治疗的病人。因此,高剂量的生存受益jx - 594无法解释已知的预后因素的失衡。gydF4y2Ba
大型随机试验充分有力的整体存活率的影响正在或已经计划jx - 594年的晚期肝癌患者。在随机试验中涉及病人未能与索拉非尼治疗,病人被随机要么jx - 594 +最好的支持(缓和)保健或单独最好的支持性护理(ClinicalTrials.gov,gydF4y2BaNCT01387555gydF4y2Ba)。在其他实体瘤人口正在试验,包括结肠癌癌突变gydF4y2Bak -gydF4y2Ba基因型。此外,针对溶瘤细胞的牛痘病毒如jx - 594能被设计用来表达多元和多样的和潜在的协同农业部生物制剂;这些包括细胞因子、肿瘤抗原,检查点抑制剂,prodrug-activating酶,单链抗体和肿瘤抗原(引用文献综述。gydF4y2Ba6gydF4y2Ba)。特别是,探索肿瘤抗原表达的给我们示范在这个实验中,T细胞反应是诱发jx - 594转基因β-gal。鉴于大型transgene-encoding牛痘病毒的能力,多个肿瘤抗原,以及补充细胞因子(例如,gm - csf或白介素2(2)),可以从相同的表达病毒骨干。总之,溶瘤细胞的免疫治疗牛痘病毒jx - 594 (Pexa-Vec)拥有先进承诺治疗实体肿瘤,并进一步临床试验是必要的。gydF4y2Ba
方法gydF4y2Ba
研究设计。gydF4y2Ba
这个试验是一个多中心、跨国随机和分层,与这些相应平行的组织研究研究晚期肝癌患者。患者分层(病毒或病毒)和随机一对一的高剂量或低剂量组。主要终点是由独立评估专家放射科医生对治疗组也不清楚;主要调查人员没有蒙蔽剂量组。所有患者给予书面知情同意根据良好的临床实践的原则。研究协议,并同意表格由美国食品和药物管理局批准,韩国食品和药物管理局和健康加拿大,以及机构审查和感染控制委员会在以下中心:加州大学圣地亚哥(UCSD)摩尔癌症中心,麦克马斯特大学医学中心,三星医疗中心,俄亥俄州立大学,遣散医院延世大学健康系统和釜山国立大学医院。一个独立的数据安全监测委员会回顾了主要安全评估和定期评估安全性和有效性。生存分析的数据截止日期是生存随访收集的数据当最后一个病人到达第八周主要终点评估访问。gydF4y2Ba
这项研究是由Jennerex设计公司与主要调查人员合作。数据采集和监视被Jennerex inc .和绿十字公司执行。数据管理、安全报告管理、统计和影像学图像管理、由独立专家承包商进行评估和分析。手稿写和编辑Jennerex inc .)和主要调查人员一起合作绿十字公司共同决定发布后。学术调查人员保证结果的有效性。gydF4y2Ba
病人。gydF4y2Ba
入选标准包括不可切除的和注射(肿瘤边缘定义)肝癌(组织学证实或临床和实验室诊断定义根据美国肝病研究协会的指导方针),充足的血液功能(绝对中性粒细胞计数> 1250 mm细胞gydF4y2Ba−3gydF4y2Ba白细胞计数> 2500 mm细胞gydF4y2Ba−3gydF4y2Ba和< 50000 mm细胞gydF4y2Ba−3gydF4y2Ba血红蛋白≥9 g dlgydF4y2Ba−1gydF4y2Ba细胞,血小板数≥50000毫米gydF4y2Ba−3gydF4y2Ba与国际标准化比率(INR)≤1.5倍正常上限)和器官功能(包括血清肌酐< 2毫克dlgydF4y2Ba−1gydF4y2Ba天冬氨酸转氨酶(AST)、丙氨酸转氨酶(ALT) <正常上限的5.0倍,总胆红素≤2.5倍正常上限和儿童的A或B)和KPS评分70或更高。排除标准包括肝肿瘤的位置可能导致临床副作用的肿瘤治疗后肿胀(例如,肿瘤侵犯胆道),中枢神经系统恶性肿瘤,严重或不稳定的心脏疾病,症状性腹水,疫苗接种并发症的风险增加(表皮剥脱的皮肤病如湿疹、异位性皮炎),免疫缺陷造成的潜在疾病,抗癌治疗前4周内第一个治疗,使用某些抗病毒药物的活动对牛痘(例如,利巴韦林、阿德福韦,cidofovir PEG-IFN)和怀孕或护理。患者家庭接触者在已知风险牛痘疫苗并发症(例如,严重的免疫缺陷或湿疹)不能安置被排除在外。门静脉血栓形成或入侵和肝外疾病被允许。三个病人在这个实验中是包含在出版后使用索拉非尼jx - 594治疗gydF4y2Ba10gydF4y2Ba。gydF4y2Ba
临床试验材料(CTM)。gydF4y2Ba
中医是根据良好生产规范生产的指导方针。中医是感染后生成人类癌的细胞。细胞后大约48 h和细胞溶解,细胞碎片是通过一个标准的过滤步骤。剩下的上层清液由切向流过滤净化。最终产品的质量控制测试包括化验不育和内毒素(缺席),外源病毒(缺席),DNA和蛋白质含量,力量用PFU毫升gydF4y2Ba−1gydF4y2Ba和hGM-CSF生产。立即在瘤内注射(IT), jx - 594在bicarbonate-buffered盐水稀释。gydF4y2Ba
随机化,掩蔽和治疗。gydF4y2Ba
登记和分层后肝癌病因(B或C型肝炎病毒infection-associated病毒相关),我们随机患者集中使用交换块接受剂量的10gydF4y2Ba9gydF4y2Ba或10gydF4y2Ba8gydF4y2Ba空斑形成单位分布在5天1肝内肿瘤,15 - 29。我们管理jx - 594通过成像制导注射用多管齐下Quadrafuse针(雷克斯医疗公司),以确保病毒的均匀分布在整个肿瘤如果可能的话(如果这不是技术上可行,使用直针)。每人总剂量治疗会议是固定在10gydF4y2Ba9gydF4y2Ba或10gydF4y2Ba8gydF4y2Ba空斑形成单位。jx - 594溶液的体积注射肿瘤的体积成正比是注射(肿瘤体积的25%)。gydF4y2Ba
物理和实验室评估。gydF4y2Ba
我们进行了物理评估和间隔病史在每个访问的前8周的研究。安全监测包括不良事件监测根据美国国家癌症研究所常见毒性标准(3.0版)和标准实验室为血液学毒性分级,肝、肾功能,凝固的研究中,血清化学和验尿。我们进行白细胞计数的常规实验室检测中定义的协议。我们评估了白细胞计数在基线和5天,15日,22日,29日,第三十六条、第四十三条、57。gydF4y2Ba
qPCR。gydF4y2Ba
我们评估jx - 594的基因组在血液的浓度随着时间的推移使用qPCR如前所述gydF4y2Ba14gydF4y2Ba,gydF4y2Ba23gydF4y2Ba。我们收集样品每次注入和前15分钟,3 h和5或7 d后治疗和43天和57(最后2和4周后治疗)。gydF4y2Ba
hGM-CSF ELISA。gydF4y2Ba
我们评估hGM-CSF蛋白质浓度在第一次治疗后血浆在基线和5 d通过固相夹心ELISA使用Quantikine hGM-CSF工具包(研发系统)由制造商。gydF4y2Ba
β-gal-specific抗体ELISA。gydF4y2Ba
我们评估抗体诱导在基线和β-gal 29天。人类免疫球蛋白抗体β-gal ELISA测定。短暂,我们孵化板块(NUNC MaxiSorp,热费希尔科学)与包含β-gal井碳酸(σ)或碳酸氢盐缓冲一夜之间在4°C和洗盘子与孵化前PBS-Tween阻断缓冲区(PBS 1% BSA, ELISA年级(σ))。我们添加了稀释血清(1:50,1:10 0或1:200 PBS渐变为0.05%和1% BSA)β-gal-coated和控制井在复制和孵化在23°C。我们洗盘子,孵化alkaline-phosphatase-labeled山羊人类免疫球蛋白(Abcam)稀释下。洗后,我们添加了比色黄色衬底碱性磷酸酶(pNPPσ)和添加氢氧化钠10分钟后停止显色。我们看405海里的吸光度,减去630海里的吸光度。我们减去控制井值占非特异性和效价计算值相比之下绑定到一个标准阳性血清,曲线任意分配效价8000。gydF4y2Ba
中和抗体的检测。gydF4y2Ba
我们测量jx - 594 -特定的中和抗体滴度在基线和5天,15日,29日,57细胞病变效应抑制试验(如前所述)gydF4y2Ba14gydF4y2Ba,gydF4y2Ba15gydF4y2Ba。浓度的倒数表示为最高的heat-inactivated血清稀释(集中),导致细胞生存能力≥50%;稀释测试最低是10%,因此试验的检测极限是10。我们测量β-gal-specific抗体滴度在基线和ELISA如前所述的29天gydF4y2Ba15gydF4y2Ba。gydF4y2Ba
组织病理学分析。gydF4y2Ba
我们获得临床上肝肿瘤活检的患者治疗后的一个子集。福尔马林固定和石蜡包埋组织。我们染色的部分)来评估组织组织学坏死和炎症。gydF4y2Ba
放射学采集和分析。gydF4y2Ba
我们进行多相腹部两侧的动态对比度增强MRI 1.5或3.0 t先生系统使用细胞外钆螯合物造影剂。我们执行扫描基线(天−14 0)和8周;每6周之后扫描是可选的。扫描是由两个独立的放射科医生评估与肝癌专业评估(r和R.L.);读者对治疗组也不清楚。鉴于肿瘤破坏的机制的基础上血管破坏前所述jx - 594 (ref。gydF4y2Ba14gydF4y2Ba),我们选来评估肿瘤血管(对比度增强)基线,在每个时间点使用mRECIST HCC标准gydF4y2Ba16gydF4y2Ba(由R.L.)和修改崔反应评估gydF4y2Ba24gydF4y2Ba(由r)。崔响应标准包括肿瘤减少基线最长的直径或> > 10%的肿瘤密度下降15%;公布的标准相比,这些标准修改崔崔标准因为标准使用电脑断层扫描,而不是核磁共振扫描。28例可评价的整体mRECIST回应:2例死在第八周疗效评估和被归类为进行性疾病,4例可评价的mRECIST但没有可测量的肿瘤,和22患者可测量的和可评价的疾病。崔26例可评价的整体反应:2例死在第八周疗效评估和被分类为nonresponders,和24例可测量的肿瘤。两个病人可评价的时间最长mRECIST直径变化不对比度增强可评价的变化。gydF4y2Ba
补体依赖细胞毒性试验。gydF4y2Ba
SNU349, SNU482 SNU267(人类肾细胞癌;从韩国细胞系获得银行(KCLB))和SNU475, SNU398, SNU449 SNU739(人类肝细胞癌,乙型肝炎相关;从KCLB)细胞培养获得RPMI 1640 (Gibco)补充10%的边后卫(Hyclone)青霉素和链霉素。HepG2细胞(人类肝细胞癌,而不是病毒有关;在DMEM培养基培养获得写明ATCC)含有10%的边后卫青霉素和链霉素。MRC-5是非细胞(肺成纤维细胞;从KCLB)获得的最低基本培养基培养(MEM)包含10%的边后卫青霉素和链霉素。HUVEC(内皮细胞;Lonza)在内皮细胞培养介质EBM-2 (Lonza,医学博士,美国)补充2%的边后卫青霉素和链霉素。SK-MEL-2 SK-MEL-5和wm - 266 - 4细胞(人类黑色素瘤细胞; obtained from KCLB) were cultured in RPMI 1640 (Gibco) supplemented with 10% FBS (Hyclone) with penicillin and streptomycin. Lox IMVI cells (human melanoma cells; ATCC) were cultured in MEM containing 10% FBS with penicillin and streptomycin.
我们评估中心活动通过测量细胞生存能力与5%血清在孵化后96 -孔板。我们归一化细胞生存能力在血清jx - 594管理病人血清的细胞生存能力基线(jx - 594治疗前)。我们播种每个细胞株在一夜之间96 -孔板和细胞孵化。我们随后孵化细胞在DMEM(没有的边后卫)和血清样本在37°C 4 h。然后我们将细胞暴露在PBS和10μl细胞计数kit-8 (CCK-8)解决方案(Dojindo CCK-8工具包,Inc .)和孵化细胞在37°C 2 h。细胞生存能力是由光密度测量在450海里。gydF4y2Ba
β-gal-specific T细胞分析。gydF4y2Ba
我们画外周血单核细胞(PBMCs)从两个患者治疗前后jx - 594,用自体树突状细胞刺激脉冲重叠肽库(由15个氨基酸20-mer氨基酸重叠)横跨整个β-gal的蛋白质序列。最后我们还画PBMCs 1.5年后jx - 594剂量的额外的病人。我们也孤立PBMCs从四个健康的捐赠者的控制。我们保持T细胞在T细胞培养基(中医)(RPMI 1640 (Hyclone)补充45%点击的介质(欧文科学),2更易与lgydF4y2Ba−1gydF4y2BaGlutaMAX TM-I人类AB血清(表达载体)和5%(谷生物医学,温彻斯特,VA))与1000 U ml补充gydF4y2Ba−1gydF4y2Bail - 4(研发系统、明尼阿波利斯、MN)和10 ng毫升gydF4y2Ba−1gydF4y2BaIL-7 (PeproTech)。在9天我们收获细胞和测试β-gal特异性有关酶联免疫斑点试验使用。gydF4y2Ba
有关酶联免疫斑点分析我们使用的半定量的测量抗原特异效应T细胞如前所述gydF4y2Ba25gydF4y2Ba。简单地说,我们播种2.5×10gydF4y2Ba4gydF4y2Ba到10gydF4y2Ba5gydF4y2BaT细胞在一式三份个人pepmixes跨越β-gal 0.1μg每肽。我们使用的pepmix睾丸癌抗原,NY-ESO1, 0.1μg /肽/好,PHA (phytohemagluttinin) 2μl(1毫克毫升gydF4y2Ba−1gydF4y2Ba分别),正面和负面的控制。18 h的孵化后,我们开发了盘子和送他们到Zellnet咨询、新泽西量化。证监会计数和输入手机号码被绘制,排除高原后线性回归计算数据点。我们表示特定于每个抗原的T细胞的频率为每个输入单元的具体证监会数字。gydF4y2Ba
统计分析。gydF4y2Ba
审判是为了招收30例可评价的安全性和影像学的端点。疾病控制的主要目标是肝内率(mRECIST完全或部分响应或稳定的疾病)在第八周。二级目标包括安全性和抗肿瘤活性(对比度增强的变化,mRECIST HCC);药物动力学、免疫参数和总体存活率其他端点。所有患者接受至少一剂jx - 594可评价的安全。所有患者接受至少一个剂量和没有主要记录协议偏差可评价的总体存活率;可评价的患者基线和第八周扫描可评价的影像学疗效端点。通过协议,15名可被登记在每个剂量测试假设真正的成功率最多33%(这意味着很少或根本没有活动)和备择假设,真正的成功率是66%或更大的独立在每个治疗手臂(78%力量,片面的错误的0.03)。总生存期被kaplan meier分析评估gydF4y2Ba26gydF4y2Ba,比较了使用Gehan-Breslow-Wilcoxon测试和片面的α大剂量优势的统计学意义。一个片面的gydF4y2BaPgydF4y2Ba值适合这个研究研究,因为目标是确定肿瘤的高剂量更有效的控制和整体生存证明其潜在副作用的风险更高。Gehan-Breslow-Wilcoxon测试被选中,因为剂量发生只在前4周,因此一个加权的早期测试整体更多的生存曲线是合适的和合理的。二分变量被确切概率法计算,而连续变量进行比较gydF4y2BatgydF4y2Ba测试使用GraphPad Prism 5.0软件(GraphPad软件)。gydF4y2Ba
资金来源的角色。gydF4y2Ba
研究赞助商参与研究设计、数据收集、数据分析、数据解释和报告的写作。相应的作者有完全访问所有的数据在这项研究中,并最终负责决定提交出版。gydF4y2Ba
引用gydF4y2Ba
考夫曼上半叶et al .局部和远处intralesional引起的免疫接种的溶瘤细胞的疱疹病毒编码gm - csf第四阶段IIIc和黑色素瘤患者。gydF4y2Ba安。Surg.杂志。gydF4y2Ba17gydF4y2Ba,718 - 730 (2010)。gydF4y2Ba
收获节,D。,Martuza, R.L. & Zwiebel, J. Replication-selective virotherapy for cancer: biological principles, risk management and future directions.Nat,地中海。gydF4y2Ba7gydF4y2Ba,781 - 787 (2001)。gydF4y2Ba
刘,教学楼。,Galanis, E. & Kirn, D. Clinical trial results with oncolytic virotherapy: a century of promise, a decade of progress.Nat。中国。Pract。肿瘤防治杂志。gydF4y2Ba4gydF4y2Ba,101 - 117 (2007)。gydF4y2Ba
Chiocca,电子艺界溶瘤病毒。gydF4y2BaNat。启癌症gydF4y2Ba2gydF4y2Ba,938 - 950 (2002)。gydF4y2Ba
接着,c & Kirn d.h Replication-selective溶瘤腺病毒的间谍活动。gydF4y2Baj .中国。投资。gydF4y2Ba105年gydF4y2Ba,847 - 851 (2000)。gydF4y2Ba
收获节、D.H. &索恩,萨达姆政权针对性和武装溶瘤细胞的痘病毒:小说multi-mechanistic治疗类癌症。gydF4y2BaNat。启癌症gydF4y2Ba9gydF4y2Ba,64 - 71 (2009)。gydF4y2Ba
金,J.H. et al .系统性武装溶瘤细胞的免疫治疗癌症和jx - 594,有针对性的痘病毒表达gm - csf。gydF4y2Ba摩尔。其他。gydF4y2Ba14gydF4y2Ba,361 - 370 (2006)。gydF4y2Ba
Parato·et al,溶瘤细胞的痘病毒jx - 594选择性地复制和破坏癌细胞的基因一般途径激活癌症。gydF4y2Ba摩尔。其他。gydF4y2Ba20.gydF4y2Ba,749 - 758 (2012)。gydF4y2Ba
黄,T.H. et al。一种机械的概念与jx - 594的临床试验,有针对性multi-mechanistic溶瘤细胞的痘病毒,在转移性黑色素瘤患者。gydF4y2Ba摩尔gydF4y2Ba。gydF4y2Ba其他。gydF4y2Ba19gydF4y2Ba,1913 - 1922 (2011)。gydF4y2Ba
Heo, j . et al .序贯疗法jx - 594,有针对性的溶瘤细胞的痘病毒,紧随其后的是索拉非尼在肝细胞癌:临床前和临床的组合效果。gydF4y2Ba摩尔。其他。gydF4y2Ba19gydF4y2Ba,1170 - 1179 (2011)。gydF4y2Ba
索恩,萨达姆政权et al . Rational应变选择和工程创建一个广谱、系统有效的溶瘤细胞的痘病毒,jx - 963。gydF4y2Baj .中国。投资。gydF4y2Ba117年gydF4y2Ba,3350 - 3358 (2007)。gydF4y2Ba
葡萄酒,L.M.,Wu, J.T. & Kirn, D.H. Validation and analysis of a mathematical model of a replication-competent oncolytic virus for cancer treatment: implications for virus design and delivery.癌症Res。gydF4y2Ba63年gydF4y2Ba,1317 - 1324 (2003)。gydF4y2Ba
senz N.N. et al。集落刺激factor-encoding II期临床试验,第二代溶瘤细胞的疱疹病毒患者不可切除的转移性黑素瘤。gydF4y2Baj .中国。肿瘤防治杂志。gydF4y2Ba27gydF4y2Ba,5763 - 5771 (2009)。gydF4y2Ba
公园,林丙辉et al。使用有针对性的溶瘤细胞的痘病毒,jx - 594,难治性原发性或转移性肝癌患者:第一阶段的审判。gydF4y2Ba柳叶刀杂志。gydF4y2Ba9gydF4y2Ba,533 - 542 (2008)。gydF4y2Ba
Breitbach, C.J. et al .静脉注射multi-mechanistic cancer-targeted溶瘤细胞的痘病毒在人类身上。gydF4y2Ba自然gydF4y2Ba477年gydF4y2Ba,99 - 102 (2011)。gydF4y2Ba
Lencioni, r & Llovet J.M.修改RECIST (mRECIST)评估肝细胞癌。gydF4y2BaSemin。肝脏说。gydF4y2Ba30.gydF4y2Ba52-60 (2010)。gydF4y2Ba
刘,教学楼。,Hwang, T., Park, B.H., Bell, J. & Kirn, D.H. The targeted oncolytic poxvirus JX-594 demonstrates antitumoral, antivascular, and anti-HBV activities in patients with hepatocellular carcinoma.摩尔。其他。gydF4y2Ba16gydF4y2Ba,1637 - 1642 (2008)。gydF4y2Ba
崔h . et al .相关的电脑断层扫描,正电子发射断层扫描患者的转移性胃肠道间质肿瘤治疗与甲磺酸伊马替尼在一个单一的机构:新的计算机断层扫描响应标准的建议。gydF4y2Baj .中国。肿瘤防治杂志。gydF4y2Ba25gydF4y2Ba,1753 - 1759 (2007)。gydF4y2Ba
Llovet J.M. et al。索拉非尼在先进的肝细胞癌。gydF4y2Ba心血管病。j .地中海。gydF4y2Ba359年gydF4y2Ba,378 - 390 (2008)。gydF4y2Ba
程,A.L. et al。索拉非尼的病人的临床疗效和安全性在亚太地区拥有先进的肝细胞癌:III期随机,双盲,安慰剂对照试验。gydF4y2Ba柳叶刀杂志。gydF4y2Ba10gydF4y2Ba,25 - 34 (2009)。gydF4y2Ba
副检察官,s . et al .晚期患者的肿瘤密度变化hepato-cellular癌接受舒尼替。gydF4y2Ba中国。癌症Res。gydF4y2Ba17gydF4y2Ba,4504 - 4512 (2011)。gydF4y2Ba
Edeline, j . et al。比较肿瘤反应的反应评估标准(RECIST)和修改RECIST索拉非尼对肝细胞癌患者。gydF4y2Ba癌症gydF4y2Ba118年gydF4y2Ba,147 - 156 (2012)。gydF4y2Ba
Kulesh, D.A. et al。天花和pan-orthopox病毒检测的实时3′小槽粘合剂TaqMan化验罗氏LightCycler和造父变星智能循环平台。gydF4y2Baj .中国。Microbiol。gydF4y2Ba42gydF4y2Ba,601 - 609 (2004)。gydF4y2Ba
崔h . et al . CT评价甲磺酸伊马替尼治疗后胃肠道间质瘤的反应:定量分析与FDG PET发现。gydF4y2Ba学杂志。j . Roentgenol。gydF4y2Ba183年gydF4y2Ba,1619 - 1628 (2004)。gydF4y2Ba
Gerdemann, et al .快速生成multivirus-specific细胞毒性T淋巴细胞对病毒感染的预防和治疗。gydF4y2Ba摩尔。其他。gydF4y2Ba20.gydF4y2Ba,1622 - 1632 (2012)。gydF4y2Ba
一口油井为el瑞& Meier卡普兰,p .非参数估计的不完整的观察。gydF4y2Baj。统计协会。gydF4y2Ba53gydF4y2Ba,471 - 481 (1958)。gydF4y2Ba
确认gydF4y2Ba
人类。Limacher, m . Homerin B.M. Bastien和m . Lusky(所有从转基因SA)给手稿深刻的评论。T.-H.H.和M.K.K.支持格兰特的韩国医疗技术研究和开发项目,省卫生、福利和家庭事务,大韩民国(A091047)。C.R.由一名飞行员拨款丹邓肯癌症中心。M.N.支持的罗伯特和贾尼斯•麦克奈尔基金会和贝勒研究倡导学生科学家基金。支持J.C.B.安大略癌症研究所和特里福克斯基金会。资金是由Jennerex,转基因SA (Illkirch、法国)和绿十字公司;赠款T.-H.H.从韩国医疗技术研发项目,省卫生、福利和家庭事务,韩国;从特里J.C.B.福克斯基金会和加拿大健康研究所(CIHR);和一个飞行员格兰特C.R.从丹邓肯癌症中心。 This trial was registered with ClinicalTrials.gov, numberNCT00554372gydF4y2Ba。gydF4y2Ba
作者信息gydF4y2Ba
作者和联系gydF4y2Ba
贡献gydF4y2Ba
D.H.K.和r。设计的研究。C.J.B.,D.H.K., T.-H.H., A.M., R.P., T.H., K.D., J.C.B., R.L., L.L., B.-G.R., M.C., C.R. and J.B. analyzed the data and wrote the manuscript. Y.S.L., M.K.K., M.D. and M.N. performed bioanalytical analyses. J.H., T.R., L.R., S.R., M.B., H.Y.L., H.C.C. and C.W.K. enrolled and managed the patients. C.J.B. and D.H.K. had access to all the data in the trial. D.H.K. made the final decision to submit for publication.
相应的作者gydF4y2Ba
道德声明gydF4y2Ba
相互竞争的利益gydF4y2Ba
C.J.B.,J.C.B., A.M., K.D., L.L. and D.H.K. are employees of Jennerex, Inc. R.L., M.D., R.P., J.C.B. and T.-H.H. consult for Jennerex, Inc. J.H. and M.C. have received travel grants from Jennerex, Inc. B.-G.R. is an employee of Green Cross, Inc.
补充信息gydF4y2Ba
补充文本和数字gydF4y2Ba
补充图1 - 3和补充表1 (PDF 350 kb)gydF4y2Ba
权利和权限gydF4y2Ba
关于这篇文章gydF4y2Ba
引用这篇文章gydF4y2Ba
Heo, J。,Reid, T., Ruo, L.et al。gydF4y2Ba随机临床试验的研究溶瘤细胞的免疫治疗牛痘jx - 594肝癌。gydF4y2BaNat地中海gydF4y2Ba19gydF4y2Ba,329 - 336 (2013)。https://doi.org/10.1038/nm.3089gydF4y2Ba
收到了gydF4y2Ba:gydF4y2Ba
接受gydF4y2Ba:gydF4y2Ba
发表gydF4y2Ba:gydF4y2Ba
发行日期gydF4y2Ba:gydF4y2Ba
DOIgydF4y2Ba:gydF4y2Bahttps://doi.org/10.1038/nm.3089gydF4y2Ba
本文引用的gydF4y2Ba
间充质干细胞cell-released溶瘤病毒:癌症治疗的创新策略gydF4y2Ba
细胞通讯和信号传导gydF4y2Ba(2023)gydF4y2Ba
联合治疗与溶瘤细胞的病毒和免疫抑制剂检查站在头颈部鳞状细胞癌:一种方法的优势互补gydF4y2Ba
癌细胞国际gydF4y2Ba(2023)gydF4y2Ba
治疗晚期肝癌的发展gydF4y2Ba
自然评论胃肠病学和肝脏病学gydF4y2Ba(2023)gydF4y2Ba
溶瘤病毒治疗:基本原则、最新进展和未来的发展方向gydF4y2Ba
信号转导和有针对性的治疗gydF4y2Ba(2023)gydF4y2Ba
细胞外囊泡:特洛伊木马交付方法系统性管理溶瘤细胞的病毒gydF4y2Ba
再生工程和转化医学gydF4y2Ba(2023)gydF4y2Ba