摘要
阿尔茨海默病的实验研究主要依赖于转基因小鼠过表达淀粉样前体蛋白(APP)。然而,这些小鼠受到人工表型的影响,因为除了淀粉样β肽(Aβ)外,它们还会过度产生其他APP片段。我们产生了带有瑞典和贝鲁瑟/伊比利亚突变的敲入小鼠,在基因中有或没有北极突变应用程序基因。小鼠表现出典型的Aβ病理,神经炎症和记忆障碍,并呈年龄依赖性。
这是订阅内容的预览,通过你所在的机构访问
相关的文章
引用本文的开放获取文章。
在阿尔茨海默病敲入模型中明显记忆丧失之前,通过行为标记和捕获促进新颖性记忆的损害
科学报告开放获取12月24日
SNCA基因降低揭示了α -突触核蛋白认知功能的性别差异
神经病理学通讯学报开放获取2022年12月14日
通过高截止微透析测定野生型和阿尔茨海默病小鼠中单特异性和双特异性淀粉样蛋白β抗体的脑药代动力学
中枢神经系统的液体和屏障开放获取12月12日
访问选项
订阅期刊
获得1年的完整期刊访问权限
79.00美元
每期只要6.58美元
所有价格均为净价格。
增值税稍后将在结帐时添加。
税务计算将在结账时完成。
买条
在ReadCube上获得时间限制或全文访问。
32.00美元
所有价格均为净价格。
参考文献
Jonsson, T.等人。自然488, 96-99(2012)。
哈代,J. &奥尔索普,D。趋势杂志。科学。12, 383-388(1991)。
萧,K.等。科学274, 99-102(1996)。
Sturchler-Pierrat, C.等。Proc。国家的。学会科学。美国94, 13287-13292(1997)。
Citron, M.等人。自然360, 672-674(1992)。
Lichtenthaler, S.F.等人。Proc。国家的。学会科学。美国96, 3053-3058(1999)。
Guardia-Laguarta, C.等。j . Neuropathol。经验,神经。69, 53-59(2010)。
福尔曼,M.S.等。生物。化学。272, 32247-32253(1997)。
Saido, T.C.等。神经元14, 457-466(1995)。
Mitani, Y.等人。j . >。32, 2037-2050(2012)。
Higuchi, M.等人。美国实验生物学学会联合会J。26, 1204-1217(2012)。
罗伯逊,E.D.等人。科学316, 750-754(2007)。
刘春春,金景洋,徐辉,卜国强。纳特。神甫。9, 106-118(2013)。
桥本等人。生物。化学。286, 27081-27091(2011)。
Tsubuki, S, Takaki, Y. & Saido, T.C.《柳叶刀》361, 1957-1958(2003)。
Kalimo, H.等。Acta Neuropathol。Commun。1, 60(2013)。
程,I.H.等人。Nat,地中海。10, 1190-1192(2004)。
卡什,D.M.等人。神经学81, 1425-1433(2013)。
尼尔森,P.等。细胞的报道5, 61-69(2013)。
高野,J.等。生物。化学。280, 16175-16184(2005)。
斋藤等人。Nat,地中海。11, 434-439(2005)。
岩田,N.等人。j . >。24, 991-998(2004)。
恩雅,M.等。点。j .分册。154, 271-279(1999)。
斋藤等人。Nat。>。14, 1023-1032(2011)。
Sarnyai, Z.等人。Proc。国家的。学会科学。美国97, 14731-14736(2000)。
确认
我们感谢C.A. Lemere(布莱根妇女医院)和M. Higuchi(国家放射科学研究所)所作的宝贵讨论。我们也感谢高野E.、藤冈R.和富田Y.的技术援助。这项工作得到了理研脑科学研究所、教育、文化、体育、科学和技术部、卫生和福利部、分子成像计划资助、日本科学技术厅胚胎科学技术前导研究、细胞科学研究基金会和武田科学基金会的研究资助。
作者信息
作者及隶属关系
贡献
本研究由T.S.和T.C.S.设计,敲入小鼠的生成由S.I.支持,实验由T.S.、y.m.、N.M.和j.t.t.s.进行,J.T.、p.n.、N.I.和T.C.S.共同分析和解释数据。
相应的作者
道德声明
相互竞争的利益
t.c.s., t.s., N.I.和J.T.拥有一项名为“表达FAD APP 716的阿尔茨海默病模型小鼠及其使用”的美国专利。专利号为7,745,688。然而,作者将免费向学术界提供突变小鼠。
综合补充信息
补充图1生成新的AD鼠标模型的概念。
(一个) APP-Tg小鼠的内在问题。小鼠表达非生理性高水平的APP。由于APP与c-Jun - n端激酶相互作用蛋白-1 (jpp -1)相互作用,后者是肌动蛋白-1的中介,过表达的APP可能会扰乱轴突运输并产生人工表型。Aβ以外的APP片段,即。sAPP、CTF-β和AICD也过量生产。因此,在这些小鼠中观察到的各种表型是否真的由Aβ沉积引起仍然不确定。其他问题见补充表1。(b)设计新的小鼠模型。我们将小鼠Aβ序列人源化,并通过敲入技术引入瑞典和Beyreuther/Iberian突变。我们还培育了携带北极突变基因的突变小鼠。
补充图2生成程序应用程序NL-F / NL-F老鼠。
(一个) APP野生型等位基因、靶向载体和靶向等位基因。外显子16和17的突变用闭合三角形表示。ApaLI, NotI和XbaI也显示了酶切位点。Neo表示由lox/FRT序列包围的新霉素耐药基因盒,用于阳性选择。SA和LA分别表示目标向量的短臂和长臂。Southern blot分析中使用的5'和3'探针的退火位置位于目标等位基因之外。(b)外显子16和17发生突变。描述了基因组序列和氨基酸序列的变化。外显子16包含瑞典突变和人性化序列;外显子17包含北极(在情况下)应用程序NL-G-F / NL-G-F小鼠)和Beyreuther/Iberian突变。数字表示氨基酸在Aβ序列中的位置。(c)通过Southern blot分析鉴定种系传播。基因组DNA提取自应用程序NL-F / NL-F用XbaI和ApaLI酶切小鼠尾巴(克隆号271),并与图a中所示的5'和3'探针杂交,重复Southern blot分析两次以选择阳性克隆进行微量注射。(d)用PCR法对小鼠进行基因分型。上面的条带由野生型等位基因扩增而来,下面的条带由突变型等位基因扩增而来。(e) APP mRNA的Northern blot分析。使用小鼠app特异性探针检测从大脑中提取的总RNA。β-肌动蛋白作为内对照。我们通过密度测定法定量表达水平,发现野生型小鼠和突变型小鼠之间没有显著差异。数据表示平均值±s.e.m (n= 3).每组实验至少重复三次以确认结果。全长图像显示在补充图12.
补充图3 APP表达水平与神经炎症的Western blot分析及定量结果应用程序NL-F老鼠。
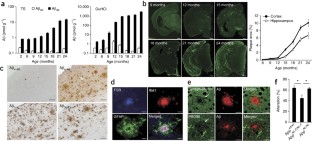
(一个)蛋白印迹分析APP及APP衍生片段应用程序NL-F / NL-F老鼠。应用APP n端抗体(22C11)、人Aβ序列抗体(6E10)和APP c端抗体。全长图像显示在补充图13.(b) APP的量化及其在大脑中的碎片应用程序问而且应用程序NL-FKI老鼠。免疫印迹实验中免疫反应条带的强度一个用密度分析法定量。我们发现,在野生型小鼠和突变型小鼠之间,22c11反应性APP或AICD的数量没有显著差异(n= 6的应用程序wt / wt, 6应用程序NL-F / wt, 6应用程序NL-F / NL-F, 4应用程序问/ wt4个应用程序问/问,单向方差分析)。人含a β序列(6e10反应性)APP和CTF-β信号随瑞典突变基因剂量的增加而增加;CTF-α信号降低。血清CTF-β和CTF-α水平应用程序NL-F / NL-F小鼠与小鼠相似应用程序问/问老鼠(n= 6的应用程序wt / wt, 6应用程序NL-F / wt, 6应用程序NL-F / NL-F, 4应用程序问/ wt4个应用程序问/问, sheffield的单向方差分析F测试)。数据表示均数±s.e.m (c) 18月龄儿童Iba1和GFAP信号皮质免疫反应性应用程序wt / wt,应用程序问/问而且应用程序NL-F / NL-F老鼠(图1 d)被量化。数据表示均数±s.e.m (n= 4的应用程序wt / wt, 6应用程序NL-F / NL-F4个应用程序问/问, sheffield的单向方差分析F测试中,* *P< 0.01)。
补充图4 2月龄APP、APP衍生片段及Aβ水平应用程序问,应用程序NL-F和APP23小鼠。
(一个)蛋白印迹分析APP及APP衍生片段应用程序NL-F / NL-F和APP23小鼠。看到图1一个详情请参考图例。全长图像显示在补充图13b.(抵扣) Aβ的稳态水平40和β42和Aβ的比值42/β40在老鼠的大脑里。图B和C分别显示了ts -可溶性和guhcl -可提取的Aβ的数量。图D和E显示了Aβ的比例42/β40分别在TS和GuHCl组分中。数据表示均数±s.e.m (n= 5的应用程序wt / wt, 4应用程序NL-F / wt, 5应用程序NL-F / NL-F, 4应用程序问/ wt4个应用程序问/问APP23的3个为Scheffe的单因素方差分析F测试中,* *P< 0.01)。
补充图5 Aβ在应用程序NL-F / NL-F老鼠。
(一个) Aβ斑块免疫组化染色应用程序NL-F / NL-F老鼠。6个月大的大脑切片应用程序NL-F / NL-F老鼠(n= 4)用抗a β抗体6E10免疫染色。右侧面板显示了左侧面板中正方形所指示区域的放大图像。我们检测到大约1 - 2个斑块应用程序NL-F / NL-F这个年龄段的皮层切片。(b)中Aβ物种的N端和c端结构应用程序NL-F / NL-F的大脑。6个月大的大脑切片应用程序NL-F / NL-F老鼠(n= 4)用4G8抗体联合Aβ抗体双染色1 - x,生成Aβ3 pe-x,生成Aβ×40和AβX-42.比例尺为100 μm (一个(左面板),25 μm (一个(右侧)和50 μm (b),分别。
补充图6 Aβ在APP23小鼠中的沉积。
(一个) Aβ的定量40和β42在APP23小鼠大脑中。结果表明,不同年龄guhcl可提取Aβ物种的数量不同。(b) APP23脑Aβ沉积。9月龄、12月龄和15月龄APP23小鼠脑切片用抗a β抗体4G8免疫染色。从12个月大开始检测到免疫反应性Aβ沉积(n= 4/时间点)。虽然敲入小鼠像人类一样开始在皮层中积累Aβ,但在Thy-1启动子的控制下,APP23小鼠同时在皮层和海马中积累Aβ。(c) APP23小鼠大脑中Aβ物种的N端和c端结构。18个月大的APP23小鼠大脑序列切片(n= 4) Aβ抗体免疫染色1 - x,生成Aβ3 pe-x,生成Aβ×40和AβX-42.比例尺为500 μm (b)和100 μm (c).
补充图7杂合子Aβ淀粉样变应用程序NL-F / wt老鼠。
24月龄和30月龄小鼠脑切片用抗a β免疫染色1 - x抗体(n= 6)。Aβ斑块可见于脑皮层应用程序NL-F / wt24月龄以上的小鼠,而在小鼠中未检测到斑块应用程序wt / wt而且应用程序问/问小鼠(数据未显示)。比例尺为200 μm。
补充图8散发性AD脑中的Aβ淀粉样变。
(一个)散发性AD脑组织中Aβ物种的N端和c端结构。零星AD患者的连续皮质切片(n= 4)用Aβ抗体免疫染色1 - x,生成Aβ3 pe-x,生成Aβ×40和AβX-42.(b)散发性AD脑的神经炎症。采用FSB、抗gfap抗体和抗iba1抗体三染色法分别检测Aβ斑块、星形细胞增生和微胶质细胞增生的炎症反应。(c)散发性AD的突触前改变。脑切片分别用4G8抗体和抗突触素抗体双染色。(d)散发性AD的突触后改变。脑切片分别用4G8抗体和抗psd95抗体双染色。我们在核心斑块观察到突触中断,但在弥漫性斑块未观察到。比例尺为50 μm (一个), 20 μm (b)和10 μm (c,d),分别。
补充图9 calpastatin缺失的表型应用程序NL-F / NL-F老鼠。
(一个钙钙蛋白缺乏对小鼠生存的影响应用程序NL-F / NL-F,应用程序问/问以及60周龄以上的APP-Tg小鼠。所有的小鼠系都被安置在相同的条件下。(n= 22的应用程序NL-F / NL-F, 24应用程序问/问, 25应用程序NL-F / NL-Fx投- / -20个应用程序问/问x投- / -) (b加速Aβ沉积应用程序NL-F / NL-Fx投- / -的大脑。使用针对Aβ不同n端结构的抗体对15月龄小鼠的脑切片进行免疫染色。比例尺为500 μm。(c)神经炎症增加应用程序NL-F / NL-Fx投- / -的大脑。使用抗iba1和抗gfap抗体对12个月大的小鼠的大脑切片进行双重染色。皮层免疫反应定量如图所示(n= 3,谢氏单因素方差分析F测试中,*P< 0.05和**P< 0.01)。比例尺为100 μm。(d) Aβ的生化量应用程序NL-F / NL-Fx投- / -的大脑。Aβ水平40和β42采用夹心ELISA法测定15月龄小鼠皮层TS和GuHCl组分的含量。数据表示均数±s.e.m (n= 5的应用程序问/问, 5应用程序问/问x投- / -, 6应用程序NL-F / NL-F4个应用程序NL-F / NL-Fx投- / -, Student-t test, *P< 0.05和**P< 0.01)。(e)记忆力减退应用程序NL-F / NL-Fx投- / -老鼠。y迷宫测试是用15个月大的老鼠进行的。数据表示均数±s.e.m (n= 9的应用程序问/问, 10应用程序问/问x投- / -, 9应用程序NL-F / NL-F11个应用程序NL-F / NL-Fx投- / -, sheffield的单向方差分析F测试中,*P< 0.05)。
补充图10 Western blot分析APP表达水平与神经炎症的定量结果应用程序NL-G-F老鼠。
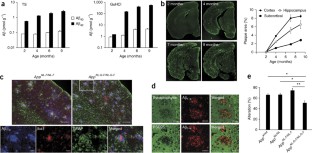
(一个)蛋白印迹分析APP及APP衍生片段应用程序NL-G-F / NL-G-F老鼠。详见图1A图例。全长图像显示在补充图13c.(b) APP及其在大脑中的片段量化应用程序NL-G-FKI老鼠。免疫印迹的免疫反应条带强度显示在一个用密度分析法定量。我们发现,在野生型小鼠和突变型小鼠之间,22c11反应性APP或AICD的数量没有显著差异(n= 4,单向方差分析)。人含a β序列(6e10反应性)APP和CTF-β信号随瑞典突变基因剂量的增加而增加;CTF-α信号降低。血清CTF-β和CTF-α水平应用程序NL-G-F / NL-G-F小鼠与对照组相似应用程序NL-F / NL-F小鼠(n = 4,谢氏单因素方差分析F测试)。与中提供的数据一致补充图10d, APP的6E10免疫反应性应用程序NL-G-F老鼠比那只小应用程序NL-F老鼠(n= 4,谢氏单因素方差分析F测试中,* *P< 0.01)。数据表示均数±s.e.m (c) 6月龄儿童Iba1和GFAP信号的皮质免疫反应应用程序wt / wt,应用程序NL-F / NL-F,应用程序NL-G-F / NL-G-F和18个月大的APPNL-F / NL-F对小鼠(图3d)进行定量。数据表示均数±s.e.m (n= 3的应用程序wt / wt, 4应用程序NL-F / NL-F(6个月),6个应用程序NL-G-F / NL-G-F5个应用程序Nl-F / Nl-F(18个月),谢菲单因素方差分析F测试中,*P< 0.05, **P< 0.01)。
补充图11抗体对Arctic Aβ的反应性应用程序NL-G-F / NL-G-F老鼠。
(一个)抗ap抗体表位图。(b)使用BNT77作为捕获抗体对北极AP种进行定量。BNT77与Aβ的中间部分结合。采用夹心ELISA试剂盒(Wako, Japan)。(c)使用BAN50作为捕获抗体对北极a β物种进行定量。BAN50与Aβ的n端区结合。BNT77和BAN50对北极Aβ的捕获能力弱于野生型Aβ。(d)免疫组化使用各种抗a β抗体。24个月大的大脑切片应用程序NL-F / NL-F小鼠按指示提取抗原后,使用不同表位的抗体进行免疫染色(上图);9个月大的婴儿应用程序NL-G-F / NL-G-F小鼠同样进行免疫染色(下图)。
补充图12杂合子Aβ沉积应用程序NL-G-F / wt老鼠。
(一个) Aβ的定量40和β42在杂合的APPNL-G-F / wt老鼠的大脑。一个β40和β42采用基于Arctic a β的标准曲线ELISA法定量2- 12月龄小鼠皮层TS和GuHCl组分的含量。BNT77作为捕获抗体。数据表示均数±s.e.m (n= 3,4,4,4和4/指定的时间点)。(b) Aβ沉积应用程序NL-G-F / wt的大脑。2个月,4个月,6个月,9个月和12个月大的大脑切片APPNL-G-F / wt用抗a β免疫染色小鼠x-42抗体比例尺为500 μm。斑块面积的定量方法与图1和图3中描述的方法相同。数据表示均数±s.e.m (n= 3,4,4,4和4/指定的时间点)。
补充信息
补充文字及图表
补充表1及补充图1 - 14 (PDF 2596kb)
权利和权限
关于本文
引用本文
斋藤,T.,松叶,Y.,三平,N.。et al。单应用程序敲入阿尔茨海默病的小鼠模型。Nat >17, 661-663(2014)。https://doi.org/10.1038/nn.3697
收到了:
接受:
发表:
发行日期:
DOI:https://doi.org/10.1038/nn.3697
这篇文章被引用
在阿尔茨海默病的APP-KI NL-G-F和NL-NL小鼠模型中播种人源性tau病理的病理和神经生理学结果
神经病理学通讯学报(2022)
地氟醚和七氟醚对老龄AppNL-G-F/NL-G-F小鼠运动学习缺陷的长期影响评估
分子的大脑(2022)
长期自愿锻炼后,敲入APPNL-G-F阿尔茨海默病小鼠模型对大脑病理、焦虑和认知功能的显著影响
阿尔茨海默氏症研究与治疗(2022)
通过高截止微透析测定野生型和阿尔茨海默病小鼠中单特异性和双特异性淀粉样蛋白β抗体的脑药代动力学
中枢神经系统的液体和屏障(2022)
CRISPR/ dcas9 - dnmt3a介导的APP靶向DNA甲基化挽救了阿尔茨海默病小鼠模型的大脑病理
转化神经退化(2022)
