文摘
积累的证据牵连到肠道微生物产生的代谢物的重要介质食源性host-microbial相声。在这里,我们回顾新兴数据表明微生物色氨酸副产物产生的蛋白水解作用影响宿主的健康。建议这些代谢物激活免疫系统通过绑定到芳基碳氢化合物受体(AHR),提高肠上皮屏障,刺激胃肠蠕动,以及肠道激素的分泌,产生抗炎,氧化或毒性作用在体循环,推定地调节肠道微生物组成。色氨酸副产物从而影响各种生理过程和可能导致肠道和系统性的健康和疾病的动态平衡。
介绍
多样化的和动态的人类胃肠道微生物群落健康和营养的起着至关重要的作用1。主机和肠道微生物群之间的互惠关系依赖于复杂的分子的相互作用,这是基本的肠道内稳态。尽管最近进展描述肠道微生物群的组成和功能有了许多新的发现对人类健康的肠道微生物群的角色,只有少数microbiota-generated代谢物影响宿主生理已确定,但其中包括短链脂肪酸(SCFA)来自细菌降解的膳食纤维2、二次胆汁酸来自细菌转化胆汁酸在结肠3和trimethylamine-N-oxide (TMAO)的产物microbial-host co-metabolism营养如磷脂酰胆碱,胆碱,l肉碱,出现在高脂肪的食物4,5。细菌代谢产物的作用来自蛋白质水解对宿主生理然而只有稀缺的注意力。尽管细菌蛋白质降解产物通常被认为是有害的6,最近的数据表明色氨酸副产物生成的肠道微生物群是肠道内稳态的重要贡献者。在这里,我们回顾最近的发现与微生物分解产物色氨酸和讨论未来的努力探索其潜在作用调解microbe-host交互(无花果。1)。由于可用研究色氨酸分解代谢物与健康通常关联或源自小鼠模型,还需要更多的研究来提供实实在在的色氨酸副产物和人类健康之间的联系。
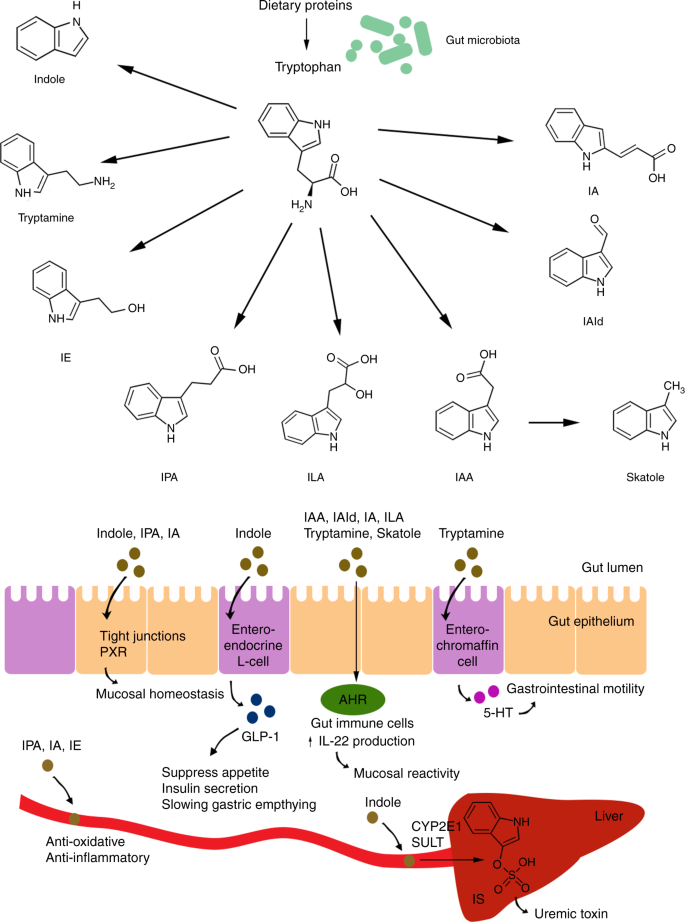
微生物的作用机制色氨酸分解代谢物在主机生理学。膳食蛋白质的退化导致色氨酸的释放,转换成各种副产物的肠道微生物群。色氨酸分解代谢物包括吲哚、色胺,indoleethanol (IE), indolepropionic酸(IPA) indolelactic酸(马尼拉),吲哚乙酸(IAA)、粪臭素,indolealdehyde (IAld)和indoleacrylic酸(IA)和在许多方面可能影响宿主的生理。吲哚、IPA和IA影响粘膜内稳态的肠道通透性下降可能是由孕烷X受体(PXR)。吲哚诱发释放glucagon-like肽1 (GLP-1) enteroendocrine L-cells。GLP-1众所周知,抑制食欲,胰岛素分泌和减缓胃排空。几个色氨酸副产物作用于肠道中的芳基碳氢化合物受体(AHR)免疫细胞,从而改变先天和适应性免疫反应ligand-specific的方式(例如IAld诱发增加生产interleukin-22 (il - 22生成)通过AHR激活)。色胺诱发释放5 -羟色胺(5 -羟色胺)肠嗜铬细胞的细胞。5 -刺激胃肠蠕动的作用在肠神经系统的神经元。色氨酸分解产物通过肠上皮细胞吸收,进入血液中,一些(例如音标,即IA)氧化和抗炎作用,而indoxyl-sulfate(是),这是在肝脏产生吲哚的CYP2E1和sulfotransferases(饥饿),在高浓度细胞毒性的影响
肠道细菌色氨酸分解代谢
色氨酸是人类的必需氨基酸,是由饮食蛋白(盒子1)。虽然大多数的摄取蛋白质在小肠消化和吸收7、依赖摄入大量的蛋白质和氨基酸(6 - 18 g /天)可能达到结肠8,一系列共生的细菌降解。细菌蛋白质分解代谢增加而增加蛋白质的摄入量,碳水化合物消耗在结肠,结肠pH值增加和延长结肠转运时间9,10,11,12。逐渐消耗的碳水化合物基质发生从近端到远端结肠导致细菌的分解代谢转变从saccharolytic蛋白水解发酵10。协议因此,浓度的酚类化合物降解芳香族氨基酸的人类肠道内容高出四倍比近端结肠远端结肠12。据报道,细菌蛋白水解专家增长潜力低于通才和saccharolytic /分解脂肪的专家,表明蛋白水解专家茁壮成长时的生态压力快速增长却降低了13。然而,色氨酸的退化不限于蛋白水解专家或远端结肠例如乳酸杆菌分解色氨酸在小鼠的胃和回肠14。报导了几个细菌物种,能够将色氨酸转化为吲哚和吲哚衍生物(表1)。已经1897年,色氨酸被发现转化成吲哚大肠杆菌(现在大肠杆菌),霍乱(现在霍乱弧菌)15。之后,吲哚的生产已经被用作诊断标记区分大肠杆菌从其他肠道细菌。因为吲哚已经100多年来,无数indole-producing物种已确定如先前所述审查16;因此这里不详细讨论这些。短暂,吲哚形成通过酶的作用发生tryptophanase (TnaA),这是在许多革兰氏阴性表达,以及包括革兰氏阳性细菌物种大肠杆菌、梭状芽孢杆菌种虫害和拟杆菌spp。12,16,17,18。最近,一些研究表明,肠道微生物物种产生各种各样的色氨酸通过其他各种代谢途径(图分解代谢物。2)。例如,sporogenes梭状芽胞杆菌将色氨酸转化为色胺,indolelactic酸(马尼拉)和indolepropionic酸(异丙醇)19,20.,21。同样的,消化链球菌属种虫害包括P。russellii, p . anaerobius和p . stomatis已知将色氨酸转化为indoleacrylic酸(IA)和异丙醇,可能由于存在phenyllactate脱水酶基因簇(fldAIBC这些物种的染色体上22。事实上,这种集群的同系物发现负责色氨酸转化为马尼拉和国际音标c . sporogenes21。此外,同系物基因被发现cadaveris梭状芽胞杆菌,肉毒梭状芽胞杆菌和消化链球菌属anaerobius21同意他们的能力产生出来17,21,22。另一组的细菌能够将色氨酸是乳酸杆菌。乳酸菌种虫害将色氨酸转化为indolealdehyde ILA通过(IAld)和芳香族氨基酸转氨酶(ArAT)和一个indolelactic酸脱氢酶(ILDH)14,23,24。瘤胃球菌属gnavus将色氨酸转化为色胺通过色氨酸脱羧酶酶的作用20.。几个拟杆菌物种,以及bartlettii梭状芽胞杆菌已报告生产马尼拉和吲哚乙酸(IAA)25,而双歧杆菌属种虫害已报告生产马尼拉25,26。最后,常见的肠道代谢物3-methylindole(粪臭素),已被广泛研究猪肉异味的原因,是由脱IAA拟杆菌种虫害和梭状芽胞杆菌spp。12,17,25,27。尽管几个物种能够在体外代谢色氨酸(表1),研究细菌物种的丰度与色氨酸的浓度分解代谢物在人类还需要确定人类肠道中的主要副产物色氨酸生产商。吲哚和IAA在人类粪便样本中发现的健康成人平均浓度的2.6毫米28和5µM29日,分别。然而,其他副产物色氨酸的浓度(IPA,伊拉,IAld色胺和IA)在人类肠道需要我们的知识没有评估。在血清中,意味着在健康成年人之前报道了IAA浓度(1.3µM),异丙醇(1.0µM),和伊拉(0.15µM)30.而最近的一项研究报道,平均血清异丙醇浓度50 nM31日。此外,微生物分解产物色氨酸的平均浓度在孕妇的尿液是最近报道IAA(61µM), methyl-IAA(8µM),色胺(9µM),和methyl-IPA(0.5µM)32。尽管报告的浓度差异,这些研究表明,在成人中,吲哚是最丰富的微生物分解产物色氨酸,其次是IAA和异丙醇。的可用性的方法测定微生物分解产物色氨酸浓度然而目前在生物标本是有限的28,32和更好的定量分析方法针对一个更大的各种各样的微生物色氨酸代谢产物是必要的。这种方法将使跨生物代谢物浓度的比较隔间之间(如粪便、血液和尿液)和不同的人群。
微生物色氨酸分解代谢物的作用机制
越来越多的文献表明,肠道微生物群色氨酸生成副产物的微生物群落的重要信号分子,以及host-microbial相声,并可能导致肠道和系统性的体内平衡(无花果。1)。
色氨酸代谢微生物的好处
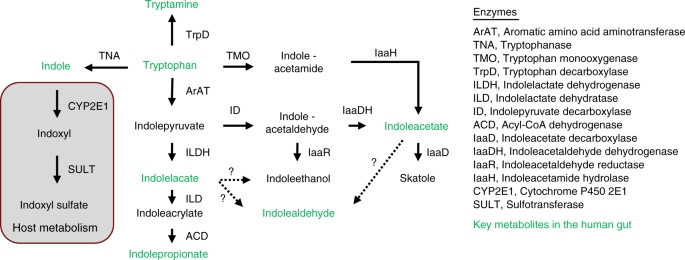
而肠道细菌色氨酸代谢产物与宿主之间的相互作用近年来受到越来越多的关注,回顾了在下面几节中,知识的好处色氨酸代谢与肠道微生物本身是有限的。色氨酸具有多种代谢功能,例如,纳入多肽链的细菌酶和作为辅因子NAD的前兆33。然而,最重要的是丰富的肠道环境可能是氧化还原内稳态的细菌需要维护。在肠道细菌发酵产生ATP的碳水化合物,通常包括氧化步骤。因此必须进行补偿减少。最近检查食品涉及乳酸菌的发酵34,微生物应用多种不同的反应为了找到最终电子受体允许他们平衡发酵代谢在缺乏氧气。同样在肠道,因此,色氨酸的吲哚丙酮酸转氨作用生成的可能被应用作为电子受体和行动减少到马尼拉的伊拉脱氢酶(无花果。2)。这种反应可能微调从而平衡氧化还原电位,给肠道微生物竞争优势。此外,细菌槽芳香族氨基酸的降解产物是可能发生在人类结肠35,并可能为特定的细菌提供生长优势在竞争激烈的肠道生态系统。
色氨酸分解代谢物作为信号和抗菌药物
吲哚都可以作为一个细胞间信号分子似乎是重要的微生物群落的影响孢子的形成,质粒稳定性、耐药、生物膜的形成和毒性16。同样,indoleethanol(即tryptophol)已被确定为一个群体感应分子在真菌36。这种代谢物也产生抗菌活性金黄色葡萄球菌,沙门氏菌血清和乳杆菌37,38。此外,即抑制嗜热细菌噬菌体复制,Geobacillussp。E26339在虾病毒复制40和寄生原生动物扩散41。ILA据报道,也有抗真菌活性青霉菌菌株42和抗菌活性大肠杆菌和b的仙人掌43。此外,有证据表明,吲哚影响线虫生存的秀丽隐杆线虫44,45。集体,这些不同的例子表明,吲哚发挥作用的调节器肠道微生物群落在王国包括细菌,真菌和病毒。然而,色氨酸分解代谢物是否调节哺乳动物肠道的微生物群落仍是未知的。
色氨酸分解代谢物作为芳基碳氢化合物受体配体
近年来,它已成为明显的细菌分解产物色氨酸包括色胺,粪臭素,IAA, IA, IAld,伊拉是芳基碳氢化合物作为配体受体(AHR)14,23,46,47。AHR是一个转录因子广泛表达的细胞免疫系统48气道高反应性和大量的研究已经证明,改变先天和适应性免疫反应激活ligand-specific时尚49,50,51。重要的是,色氨酸分解代谢物的亲和力老鼠和人类之间的不同气道高反应性47甚至在实验室老鼠菌株,四个等位基因编码不同形式的AHR是已知的存在52。气道高反应性而啮齿动物被发现绑定外源性配体2、3、7日8-tetrachlorodibenzo-p-dioxin (TCDD或二恶英)大约10倍的亲和力高于人类的大战53气道高反应性,最近的研究表明,人类具有较高的亲和力比鼠标的AHR tryptophan-derived配体47。气道高反应性在一起,这些研究表明,啮齿动物和人类的AHR展览不同的配位选择性,这是非常重要的考虑考虑到气道高反应性预测中的相互作用在人类往往基于啮齿动物研究。此外,在肠细胞系模型,发现了色氨酸分解代谢物是受体激动剂或拮抗剂取决于他们的分子结构46,54。最近的研究强调indole-induced AHR激活可能是细菌导致粘膜内稳态的一种方式。乳酸菌种虫害发现调节白介素(IL) -22通过IAld-mediated激活AHR粘膜内稳态,从而保护小鼠免受黏膜念珠菌病14。此外,治疗的老鼠有三个乳酸菌菌株的代谢色氨酸通过激活气道高反应性稀释肠道炎症,影响被废除的AHR拮抗剂29日。也乳酸菌bulgaricusOLL1181发现激活途径和抑制气道高反应性结肠炎小鼠模型55。进一步解密机制,最近对老鼠的研究表明这种乳酸菌通过IAld和伊拉激活AHR,重组上皮内CD4 + T辅助细胞在免疫调节T细胞(CD4 + CD8ααdouble-positive上皮内淋巴细胞)23。此外,伊拉发现抑制小鼠极化的辅助T 17 (TH17)细胞在体外24。这些研究表明色氨酸气道高反应性副产物通过影响天真的CD4 + T辅助细胞的分化成调节性T细胞和T (Treg)H17细胞。TH17 / Treg平衡自身免疫和炎症性疾病中起着重要的作用56。因此,发现色氨酸气道高反应性副产物作为配体可以提供新的见解如何微生物代谢物影响肠道的免疫系统,以及在体循环。此外,吲哚共生的细菌被发现提供的改进包括一系列不同的生物的健康秀丽隐杆线虫,果蝇和老鼠AHR-dependent地57。这就提出了一个有趣的可能性,色氨酸气道高反应性副产物通过人类也可能减少弱点和改善人们健康。
色氨酸分解代谢物和肠道屏障功能
在体外和体内研究表明,吲哚增强肠上皮屏障功能通过增加相关基因的表达在上皮细胞结构和功能的维护58,59。此外,还发现了异丙醇调节肠道屏障功能在老鼠体内异型生物质传感器作为配体,孕烷X受体(PXR),特别是在吲哚的存在60。激活PXR已被证明保护屏障功能结肠炎小鼠模型61年。此外,异丙醇被发现减少肠道通透性的老鼠喂食高脂肪的饮食62年。进一步强调音标和肠道屏障功能之间的联系,最近的一项研究殖民与野生型或无菌鼠fldC突变体c . sporogenes(异丙醇生产c . sporogenes需要一个完整的fldC基因),和显示fldC殖民的老鼠表现出显著增加渗透率FITC-dextran wild-type-colonized同行相比,整合水平枯竭的腔的音标21。还IA最近已被证明能够促进小鼠肠上皮屏障功能和减轻炎症反应通过促进杯状细胞分化和粘液,气道高反应性可能由激活22。总的来说,这些研究表明色氨酸分解代谢物信号通过PXR和AHR增强肠上皮屏障功能。
色氨酸分解代谢物和肠道激素分泌
吲哚已经作为信号分子,能够调节分泌的glucagon-like peptide-1 (GLP-1)结肠enteroendocrine L细胞无限增殖和初级老鼠63年。glp - 1在刺激中扮演着一个关键的角色从胰腺β细胞胰岛素分泌,抑制食欲和减缓胃排空64年。因此,肠道吲哚的水平可能影响食欲。高血清浓度的异丙醇最近与减少2型糖尿病的患病率和更好的胰岛素分泌和敏感性65年增加了证据指向一个假定的吲哚在调节葡萄糖代谢的作用,可能通过L cell-induced GLP-1的分泌。符合这一点,最近的一项研究发现,老鼠的饮食含有异丙醇的空腹血糖水平有显著降低而控制饮食喂养的老鼠66年。虽然吲哚衍生物的传感L-cells仍然是难以捉摸的,这似乎是可信的G protein-coupled受体(GPCRs),这是对各种营养物质和其他食物组件67年,也可能对微生物代谢产物包括色氨酸分解代谢物他处68年。尽管如此,这些研究需要做更多的研究来阐明如何色氨酸分解代谢物可能调节enteroendocrine系统包括葡萄糖代谢与代谢体内平衡。
色胺和肠胃蠕动
色胺,色氨酸产生的副产物c . sporogenes和瘤胃球菌属gnavus20.,是β-arylamine神经递质,它可能会影响肠道健康。在肠道,色胺诱导释放神经递质5 -羟色胺(5 -羟色胺)肠嗜铬细胞的细胞69年位于粘膜表面70年。5 -刺激胃肠蠕动的作用在肠神经系统的神经元70年。此外,使用一个美国商会与一段proximal-mid小鼠结肠粘膜,发现色胺本身引起的短路电流的显著变化,确认它可以影响离子在肠道上皮细胞分泌20.在胃肠蠕动,起着重要的作用。因此,色胺可以作为一种信号分子,影响肠转运时间,这是与肠道微生物组成、多样性和人类的新陈代谢10,71年。是否细菌生产色胺在肠易激综合症的发病机制中发挥作用,通常表现为慢性腹泻或慢性便秘72年,目前仍是个谜。一种特别感兴趣r . gnavus,这是在炎症性肠病(IBD)中73年,74年、生产色胺20.并利用粘蛋白75年,这表明它在近距离与肠嗜铬细胞的细胞。的确,r . gnavusmono-associated老鼠感应的几个色氨酸代谢基因与无菌鼠76年。作为r . gnavus是一种常见的肠道微生物群中发现大约90%的成年人吗77年和婴儿78年,这个物种产生色胺的能力可能会影响人类的健康。
色氨酸在体循环分解代谢物
色氨酸副产物也可能影响宿主的生理系统,因为它们是通过肠上皮细胞吸收,进入血液中19才会在尿液中排出10,32。人类肠道微生物之间的关联分析和体外细胞因子反应在全血微生物刺激发现负面关联干扰素γ(IFNγ)生产和细菌基因负责色氨酸转化为IE79年,这表明IE有消炎的作用。以往进行的调查显示,异丙醇羟基自由基的清道夫80年,抵抗氧化损伤在不同的组织81年,82年,83年。然而最近的一项研究发现,IA,但不出来有抗炎和氧化LPS-activated人类外周血单核细胞(PBMCs)表示为降低il - 6和IL-1βNRF2-ARE通路的分泌和激活22,一个通路建议对预防神经退行性疾病的治疗目标84年和炎症性肠病85年。同样,IAA和色胺减毒鼠巨噬细胞的促炎细胞因子反应文化和肝细胞文化以AHR-dependent方式86年色氨酸,这表明微生物分解代谢物可能影响肝脏的炎症反应。色氨酸分解代谢物的影响细胞因子的生产可能取决于AHR激活,因为它已被证明,AHR信号修改toll样受体(TLR)监管反应人类的树突细胞87年。增加了复杂性,据报道,感应可以增强SCFA AHR-mediated基因88年。
虽然一般吲哚似乎是有益的,一个例外是硫酸吲哚酚(是),这是一个host-microbial co-metabolite产生吲哚在肝脏细胞色素P450酶的行为,包括CYP2E1和sulfotransferase(饥饿)89年。这种代谢物特征通常是作为一个尿毒症毒素累积在慢性肾脏疾病(CKD)患者血清浓度约100µM 2µM相比健康的成年人90年,91年。AHR是一个强有力的兴奋剂吗92年阻力指标纤维化也许可以诱发93年、肾小球硬化94年血管内皮细胞功能障碍95年并在内皮细胞氧化应激96年。在无菌鼠是发现不了的,是取决于共生的细菌的生产吗19。因此,色氨酸操纵肠道微生物分解代谢的循环水平低可能是一个策略是,最近在无菌的演示和传统的老鼠18。肠道色氨酸分解代谢被转移,从是否将有益肾疾病需要在将来的研究中确认的。
色氨酸分解代谢物在健康和疾病
的色氨酸分解代谢物在各种生理过程的影响,我们将讨论三个领域中色氨酸分解代谢物可能发挥了重要作用。
早期的生活
的肠道微生物群组成的巨大的变化发生在第一年的生活97年,98年,这在很大程度上是由饮食的改变99年,One hundred.很有可能,肠道微生物色氨酸代谢也在这一时期变化。事实上,indole-producing大肠杆菌众所周知,丰富的生命第一周吗101年,随后双歧杆菌属物种,能够生产马尼拉报道26,开始主导母乳喂养婴儿的肠道微生物组One hundred.,101年,102年。后来,作为补充介绍了饮食,细菌属包括色氨酸异化物种等乳酸菌,瘤胃球菌属、拟杆菌属、消化链球菌属和梭状芽胞杆菌在婴儿的肠道变得丰富99年。结合这一事实色氨酸气道高反应性副产物通过激活免疫系统调节和教育上面了,这使得微生物分解产物色氨酸在生命早期非常相关的研究领域,没有得到太多的关注。在老鼠身上,AHR的产后扩张需要激活肠道淋巴细胞表达转录因子RORγt和肠道淋巴滤泡的形成,是免疫系统组件参与维护肠道内稳态和抵抗感染103年。这些线,最近表明,母体传播微生物派生的AHR配体形状老鼠的后代的早期免疫系统通过增加肠道组3先天淋巴细胞和F4/80 (+) CD11c(+)单核细胞104年。此外,交付模式和胎龄婴儿的报道影响尿代谢物水平属于色氨酸途径105年。最近的一项研究显示,膳食蛋白质消耗妥协适应性免疫反应和色氨酸的氨基酸改变人类婴儿microbiota-transplanted猪体内平衡人类轮状病毒感染106年新生儿猪,另一个研究表明,配方奶粉喂养相比,母猪喂食enterochomaffin细胞数量减少和转移色氨酸代谢从5 -羟色胺、色胺107年。总的来说,这些研究表明,产妇微生物群和饮食等因素,交付模式,妊娠年龄、婴儿早期的微生物群和饮食影响色氨酸代谢,这可能是必不可少的肠道屏障功能和免疫系统的发展。
炎症性肠病
在过去的十年中,炎症性肠病一直是研究最多的人类条件与肠道微生物群。有趣的是,血清色氨酸水平在IBD患者明显低于健康对照组,患者,尤其减少克罗恩病(CD)相比,患有溃疡性结肠炎(UC)108年。此外,据报道,血浆色氨酸水平降低的CD109年,110年,而粪便色氨酸水平升高与健康人相比111年。这些观察表明,色氨酸代谢的变化参与炎症性肠病的病因。符合这一点,色氨酸免费饮食增加易感性DSS-induced炎症小鼠112年。重要的是,不仅色氨酸似乎扮演一个角色在炎症性肠病的病因。也消耗肠道色氨酸的分解产物可能会影响炎症性肠病的严重程度,因为它是最近表明,炎症性肠病病人减少了粪便AHR受体激动剂IAA的含量29日。与此一致的是,AHR是IBD患者肠道组织的表达下调113年激活保护气道高反应性和人性化对结肠炎小鼠诱导调节性T细胞114年。此外,异丙醇选择性减少循环从人体血清活跃结肠炎与健康人相比31日和口服吲哚,以及音标发现改善小鼠的结肠炎症31日,115年。肠道微生物色氨酸代谢从而拥有承诺作为IBD患者的治疗目标,如果未来的研究将理清关系个人色氨酸分解代谢物和炎症的倾向。
神经系统疾病
多发性硬化(MS)是一种神经退行性自身免疫性疾病。星形胶质细胞,人口的细胞在中枢神经系统(CNS),被认为发挥重要作用的发病机制女士最近的一项研究显示,微生物分解代谢物的膳食色氨酸结合I型干扰素信号激活信号在气道高反应性星形胶质细胞和抑制中枢神经系统炎症在实验性自身免疫性脑脊髓炎)(实验性自身免疫性脑脊髓炎动物模型116年。此外,他们发现循环水平下降的AHR受体激动剂与女士个人,表明在吸收失衡,生产、受体激动剂可能导致气道高反应性或退化的女士和其他自身免疫性疾病的发病机制116年。因此,Laquinimod,口服药物,目前正在评估治疗MS和亨廷顿氏舞蹈症(HD),一种罕见的神经退行性疾病,最近被证明有抗炎作用由AHR在实验性自身免疫性脑脊髓炎117年。有趣的是,等离子体水平的异丙醇显著降低在主题与HD与健康对照组相比30.。因此,针对肠道微生物色氨酸代谢通过调节内源性肠道微生物群或改变饮食可能代表替代策略来预防和治疗女士和其他神经系统疾病。
未来的发展方向
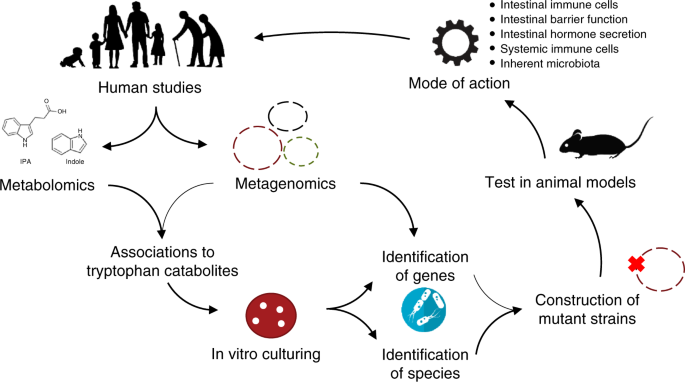
虽然能够生产色氨酸的几种细菌分解产物已确定(表1),人类肠道中的主要贡献者在很大程度上仍然未知,尽管大量的粪便宏基因组数据。我们锐意进取,以确定的贡献者,我们建议结合分析微生物(宏基因组)和量化的色氨酸分解代谢物(代谢组学)从人类粪便样本人群。这将允许我们识别重要的色氨酸分解代谢物和微生物物种之间的关联,可以使用经典的体外培养和代谢表型出现验证。因为色氨酸分解代谢物也比细菌产生的其他微生物,当务之急是我们远离分析只有细菌社区,开始探索人类肠道微生物群在王国。一旦我们确定相关的微生物和色氨酸婴儿肠道内分解代谢物,成年人和老年人,我们必须确定每个色氨酸的确切作用分解代谢物在主机(patho)生理学和解开他们的精确机制在不同肠段和细胞,以及在不同的组织利用动物模型和人类干预(图进行。3)。此外,有必要识别受体识别代谢物。此外,色氨酸的生物配体气道高反应性偏好分解代谢物当比较不同的哺乳动物22,47强调学习的重要性色氨酸分解代谢物的相互作用在人类细胞中,而不是仅仅在小鼠模型。目前,色氨酸副产物和人类健康之间的联系仍然是试探性的,与大多数数据关联或来自小鼠模型。因此,一个更全面的了解色氨酸的动力学分解代谢物及其功能的影响在生命的不同阶段,从出生到老年,从健康到疾病是必要的。这可能最重要的是扩展我们理解肠道host-microbial相声在健康和疾病。
提出战略识别tryptophan-catabolite-producing微生物和调查他们的角色在人类健康和疾病。虽然目前许多tryptophan-catabolite生产微生物被确认(表1),没有研究到目前为止他们的起点从人类数据,这意味着我们不知道的主要细菌生产色氨酸在人类肠道分解代谢物。因此,我们建议从人类研究出发,结合宏基因组和代谢组学数据,以确定最相关和潜在tryptophan-catabolite生产微生物。基于这些关联,选定目标物种应该在实验室培养和体外生产色氨酸的副产物应该评估生长实验和代谢分析。对他们的基因组结合知识,这将允许识别的基因负责代副产物色氨酸。击出识别感兴趣的基因将随后允许的功能基因的确认和测试特定基因的重要性最近在相关动物模型作为例证21。殖民与给定突变株与野生型小鼠同行将此外允许调查行动模式的色氨酸分解代谢物如肠道免疫细胞,肠道屏障功能、肠道激素分泌,固有的肠道微生物群,以及在体循环的免疫细胞。在一起,这将提供新的见解对色氨酸分解代谢物的作用,并导致更好的理解肠道微生物群在人类健康和疾病
引用
Tremaroli诉& Backhed f .功能性肠道微生物群和宿主之间的相互作用的新陈代谢。自然489年,242 - 249 (2012)。
Koh,。,De Vadder, F., Kovatcheva-Datchary, P. & Bäckhed, F. From Dietary Fiber to Host Physiology: Short-Chain Fatty Acids as Key Bacterial Metabolites.细胞165年,1332 - 1345 (2016)。
瓦尔斯特伦,。,Sayin, S. I., Marschall, H. U. & Bäckhed, F. Intestinal Crosstalk between Bile Acids and Microbiota and Its Impact on Host Metabolism.细胞。金属底座。24每周(2016)。
Koeth, r . a . et al .肠道菌群代谢左卡尼汀,红肉的营养,促进动脉粥样硬化。Nat,地中海。19,576 - 585 (2013)。
王,z . et al .肠道菌群代谢磷脂酰胆碱可以促进心血管疾病。自然472年57 - 63 (2011)。
Nyangale, e . P。,Mottram, D. S. & Gibson, G. R. Gut microbial activity, implications for health and disease: the potential role of metabolite analysis.j .蛋白质组Res。11,5573 - 5585 (2012)。
Evenepoel, p . et al .数量和鸡蛋蛋白质的命运逃离同化小肠的人类。点。j .杂志。277年G935-G943 (1999)。
吉布森,j . A。,Sladen, G. E. & Dawson, A. M. Protein absorption and ammonia production: the effects of dietary protein and removal of the colon.Br。j .减轻。35,61 - 65 (1976)。
麦克法兰,g . T。卡明斯,j . H。,Macfarlane, S. & Gibson, G. R. Influence of retention time on degradation of pancreatic enzymes by human colonic bacteria grown in a 3-stage continuous culture system.j:。Bacteriol。67年,520 - 527 (1989)。
Roager, h . m . et al .结肠转运时间与细菌新陈代谢和肠道粘膜营业额。Nat。Microbiol。116093 (2016)。本研究表明在人类结肠转运时间长导致细菌的分解代谢转变从saccharolytic蛋白水解发酵。
Geypens, b . et al .膳食蛋白质补充剂的影响在结肠细菌代谢产物的形成。肠道41,70 - 76 (1997)。
史密斯·e·a·&麦克法兰g . t .枚举的人类结肠细菌生产酚醛和indolic化合物:pH值的影响,碳水化合物可用性和保留时间异化的芳香族氨基酸代谢。j:。Bacteriol。81年,288 - 302 (1996)。
Vieira-Silva, s . et al . Species-function塑造人类肠道微生物的生态属性的关系。Microbiol Nat。116088 (2016)。
Zelante, t . et al .色氨酸从微生物群与芳基碳氢化合物分解产物受体和平衡通过interleukin-22粘膜反应。免疫力39,372 - 385 (2013)。这首次研究表明色氨酸分解代谢物如何预防真菌感染和肠道炎症。
史密斯,t .修改方法确定生产吲哚的细菌。j . Exp。地中海。2,543 - 547 (1897)。
李,j . j . h & Lee吲哚作为微生物细胞间信号的社区。《。牧师。34,426 - 444 (2010)。
Elsden, s R。,Hilton, M. G. & Waller, J. M. The end products of the metabolism of aromatic amino acids by clostridia.拱门。Microbiol。107年,283 - 288 (1976)。
Devlin, a . s . et al .调制循环尿毒症溶质通过理性的肠道微生物群的遗传操作。细胞。主机。微生物20.,709 - 715 (2016)。
Wikoff, w . r . et al .代谢组学分析揭示了大型哺乳动物血液代谢物肠道微生物区系的影响。Proc。《科学。美国106年,3698 - 3703 (2009)。
威廉姆斯,比比et al .发现和描述的肠道微生物群能产生神经递质色胺脱羧酶。细胞。主机。微生物16,495 - 503 (2014)。
多德,d . et al .肠道细菌途径代谢芳香族氨基酸分成九个循环代谢产物。自然551年,648 - 652 (2017)。一个优雅的研究结合遗传和代谢分析描述sporogenes梭状芽胞杆菌的途径生成芳香族氨基酸代谢产物。
Wlodarska, m . et al . Indoleacrylic酸由共生的消化链球菌属物种抑制炎症。细胞。主机。微生物22,25-37。e6 (2017)。
Cervantes-Barragan l . et al。这种乳酸菌诱发肠道上皮内CD4 (+) CD8αα(+)T细胞。科学357年,806 - 810 (2017)。这项研究表明,这种乳酸菌通过吲哚衍生物的生产,导致气道高反应性激活重组上皮内CD4 + T细胞的免疫调节T细胞。
Wilck: et al . Salt-responsive肠道共生的调节TH17轴和疾病。自然551年,585 - 589 (2017)。
罗素,w . r . et al。主要phenylpropanoid-derived代谢物可能出现在人体的肠道微生物发酵的蛋白质。摩尔。减轻。食物Res。57,523 - 535 (2013)。系统检查结肠细菌发酵芳香族氨基酸的能力包括色氨酸分解代谢物。
Aragozzini F。法拉利,。,Pacini, N. & Gualandris, R. Indole-3-lactic acid as a tryptophan metabolite produced by Bifidobacterium spp.达成。环绕。Microbiol。38,544 - 546 (1979)。
怀特黑德,t·R。、价格:P。,Drake, H. L. & Cotta, M. A. Catabolic Pathway for the Production of Skatole and Indoleacetic Acid by the Acetogen Clostridium drakei, Clostridium scatologenes, and Swine Manure.达成。环绕。Microbiol。74年,1950 - 1953 (2008)。
Darkoh C。,Chappell, C., Gonzales, C. & Okhuysen, P. A rapid and specific method for the detection of indole in complex biological samples.达成。环绕。Microbiol。81年,8093 - 8097 (2015)。
喇嘛,b . et al . CARD9影响结肠炎通过改变肠道微生物群色氨酸代谢为芳基碳氢化合物受体配体。Nat,地中海。22,598 - 605 (2016)。研究提供了证据,缺陷在先天免疫相关因子的表达,如CARD9,可以改变微生物分解产物色氨酸生产,然后修改宿主的免疫反应。
玫瑰花,h . d . et al .系统性“误解”:血浆代谢物在亨廷顿氏舞蹈症。安。中国。Transl。神经。2,756 - 768 (2015)。
Alexeev, e . e . et al . Microbiota-derived吲哚代谢物通过监管促进人类和小鼠肠道内稳态的白细胞介素- 10”受体。点。j .分册。188年,1183 - 1194 (2018)。
奶油蛋白甜饼、t . et al .尿中间体色氨酸作为肠道微生物代谢的指标。肛交。詹。学报987年,72 - 80 (2017)。
马尼,G。,Amici, A., Emanuelli, M., Raffaelli, N. & Ruggieri, S. Enzymology of NAD+ synthesis.放置Enzymol。遗传代数。摩尔。生物领域。73年,135 - 182 (1999)。
汉森,e . b .氧化还原反应在食品发酵。咕咕叫。当今。食品科学。19,98 - 103 (2018)。
Van der Meulen, R。Camu, N。,Van Vooren, T., Heymans, C. & De Vuyst, L. In vitro kinetic analysis of carbohydrate and aromatic amino acid metabolism of different members of the human colon.Int。j . Microbiol食物。124年,即(2008)。
陈,h·芬克& g . r .反馈控制真菌的形态发生芳醇。Dev的基因。20.,1150 - 1161 (2006)。
Elleuch l . et al。从一个新的陆地生物活性次生代谢产物链霉菌属TN262 sp。达成。物化学。Biotechnol。162年,579 - 593 (2010)。
Landete, j . M。,Rodríguez, H., De las Rivas, B. & Muñoz, R. High-added-value antioxidants obtained from the degradation of wine phenolics by Lactobacillus plantarum.j .食物防。70年,2670 - 2675 (2007)。
金,M。,Xu, C. & Zhang, X. The effect of tryptophol on the bacteriophage infection in high-temperature environment.达成。Microbiol。Biotechnol。99年,8101 - 8111 (2015)。
朱,f &金,m .嗜热生物代谢物的影响,tryptophol,防止虾白斑综合症病毒。鱼。贝类。Immunol。47,777 - 781 (2015)。
奥罕,我。,Şener, B., Kaiser, M., Brun, R. & Tasdemir, D. Inhibitory Activity of Marine Sponge-Derived Natural Products against Parasitic Protozoa.3月的药物847-58 (2010)。
欧诺瑞,a . h . et al .代谢足迹乳酸菌paracasei的抗真菌特性的调查。肛交。Bioanal。化学。408年,83 - 96 (2016)。
Narayanan, t . k . & Rao g . r . Beta-indoleethanol由念珠菌属物种和beta-indolelactic酸生产:抗菌和autoantibiotic行动。Antimicrob。代理Chemother。9,375 - 380 (1976)。
李,黄永发。et al . Indole-associated捕食线虫线虫和细菌之间的相互作用。环绕。Microbiol。19,1776 - 1790 (2017)。
Bommarius, et al。一个家庭的吲哚调节毒性和致病性大肠杆菌的志贺毒素的生产。《公共科学图书馆•综合》8e54456 (2013)。
程,y . et al。芳基碳氢化合物的色氨酸代谢产物受体活动Colonocytes成年老鼠。药物金属底座。Dispos。43,1526 - 1543 (2015)。
哈伯德,t . d . et al .适应人类的芳基碳氢化合物受体感应microbiota-derived吲哚。科学。代表。512689 (2015)。本文展示了适应人类的AHR绑定吲哚作为人类AHR选择性受体激动剂,暗示某种程度的AHR的进化适应。
袜,B。,Di Meglio, P., Gialitakis, M. & Duarte, J. H. The aryl hydrocarbon receptor: multitasking in the immune system.为基础。启Immunol。32,403 - 432 (2014)。
昆塔纳,f . j . et al .控制T (reg)和T (H) 17细胞分化的芳基碳氢化合物的受体。自然453年,65 - 71 (2008)。
Bessede, a . et al .芳基碳氢化合物受体疾病控制的公差防御通路。自然511年,184 - 190 (2014)。
甘地,r . et al .激活的芳基碳氢化合物1型受体诱发人类调节性T细胞样的,Foxp3(+)调节性T细胞。Immunol Nat。11,846 - 853 (2010)。
波兰,一个。,Palen, D. & Glover, E. Analysis of the four alleles of the murine aryl hydrocarbon receptor.摩尔。杂志。46,915 - 921 (1994)。
Ramadoss, p . & Perdew g . h .使用2-Azido-3 - [125 i] iodo-7 8-dibromodibenzo-p-dioxin作为探针来确定人类和小鼠的相对配体亲和芳基碳氢化合物在培养细胞受体。摩尔。杂志。66年,129 - 136 (2004)。
金,U.-H。et al . Microbiome-Derived色氨酸代谢产物和芳基碳氢化合物Receptor-Dependent受体激动剂和拮抗剂活动。摩尔。杂志。85年,777 - 788 (2014)。
Takamura, t . et al .乳酸菌发酵剂OLL1181保加利亚激活芳基碳氢化合物受体通路,抑制结肠炎。Immunol。细胞生物。89年,817 - 822 (2011)。
Noack, m & Miossec, p . Th17和调节性T细胞平衡自身免疫和炎症性疾病。Autoimmun。牧师。13,668 - 677 (2014)。
Sonowal, r . et al .吲哚从共生的细菌扩展健寿。Proc。《科学。美国114年E7506-E7515 (2017)。
邦萨尔,T。,Alaniz, R. C., Wood, T. K. & Jayaraman, A. The bacterial signal indole increases epithelial-cell tight-junction resistance and attenuates indicators of inflammation.Proc。《科学。美国107年,228 - 233 (2010)。研究首次提出,吲哚增强上皮屏障属性和减弱炎症。
什y . et al .共生体bacteria-dependent吲哚生产提高结肠上皮屏障功能。《公共科学图书馆•综合》8e80604 (2013)。
马纳尔,m . et al .共生细菌代谢物调节胃肠粘膜屏障功能,通过异型生物质传感器PXR和toll样受体4。免疫力41,296 - 310 (2014)。
Garg a等。孕烷X受体激活减弱炎症反应肠上皮屏障功能障碍通过抑制细胞因子诱导肌球蛋白轻链激酶表达和c-Jun n端激酶1/2激活。j .杂志。其他实验。359年,91 - 101 (2016)。
珍妮丝,m . et al . Microbiota-derived色氨酸吲哚增加胃分流手术后和减少肠道通透性体外和体内。Neurogastroenterol。Motil。30.e13178 (2017)。
Chimerel, c . et al .细菌代谢物从肠道enteroendocrine L吲哚调节肠促胰岛素分泌细胞。细胞的代表。9,1202 - 1208 (2014)。本文表明GLP-1 enteroendocrine L细胞分泌物接触吲哚调制的浓度中发现的类似人类的大肠。
霍尔斯特,j。j Glucagon-like肽的生理1。杂志。牧师。87年,1409 - 1439 (2007)。
梅洛,v . d . et al . Indolepropionic小说酸和脂质代谢产物与2型糖尿病的风险较低的芬兰糖尿病预防研究。科学。代表。746337 (2017)。
Abildgaard,。,Elfving B。Hokland, M。,Wegener, G. & Lund, S. The microbial metabolite indole-3-propionic acid improves glucose metabolism in rats, but does not affect behaviour.拱门。杂志。物化学。1 - 7,https://doi.org/10.1080/13813455.2017.1398262(2017)。
Reimann F。,Tolhurst, G. & Gribble, F. M. G-Protein-Coupled Receptors in Intestinal Chemosensation.细胞。金属底座。15,421 - 431 (2012)。
hust, a S。,Trauelsen, M., Rudenko, O., Hjorth, S. A. & Schwartz, T. W. GPCR-Mediated Signaling of Metabolites.细胞。金属底座。25,777 - 796 (2017)。
高木,M。,Mawe, G. M., Barasch, J. M., Gershon, M. D. & Gershon, M. D. Physiological responses of guinea-pig myenteric neurons secondary to the release of endogenous serotonin by tryptamine.神经科学16,223 - 240 (1985)。
Mawe、通用汽车和霍夫曼,j . m . 5 -羟色胺信号gut-functions,障碍和治疗目标。Nat,启杂志。乙醇。10,473 - 486 (2013)。
Vandeputte, d . et al .粪便一致性与肠道微生物群的丰富性和组成密切相关,菌群和细菌的增长速度。肠道65年57 - 62 (2015)。
花边,b E。,Chey, W. D. & Lembo, A. J. New and Emerging Treatment Options for Irritable Bowel Syndrome.杂志。乙醇。(n Y)11- (2015)。
Png, c . w . et al .黏液溶解的细菌与炎症性肠病患病率增加粘膜增强体外利用粘蛋白由其他细菌。点。j .杂志。105年,2420 - 2428 (2010)。
Joossens, m . et al .失调患者粪便微生物群的克罗恩氏病和他们亲属的影响。肠道60,631 - 637 (2011)。
Tailford l . e . et al。发现人类肠道微生物群的分子内trans-sialidases表明小说粘膜适应性机制。Commun Nat。67624 (2015)。
霍夫曼,t . w . et al .微生物与炎性肠道疾病有关的失调在无菌老鼠差别影响宿主的生理。Isme。J。10,460 - 477 (2016)。
秦,j . et al。人类肠道微生物基因目录建立了宏基因组测序。自然464年59 - 65 (2010)。
Sagheddu, V。,Patrone, V., Miragoli, F., Puglisi, E. & Morelli, L. Infant Early Gut Colonization by Lachnospiraceae: High Frequency of Ruminococcus gnavus.前面。Pediatr。457 (2016)。
Schirmer, m . et al。人类肠道微生物与炎性细胞因子的生产能力。细胞167年,1125 - 1136。e8 (2016)。
Chyan, y . j . et al。有效的神经保护属性对老年痴呆症的β-淀粉样蛋白内源性melatonin-related吲哚结构,indole-3-propionic酸。生物。化学。274年,21937 - 21942 (1999)。
黄,i . k . et al . Indole-3-propionic酸变弱缺血海马神经元损伤和氧化应激。j . >。Res。87年,2126 - 2137 (2009)。
Karbownik, M。Stasiak, M。Zasada, K。,Zygmunt, A. & Lewinski, A. Comparison of potential protective effects of melatonin, indole-3-propionic acid, and propylthiouracil against lipid peroxidation caused by potassium bromate in the thyroid gland.j .细胞。物化学。95年,131 - 138 (2005)。
Karbownik, M。Stasiak, M。Zygmunt,。Zasada, K。&lewiński, A. Protective effects of melatonin and indole-3-propionic acid against lipid peroxidation, caused by potassium bromate in the rat kidney.细胞。物化学。功能。24,483 - 489 (2006)。
乔希,g . & Johnson j . a . Nrf2-ARE通路:一个有价值的目标治疗神经退行性疾病的治疗。最近的帕特。中枢神经系统药物。7,218 - 229 (2012)。
陆,M.-C。et al . Keap1-Nrf2保护蛋白质间交互作用的抑制剂NCM460结肠细胞,减轻实验性结肠炎。科学。代表。626585 (2016)。
Krishnan, s . et al .肠道Microbiota-Derived色氨酸代谢产物调节炎症反应在肝细胞和巨噬细胞。细胞的代表。23,1099 - 1111 (2018)。
卡,s . et al。芳基碳氢化合物修改toll样受体信号receptor-regulated反应人类的树突细胞。拱门。Toxicol。91年,2209 - 2221 (2016)。
金,U.-H。等短链脂肪酸增强芳基碳氢化合物(啊)响应鼠标Colonocytes Caco-2人类结肠癌细胞。科学。代表。710163 (2017)。
Banoglu E。,Jha, G. G. & King, R. S. Hepatic microsomal metabolism of indole to indoxyl, a precursor of indoxyl sulfate.欧元。j .药物金属底座。Pharmacokinet。26,235 - 240 (2001)。
吴,I.-W。等人p-Cresyl硫酸盐和硫酸吲哚酚预测慢性肾脏疾病的进展。Nephrol。拨号。移植。26,938 - 947 (2011)。
金,h . y . et al .硫酸吲哚酚(是)介导的免疫功能紊乱引起内皮损伤患者终末期肾病(ESRD)。科学。代表。73057 (2017)。
施罗德,j . c . et al .尿毒症毒素硫酸3-Indoxyl是人类芳基碳氢化合物的一个强大的内生受体激动剂受体。生物化学49,393 - 400 (2010)。
Motojima, M。,Hosokawa, A., Yamato, H., Muraki, T. & Yoshioka, T. Uremic toxins of organic anions up-regulate PAI-1 expression by induction of NF-κB and free radical in proximal tubular cells.肾脏Int。63年,1671 - 1680 (2003)。
丹羽宇一郎,t &伊势,m .硫酸吲哚酚循环尿毒症毒素,刺激肾小球硬化的进展。j .实验室。中国。地中海。124年,96 - 104 (1994)。
窦,l . et al .尿毒症溶质p-cresol硫酸吲哚酚抑制内皮细胞增殖和伤口修复。肾脏Int。65年,442 - 451 (2004)。
窦,l . et al .尿毒症溶质硫酸吲哚酚诱发内皮细胞氧化应激。j . Thromb。Haemost。5,1302 - 1308 (2007)。
Yatsunenko, t . et al .人类肠道微生物组在年龄和地理。自然486年,222 - 227 (2012)。
Bergstrom, A . et al .肠道菌群在早期建立的生活:一个纵向,探索性研究的一大群丹麦婴儿。达成。环绕。Microbiol。80年,2889 - 2900 (2014)。
劳尔森m . f . et al .婴儿肠道微生物群的发展是由过渡到家庭食物孕妇肥胖独立的。mSphere1e00069-15 (2016)。
劳尔森,m F。巴尔,m . I。,Michaelsen, K. F. & Licht, T. R. First Foods and Gut Microbes.前面。Microbiol。8356 (2017)。
Backhed, f . et al .动力学和稳定的人类肠道微生物在生命的第一年。细胞。主机。微生物17,690 - 703 (2015)。
Bazanella, m . et al .随机对照试验的影响与双歧杆菌早期干预健康婴儿粪便微生物群和代谢物。点。j .中国。减轻。106年,1274 - 1286 (2017)。
吻,e·a·等。自然芳基碳氢化合物受体配体控制器官发生肠道淋巴滤泡。科学。(80 -)。334年,1561 - 1565 (2011)。
戈麦斯·阿奎罗,m . et al .孕产妇微生物群驱动器产后早期先天免疫的发展。科学。(80 -)。351年,1296 - 1302 (2016)。研究首次表明,色氨酸分解代谢物可能形状产后早期免疫的组成和功能。
山,c . j . et al .肠道微生物群组成的进化从出生到24周INFANTMET队列。微生物组521岁(2017年)。
费舍尔,d . d . et al .蛋白质营养不良改变色氨酸和血管紧张素转换酶2体内平衡和自适应免疫反应在人类Rotavirus-Infected无菌的猪与人类婴儿粪便微生物群移植。中国。疫苗。Immunol。24e00172-17 (2017)。
Saraf, m . k . et al .公式饮食驱动的微生物群色氨酸代谢变化从5 -羟色胺、色胺在新生儿猪结肠。微生物组577 (2017)。
尼古拉斯,et al。增加色氨酸代谢与活动相关的炎性肠道疾病。胃肠病学153年,1504 - 1516。e2 (2017)。
Hisamatsu, t . et al。小说、客观、多元生物标志物组成的等离子体氨基酸概要文件为炎症性肠病的诊断和评估。《公共科学图书馆•综合》7e31131 (2012)。
古普塔:k . et al .血清色氨酸的分析分解代谢途径:与克罗恩病相关的活动。Inflamm。肠道说。18,1214 - 1220 (2012)。
简颂,j . et al .代谢组学揭示代谢生物标记的克罗恩病。《公共科学图书馆•综合》4e6386 (2009)。
桥本,t . et al . ACE2链接氨基酸营养不良微生物生态学和肠道炎症。自然487年,477 - 481 (2012)。
Monteleone, et al .芳基碳氢化合物receptor-induced信号调控的il - 22生成生产和抑制胃肠道炎症。胃肠病学141年,237 - 248 (2011)。248. e1。
Goettel, j . a . et al .激活AHR是预防结肠炎的人源化小鼠的T细胞。细胞的代表。17,1318 - 1329 (2016)。
Whitfield-Cargile, c . m . et al . microbiota-derived代谢物吲哚减少粘膜炎症和损伤小鼠模型的非甾体抗炎药肠病。肠道微生物7,246 - 261 (2016)。
Rothhammer, v . et al . I型干扰素和微生物代谢产物色氨酸调节星形胶质细胞活动和中枢神经系统炎症通过芳基碳氢化合物的受体。Nat,地中海。22,586 - 597 (2016)。该研究提供了证据,色氨酸代谢产物调节中枢神经系统的活动居民细胞并抑制神经炎症。
凯,j . et al . Laquinimod实验性自身免疫性脑脊髓炎逮捕通过激活的芳基碳氢化合物的受体。Proc。《科学。113年E6145-E6152 (2016)。
Honeyfield特区&卡尔森,j . r .吲哚乙酸和相关吲哚对乳酸菌的影响sp。11201年应变增长,吲哚乙酸分解代谢,3-Methylindole形成。达成。环绕。Microbiol。56,1373 - 1377 (1990)。
确认
作者感谢马丁•劳尔森弗雷德里克和Egon本奇汉森有益的讨论。这项工作是创新基金支持的丹麦(批准号11 - 116163/0603 - 00487 b;中心的肠道,谷物和蔬菜)。
作者信息
作者和联系
贡献
H.M.R.起草文本和数字的输入从T.R.L.两位作者修改和定稿出版的手稿。
相应的作者
道德声明
相互竞争的利益
作者宣称没有利益冲突。
额外的信息
出版商的注意:施普林格自然保持中立在发表关于司法主权地图和所属机构。
权利和权限
开放获取本文是基于知识共享署名4.0国际许可,允许使用、共享、适应、分布和繁殖在任何媒介或格式,只要你给予适当的信贷原始作者(年代)和来源,提供一个链接到Creative Commons许可,并指出如果变化。本文中的图片或其他第三方材料都包含在本文的创作共用许可,除非另有说明在一个信用额度的材料。如果材料不包括在本文的创作共用许可证和用途是不允许按法定规定或超过允许的使用,您将需要获得直接从版权所有者的许可。查看本许可证的副本,访问http://creativecommons.org/licenses/by/4.0/。
关于这篇文章
引用这篇文章
Roager,莫莱森,licht, T.R. Microbial tryptophan catabolites in health and disease.Nat Commun93294 (2018)。https://doi.org/10.1038/s41467 - 018 - 05470 - 4
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41467 - 018 - 05470 - 4
本文引用的
环境效应variance-based弹性选择肠道代谢组的兔子
进化遗传学的选择(2023)
在结直肠癌代谢重编程:监管网络和治疗
细胞和生物科学(2023)
不同宫颈tissue-adherent和腔的微生物社区与粘膜宿主基因表达和蛋白质含量在肯尼亚的性工作者
微生物组(2023)
Microbiota-derived色氨酸代谢产物indole-3-lactic酸与肠道缺血/再灌注损伤通过积极的狂吠和Nrf2的监管
转化医学杂志》(2023)
短期的脱脂牛初乳喂养减轻肠道炎症通过代谢物的变化和微生物群在鸡的动物模型
动物微生物(2023)