文摘
背景
乳糜泻(CD)是一种自身免疫性肠病引发的谷蛋白的摄入。对个人(GS)不能容忍谷蛋白,可能出现胃肠道症状类似的CD,但整体临床情况一般不太严重,不伴有组织转谷氨酰胺酶自身抗体的赞同或自身免疫并发症。通过研究和比较粘膜与肠屏障功能相关基因的表达,以及先天和适应性免疫的CD与GS相比,我们试图更好地理解这两个gluten-associated障碍之间的异同。
方法
CD, GS和健康,gluten-tolerant个人参加这个研究。肠道通透性是评估使用乳果糖和甘露醇探测器,和粘膜活检标本收集研究基因的表达和免疫屏障功能。
结果
与CD, GS不是与肠道通透性增加有关。事实上,这是在GS与控件(相比显著降低P= 0.0308),平行的显著增加表达claudin (CLDN) 4 (P= 0.0286)。相对于控制,适应性免疫标记白介素(IL) 6 (P= 0.0124)和IL-21 (P= 0.0572)被上级表达CD但不是在GS,而表达的先天免疫标记toll样受体(TLR) 2在GS但不增加CD (P= 0.0295)。最后,t调节细胞标记FOXP3的表达显著降低GS相对于控件(P= 0.0325)和CD患者(P= 0.0293)。
结论
这项研究表明,这两个gluten-associated障碍,CD和GS,不同临床实体,它有助于GS的表征gluten-induced激活先天条件与普遍,而非自适应免疫反应没有检测到粘膜屏障功能的变化。
背景
谷蛋白的结构蛋白成分是谷物小麦、黑麦和大麦,依据各种面粉和wheat-derived食品消费在整个世界。可能引入含谷蛋白的谷类,发生在大约10000年前与农业的出现,代表着一种“进化”的错误,建立人类疾病相关蛋白的条件曝光,其中最著名的是由自适应免疫系统:小麦过敏和乳糜泻(CD)。在这两种条件下,蛋白的反应是由t细胞激活胃肠粘膜。然而,在小麦过敏,免疫球蛋白E的交联(IgE)重复序列蛋白肽(例如,Ser-Gln-Gln-Gln - (Gln) Pro-Pro-Phe)触发释放化学介质,如组胺、嗜碱粒细胞和肥大细胞(1]。相比之下,CD,影响到大约1%的普通人群,是一种自身免疫性疾病,特定的血清学标记所预示的升值,尤其是血清antitissue转谷氨酰胺酶(tTG)自身抗体,由自身免疫肠病特征这一条件和自身免疫并发症。
除了CD和小麦过敏,在某些情况下的谷蛋白反应过敏和自身免疫机制。这些通常被定义为谷蛋白敏感性(GS) [2- - - - - -5]。一些个人经验遇险时吃含谷蛋白制品和显示改进后无谷蛋白饮食可能GS而不是CD。GS病人无法容忍面筋和开发一个吃面筋时不良反应,通常,不同于CD,不会导致小肠损伤。虽然GS的胃肠道症状可能与相关的CD,整个临床情况一般不太严重,不伴有tTG自身抗体的赞同或自身免疫性疾病。通常,通过排除诊断,排除饮食和“开放的挑战”(即含谷蛋白食品的监测重新)通常用于评估病人的健康状况的改善是否消除或减少蛋白的饮食。
大量的在体外研究已经证实了谷蛋白的细胞毒性的主要抗原,醇溶蛋白。醇溶蛋白具有凝集活性,减少f -肌动蛋白含量,抑制细胞生长,诱导细胞凋亡,改变氧化还原平衡,引起细胞骨架的重排通过zonulin通路和紧密连接的损失(TJ)能力的胃肠粘膜(6- - - - - -9]。gluten-induced条件的多样性与免疫系统反应的概念和处理触发环境因素,醇溶蛋白,以不同的方式。在目前的研究中,我们试图获得最初的知识对肠道屏障功能和免疫应答与GS谷蛋白的病人。具体来说,我们有兴趣在多大程度上理解先天和适应性免疫通路被激活在GS相比CD。为了实现这些目标,我们看了粘膜的表达与肠屏障功能相关的基因和免疫参数已知的或隐含在CD。调节异常的结果提供了第一个文档的基因和途径可能参与了GS的发病机制,而且,与此同时,有助于改善我们的理解过程导致CD和其他自体免疫现象。
方法
GS的定义
GS的病人被定义为那些病人的CD,小麦过敏和其他临床重叠(1型糖尿病、炎症性肠病的疾病幽门螺杆菌感染)已被排除,其症状是由谷蛋白暴露和减轻谷蛋白撤军。所有登记患者接受了面筋的挑战在临床监督下进行了大约4个月。最后的挑战,病人接受了CD血清学筛查,人类白细胞抗原(HLA)DQ2 / DQ8打字和上层与十二指肠内镜活检。一旦进行内窥镜检查,患者在无谷蛋白饮食和其症状监测。GS患者被认为是那些消极的自身抗体血清学(肌内膜antibodies-immunoglobulin (EMA-IgA)和tTG-IgA),正常粘膜(沼泽阶段0)或增加上皮内淋巴细胞(沼泽阶段1)和改善症状在几天内实现的饮食。为了避免任何可能的选择偏差和证明这些患者不同于CD患者中,我们选择招收每个病人履行上述谷蛋白敏感性的定义。
主题
同意了从所有登记对象调查的性质解释后,按照批准的协议从那不勒斯大学的机构审查委员会。共有26个GS患者诊断根据上述标准被录取。相比之下,42活跃CD患者招募根据修改后的2004标准的欧洲社会儿科胃肠病学,肝脏病学和营养(ESPGHAN) [10]。最后,39的对照组个体接受胃镜检查的消化不良。我们有限的对照组个体完全消化不良的症状,没有潜在的炎症正常红细胞沉降率证明,c反应蛋白和粘蛋白评估。这些课程没有CD或GS,以下称为消化不良的控制(DC)。
总结在表主题特征1。每组实验中,代表小组的CD, GS和直流分析受试者的同意的基础上参与的一部分或全部提出研究和材料之间的转让协议机构参与这个项目。至少六个收集十二指肠活检组织学评价和基因表达。没有选择偏见基于性别、年龄或类型的症状被观察到。
肠道通透性测定
在活的有机体内渗透率决心通过乳果糖/甘露醇(LA / MA)测试如前所述[11]。两个糖探针的检测和测量尿液中是由高效阴离子交换色谱法加上脉冲测量电流的检测,它允许直接量化nonderivative碳水化合物与梯度Dionex模型dx - 500泵模块GP40和样品环50μl。样本装上CarboPac pa - 100卫队列和筛选了NaOH-NaAc梯度(美国Dionex,桑尼维尔CA)。
组织学和免疫组织化学的空肠的活检
串行部分(4μm)从十二指肠formalin-fixed准备,石蜡包埋切片。活检标本进行组织学根据湿地分类(12,13]。免疫染色鉴定上皮内淋巴细胞(IELs)所描述的其他地方执行14]。Acetone-fixed部分(5μm)沾CD3单克隆抗体(1:200;Dako、意大利米兰)和t细胞受体γδ(TCRγδ)(1:50;美国热科学,罗克福德,IL)使用peroxidase-antiperoxidase协议。部分终于沾Mayer的苏木精(Sigma-Aldrich,圣路易斯,密苏里州,美国)。IEL密度计算是肠上皮细胞的百分比(ECs)。所有幻灯片都分析了两个观察者对这些过程也不清楚。
粘膜测定基因表达
肠道基因表达测定,定量实时聚合酶链反应(qPCR)试验如前所述15]。小肠活检从参与的受试者均质和总RNA提取使用试剂盒试剂(美国纽约表达载体,大岛)。引物和探针qPCR特定的成绩单的18岁作为管家基因控制从应用生物系统公司购买(福斯特城、钙、美国)。qPCR使用TaqMan协议执行实时PCR系统和应用生物系统公司7500快。放大条件如下:50°C 2分钟和10分钟95°C,紧随其后的是50周期在95°C 15秒和60°C 1分钟。数据计算周期阈值的改变(ΔCT感兴趣的基因18岁并表示为百分数18岁(即2-ΔCT×100)。
统计分析
所有的数据进行了分析和画使用Prism 5.0版本软件(美国GraphPad软件,拉霍亚,CA)。大多数变量检查在这项研究似乎是安排在非正态,正偏态分布,使得传统的参数统计误导。因此,数据所描述的中位数和四分位范围(差),和变化的程度组间决心利用克鲁斯卡尔-沃利斯非参数算法。小动物——一张长有Mann-WhitneyU测试(MWU)用于成对比较。是水平的意义P< 0.05。
结果
GS受试者的临床和实验室特点
完成了GS诊断标准的病人症状重叠部分)(见方法经历了CD患者(见表1),但他们的症状后几天内解决的实现无麸质饮食,和他们保持无症状为整个随访期间(4年)。有趣的是,48%的GS患者anti-gliadin抗体(AGA)阳性,和57%的人hla dq2艾滋病患者和/或hla dq8艾滋病患者。AGA-positive GS患者的百分之五十六hla dq2艾滋病患者和/或hla dq8艾滋病,而剩下的44%的人HLA负,表明AGA生产不相关hla dq2限制和/或hla dq8限制演讲。
肠道通透性
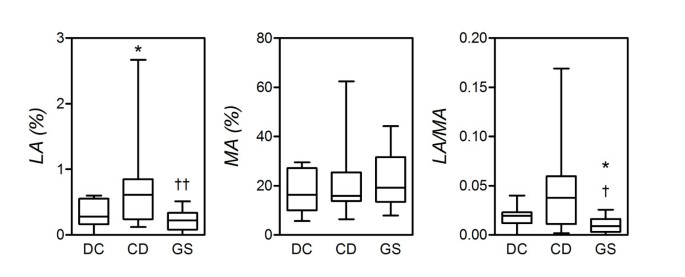
当CD始终与粘膜屏障功能受损和小肠渗透性增加,目前尚不清楚患者GS呈现相似的变化。为了解决这个问题,拉/马尿比确定的三个学习小组。洛杉矶/马比,因此小肠渗透性,在三组之间存在着显著的差异(P= 0.0113;克鲁斯卡尔-沃利斯测试)。特别是在CD患者相比,明显高于GS患者(P= 0.0138;MWU)。类似的差异只CD患者和直流近似意义(P= 0.0950)。有趣的是,拉/马比GS患者也显著降低相对于直流(P=(图0.0308)1)。
图1显示CD患者肠道通透性的增加,相对于直流,归因于一个显著增加尿乳果糖的浓度(P= 0.0400),无明显变化,甘露醇浓度(P= 0.4937;不显著)。自尿乳果糖反映其独家通过paracellular运输通路,而甘露醇是transcellular通路的标志(11),这证实了拉/马比的变化观察到CD反映paracellular渗透性增加。同样,减少拉/马比GS患者相对于CD和直流似乎完全由减少乳果糖浓度,找到了符合流程的参与调节大分子通过paracellular通路。具体来说,尿乳果糖在GS的平均百分比明显低于在CD (P= 0.0049),GS和直流之间差异不显著(P= 0.1817;不显著)。
小肠TJ蛋白的表达
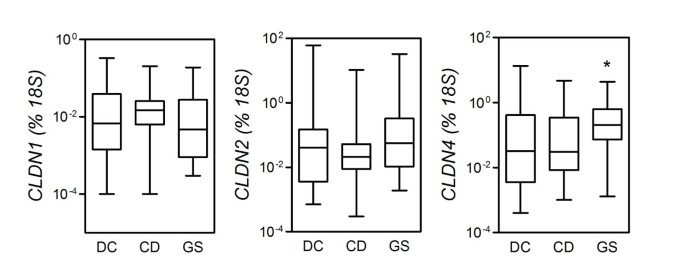
理解是否肠道通透性的变化观察到CD和GS相关编码基因的表达水平改变了关键TJ组件,claudins的表达(CLDN), TJ蛋白(TJP) 1(也称为zonula occludens-1)和occludin (OCLN)决定在肠道组织通过上消化道内窥镜检查。信使rna提取活检标本立即处理,基因的转录水平CLDN1,CLDN2,CLDN3,CLDN4,TJP1和OCLN被qPCR测量。如图2,CLDN4GS的表达明显高于水平比CD (P= 0.0286),而类似的差异与直流几乎达到意义(P= 0.0565)。类似水平的CLDN4从直流和CD(活组织检查中发现P= 0.7279;不显著)。同样,没有观察到显著差异在mRNA水平的三组CLDN1或CLDN2或其他TJ-related基因检查(没有显示)。尽管这可能是由于研究数量有限的情况下,不太可能包含一个更大的样本将弥补高度的可变性和偏态遇到在每个组。
上皮内淋巴细胞
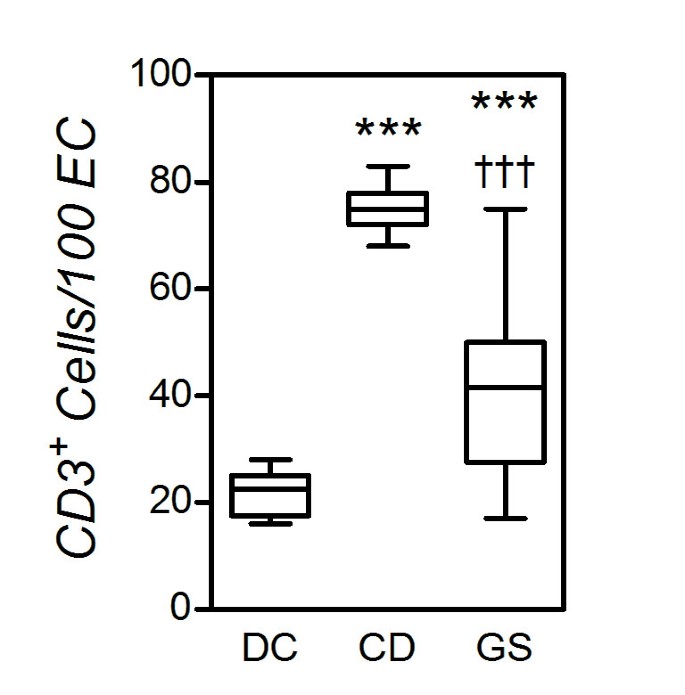
GS病人招募在这项研究中没有出现相关的自身免疫现象和自身免疫血清学(表1)。此外,在这组患者中,我们没有发现明确的协会与主要组织相容性复合体(MHC)单体型,广为记载在CD患者。这些临床研究结果让我们假设自适应免疫系统可能不是一样极度参与GS在CD(或小麦过敏)。为了证实这个观点,我们的终点包括标记的适应性和先天免疫反应小肠粘膜的科目。第一个系列的观测,我们比较IELs GS与CD患者的数量。最近报道了我们组(15轻度发炎),组织学显示正常粘膜(GS沼泽阶段0或1)的病人,尽管所有CD患者显示部分或小结绒毛萎缩地穴增生根据ESPGHAN标准(10]。CD3的免疫组织化学结果总结在图3。CD3的数量+IELs三组之间的差异(P< 0.0001;克鲁斯卡尔-沃利斯测试)。正如预期的那样,CD患者CD3的数量增加+相对于直流IEL (P< 0.0001;MWU)。CD3+IELs无数GS患者明显多于在直流(P所以< 0.0001),但显著低于在CD (P= 0.0012)。不过,值得注意的是,4 GS患者IEL数量高于目前公认的正常范围(≤30/100 EC),建议一个中级,然而pathogenetically重要,参与适应性免疫系统的条件。另一方面,TCRγδIELs一直在CD (> 3.4/100 ECs)升高,而数字GS和直流相似(数据没有显示)。
粘膜适应性immunity-related细胞因子的表达
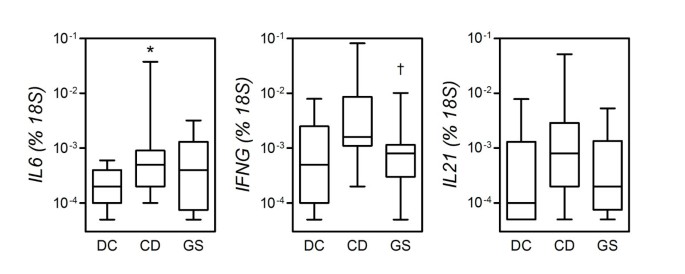
许多研究已经证实,gluten-dependent系统性和粘膜细胞因子的表达与Th1和Th17适应性反应在CD [16- - - - - -19]。我们最近表明,Th17签名细胞因子水平明显高于IL-17A,表达在CD患者的小肠粘膜而不是GS患者(15]。我们还表明,醇溶蛋白诱导循环单核细胞产生Th17-active细胞因子,IL-23,影响由伴随IL-1β和il - 6的表达17,20.]。延长这些观察和进一步定义适应性免疫的作用在GS,信使rna提取小肠活检受到qPCR表达式的多效性的,Th17-activating细胞因子白介素(IL) 6, Th1细胞因子干扰素(干扰素)-γIL-21, Th1细胞因子参与在Th17细胞的分化和维持持续的Th1反应(21]。
如图4、CD病人作为一个整体对il - 6表示更高水平的成绩单(白细胞介素6)IFN-γ(IFNG相对于直流和IL-21 IL21)。然而,由于高度的可变性的CD捐赠者和因为子群的效果已经记录在我们早些时候报告IL-17A [15),只有il - 6表达的差异具有统计学意义(P= 0.0124),而不同的IFNG和IL21转录水平近似意义(P= 0.0700,P分别为= 0.0572)。白细胞介素6的水平,IFNGGS患者标本中,IL21成绩单与直流或CD之间没有显著性差异,除了显著减少IFNG水平相对于CD (P= 0.0222)。IFNG是唯一的细胞因子基因测试显示一个重要程度的变化在三组(P< 0.0428;克鲁斯卡尔-沃利斯测试)。因此,符合Th17细胞分化的作用,il - 6表达在CD粘膜水平显著增加,但不是在GS粘膜。与此同时降低表达IFN-γGS相对于CD支持的概念较低级的参与适应性免疫系统的条件。
小肠toll样受体的表达
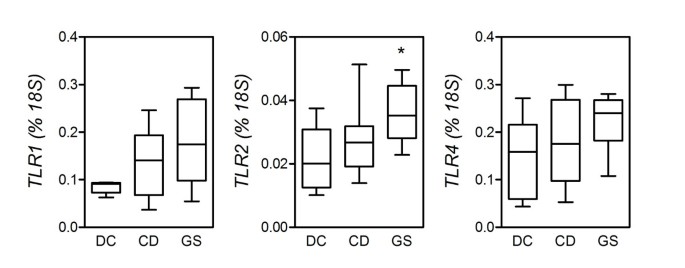
据报道,toll样受体的表达1 (TLR1),TLR2,TLR4增加小肠粘膜的CD患者中,贷款支持了这样一种观点:先天免疫现象可能会先于和/或伴随CD和其他自身免疫性疾病的恶化22- - - - - -24]。初步评估的参与先天免疫在GS,我们比较这些分子的表达在新鲜的活组织检查三个学习小组。如图5,的表达TLR1和TLR2,但不TLR4,信使rna在CD患者高于直流,但是这些差异达到意义。相比之下,相对于直流,GS提出了更高水平的患者TLR2成绩单(P= 0.0295),同时记录级别的TLR1和TLR4在GS高出一般没有达到意义(P= 0.0932,P分别为= 0.1274)。
粘膜监管T-cell-associated基因的表达
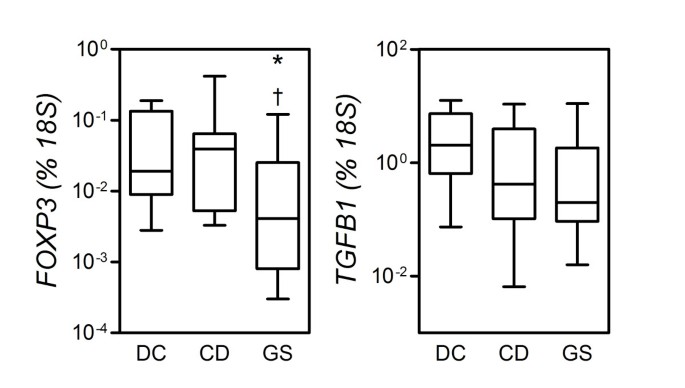
初步评估是否有免疫调节功能的差异也许可以解释微分参与自适应系统的CD和GS的病人,我们测量的mRNA表达两个调节t细胞(Treg)签名分子,forkhead盒factor-βP3 (FOXP3)和转换增长1(TGFB1)小肠活检标本。与先前的报告(25,26),FOXP3的表达水平和TGFB1 CD患者与华盛顿之间没有显著性差异(P= 0.8868,P分别为= 0.1535)。至于TGFB1,似乎有降低的趋势,而不是高水平的表达在CD患者(图6)。这种现象更多的是强调在GS病人,FOXP3的表达和TGFB1, FOXP3显著,减少相对于直流(P= 0.0325,P分别为= 0.0710)。FOXP3减少跨组(GS占一个重要的变化P< 0.0250;克鲁斯卡尔-沃利斯检验)和相对于CD也显著(P= 0.0293),而无显著差异在TGFB1表达GS和CD患者(P= 0.7832)。这些发现,完全相反的初始假设但也许符合先前的报告在CD和其他条件(27,28),可能显示激活水平的降低和/或招聘Treg GS小肠粘膜细胞相对于gluten-tolerant控制。
讨论
CD,自体免疫性肠病,结果从一个不恰当的对麦胶蛋白摄入T-cell-mediated适应性免疫反应。在过去的几年里,它已成为明显的,“经典”CD代表一个整体的冰山一角疾病负担(4,29日]。一个新兴问题是一群gluten-reactive患者的临床特征,约占总人口的10%,呈现症状类似于CD - CD血清学和组织病理学。在CD,这些病人,这里和其他地方被称为GS (15),经历痛苦时吃含谷蛋白制品和显示改进后无谷蛋白饮食。不同于CD, GS发展的不良反应而不遵守饮食蛋白自身抗体的出现和持续损害小肠。GS的症状可能类似的一些胃肠道症状与CD或小麦过敏,但客观的诊断测试这种情况目前下落不明。因此,GS的诊断通常是由排斥。
本身缺乏自身抗体和肠道病变并不排除的固有毒性蛋白,其摄入量,即使在non-CD个体,与损害其他有关组织、器官和系统除了肠(6,30.,31日]。在目前的研究中,我们试图识别功能,形态学和免疫参数来帮助区分GS和CD,初步了解其病理生理学。我们报告在这里第一次微分的证据肠道粘膜反应蛋白在这两个条件。
我们已经表明,一个正常的轻微的组织学GS由守恒的平行的屏障功能。事实上,小肠渗透性测试时拉/马双糖探针,在GS显著低于在CD患者甚至直流。肠道通透性增加被认为是早期的生物变化,预示着一些自身免疫性疾病的发病32- - - - - -34]。损失的肠道屏障功能带来了一个连续的异常通道在肠道上皮细胞抗原。这可能导致从宽容免疫力,因此代表自身免疫性和过敏性疾病的风险增加个人的其他遗传因素,MHC non-MHC,导致不适当的抗原处理和表示。在肠道上皮细胞,paracellular渗透率是由细胞间TJ蛋白。最近表明,CLDNs积分TJ组件关键维护信息粘附在上皮细胞层35- - - - - -37]。CLDN物种的整体平衡表示在一个特定的细胞类型有助于定义TJ的特点。例如,CLDN1和CLDN4提出减少,而CLDN2假设增加TJ-dependent渗透率(35]。符合这个概念,升值GS小肠渗透性降低的患者,我们这里显示GS粘膜表达明显高于水平的成绩单CLDN4相对于CD或直流。相比之下,其他CLDN基因与其他基因与TJ相关函数测量在这项研究似乎并未表示不同的GS或CD粘膜而控制。在一起,这些研究结果表明,不同的临床和血清学特征GS和CD患者之间与粘膜屏障功能和之间的显著区别明显的表达差异CLDN4,这对于一个关键编码TJ组件(38]。还需要进一步的研究来比较这个和其他的分布和组装TJ蛋白在这些条件。
GS患者并发症并不存在显著的自身免疫或过敏,,我们这里也有,常见的自身抗体的血清学,包括anti-tTG IgA、是负的。有趣的是,AGA IgA和免疫球蛋白在大约50%的情况下是积极的。同样,aga的滴度高于预期,与non-CD谷蛋白敏感性相关的症状和体征,也有精神分裂症(39和自闭症谱系障碍40]。在CD有很强的遗传协会二类MHC单体型,约有95%的患者hla dq2,剩下的5%hla dq8,我们已经表明,只有50%的患者GS携带hla dq2和/或hla dq8,这一比例略高于普通人群。这表明减少MHC-dependent适应性免疫反应参与g水平相对于CD。我们有进一步表明,GS粘膜包含增加CD3的数字+IELs,尽管这些数字明显低于那些活跃CD患者中相对守恒的绒毛状结构,对应0和1的湿地分类阶段。这是符合一个更有限的参与适应性免疫系统的GS和也许可以解释为什么这个条件不是伴随着显著的自身免疫现象。
在CD,适应性反应已被证明是由tTG-deamidated面筋肽DQ2或DQ8。这包括粘膜招聘和激活Th1 Th17克隆和Th1和Th17-associated细胞因子的生产,也就是说,IFN-γIL-17A,导致扰乱屏障功能和发起组织损伤(16,18- - - - - -21,41]。在早前的报告中,我们发现IL-17A转录表达水平明显高于在小肠粘膜至少CD患者的一组中,但不是在GS患者(15]。在这项研究中,我们已经延长这一发现表明,Th1细胞因子签名,IFN-γ,也是表达显著降低水平GS和CD粘膜。此外,在CD但不是在GS,我们观察到显著增强的il - 6的表达,是已知的多效细胞因子促进Th17细胞的分化和功能,以及一个类似的趋势在IL-21的表达,建立符合其作用的病理生理学Th1和Th17细胞。
这些发现可能表明,g是一种主要由先天免疫炎症状态机制。其中,通常代表一个家庭的进化保存通过模式识别受体能够检测微生物入侵,调解快速炎症反应可能会或可能不会发展成一个antigen-dependent适应性反应。通常表达的不同组合等造血细胞和nonhematopoietic细胞肠上皮细胞(42- - - - - -44]。在这项研究中,我们发现,小肠的表达TLR2和一定程度上的TLR1但不是TLR4在GS病人增加。在缺乏适应性免疫标记,正如我们所看到的,这表明了普遍作用先天免疫系统的GS的发病机理。
综上所述,这些研究结果支持这样的设想,即先天和适应性免疫途径的普遍参与可能有助于解释GS和CD患者的临床和血清学的差异。Treg细胞功能的降低,特别是“自适应”Treg细胞,提出了考虑到失去免疫内稳态和自身免疫反应的发展CD和相关条件(26]。它可能推断,Treg可以有效地防止发展为GS患者的这种反应。的显著降低粘膜表达独特的Treg标记,FOXP3,欣赏在GS病人在这项研究中,因此令人惊讶的和违反直觉的这些注意事项。然而,至少令人惊讶的是,在几项研究FOXP3和其他Treg-expressed分子,如TGFB1,已发现调节患者的外周血和肠道粘膜CD和相关条件,例如,1型糖尿病(28,45]。类似的结果也出现在其他条件与适应性免疫的广泛参与,如过敏和哮喘,导致猜测代偿扩张和/或动员Treg可能发生与适应性的累积效应响应(46]。自相矛盾的是,如果这种假设是真的,GS的Treg标记表达降低可能的上下文中被普遍降低激活适应性免疫相对于CD。而显然还需要更多的研究来阐明这个问题,更好地理解Treg函数在CD和相关条件将有助于描述的可能致病的作用减少Treg激活在GS和/或招聘。
结论
这项研究的结果表明,CD和GS不同的临床实体不同引起的肠道粘膜反应蛋白。CD结果复杂,还待定,相互作用的肠道通透性增加,粘膜损伤,环境因素除谷蛋白,和遗传易感性,包括MHC和non-MHC基因。典型的肠道病变CD被认为是由先天和适应性免疫效应的途径。我们的研究结果表明,以不同的方式,GS与普遍的激活先天免疫反应。虽然机制负责肠道屏障功能的丧失在CD划定部分负责的损失的因素面筋宽容和自身免疫的发展在这种情况下还不完全理解。我们相信,这项研究可能有助于GS条件的临床特征与普遍gluten-induced激活先天免疫在没有检测到粘膜屏障功能的变化,而且它提供了额外的线索的定义复杂的gluten-induced TJ的变化调节和免疫过程潜在的CD发病机理。双盲,安慰剂对照的研究是必要的定义,进一步巩固GS病人和搜索特定的生物标记一个适当的诊断。
缩写
- 将军:
-
anti-gliadin抗体
- CD:
-
乳糜泻
- CLDN:
-
claudin
- DC:
-
消化不良的控制
- 电子商务:
-
肠上皮细胞
- 教育津贴:
-
肌内膜抗体
- 具体:
-
P3 forkhead框
- g:
-
谷蛋白敏感性
- IEL:
-
上皮内淋巴细胞
- 干扰素:
-
干扰素
- IL:
-
白介素
- 拉:
-
乳果糖
- 马:
-
甘露醇
- MHC:
-
主要组织相容性复合体
- OCLN:
-
阻塞
- 聚合酶链反应:
-
聚合酶链反应
- TGF:
-
转化生长因子
- Th:
-
辅助T
- TJ:
-
紧密连接
- TLR:
-
toll样受体
- Treg:
-
调节t细胞
- 测试:
-
组织转谷氨酰胺酶。
引用
田边年代:分析食品过敏原结构和发展食品过敏的病人。学生物化学生物科技Biosci》。2008年,72:649 - 659。10.1271 / bbb.70708。
安德森,麦克米兰SA沃森RG,莫纳亨P,加文,福克斯C,穆雷LJ:恶性肿瘤和死亡率的人口基数的腹腔疾病患者或“谷蛋白敏感性”。世界杂志。2007年,13:146 - 151。
Brandtzaeg P, Halstensen TS,凯特K, Krajci P, Kvale D, Rognum,斯科特•H Sollid LM:人类肠道粘膜的免疫生物学和免疫病理:体液免疫和上皮内淋巴细胞。胃肠病学。1989年,97:1562 - 1584。
Catassi C,乳糜泻法:。当今杂志。2008,24:687 - 691。10.1097 / MOG.0b013e32830edc1e。
Hoffenberg EJ, MacKenzie T, Barriga KJ, Eisenbarth GS、包F,哈斯我,Erlich设计H, Bugawan TT,索科尔RJ,塔基•我,诺里斯JM, Rewers M:前瞻性研究的儿童腹腔疾病的发病率。J Pediatr。2003年,143:308 - 314。10.1067 / s0022 - 3476 (03) 00282 - 8。
Dolfini E, Roncoroni L,埃利- L, Fumagalli C,科伦坡R, Ramponi年代,馥兰妮F•巴尔MT:细胞骨架重组和超微结构的损伤引起的醇溶蛋白在三维体外模型。世界杂志。2005年,11:7597 - 7601。
Di皮耶罗德拉戈年代,El Asmar R, M,克莱门特MG,特里帕西,Sapone, Thakar M, Iacono G,阉,D 'Agate C T, Zampini L, Catassi C法:醇溶蛋白,zonulin和肠道通透性:影响腹腔non-celiac肠道粘膜和肠细胞系。Scand杂志。2006年,41:408 - 419。10.1080 / 00365520500235334。
弗雷泽JS,恩格尔W,埃利斯HJ,穆迪SJ, EL,波洛克维塞尔H Ciclitira PJ:腹腔疾病:体内毒性的假定的immunodominant抗原决定基。肠道。2003年,52:1698 - 1702。10.1136 / gut.52.12.1698。
白痴B,白求恩MT, Comino我Manyani H, Ferragud M,洛佩兹MC, Cebolla,科斯拉C,苏萨C:对食物中毒乳糜泻患者的评估:单克隆抗体的鉴定主要免疫原性蛋白肽。《公共科学图书馆•综合》。2008年,3:e2294 - 10.1371 / journal.pone.0002294。
Troncone R,博年代,Butzner D,卡梅伦D,希尔,Hoffenberg E, Maki M,门德斯V·德·希门尼斯MZ:乳糜泻和其他胃肠道免疫介导的疾病:工作组的报告第二次世界儿科胃肠病学大会肝脏病学和营养。39 J Pediatr杂志减轻。2004年,17 (2):S601-S610。
Generoso M·德·罗莎M, De罗莎R,独立L, Secondulfo M, Fiandra R, Carratu R, Carteni M:纤维二糖和乳果糖加上甘露醇和决定使用离子交换色谱法和脉冲测量电流的检测,是可靠的调查调查的肠道通透性。J Chromatogr B分析化学抛光工艺生物医学生命科学。2003年,783:349 - 357。10.1016 / s1570 - 0232 (02) 00766 - 3。
绿色的PH值,Rostami K,沼泽。内格罗蓬特:腹腔疾病的诊断。最好的Pract Res反应。2005年,19:389 - 400。10.1016 / j.bpg.2005.02.006。
沼泽。内格罗蓬特:谷蛋白敏感性的自然历史:定义、炼油和求变。QJM。1995、88:卖地。
Mazzarella G, Maglio M, Paparo F, G, Nardone Stefanile R, L·格列柯,van de Wal Y, Kooy Y,今敏F, Auricchio年代,Troncone R: immunodominant DQ8限制麦胶蛋白肽激活小肠免疫反应在体外培养的粘膜hla DQ8积极但不hla DQ8消极腹腔患者。肠道。2003年,52:57 - 62。10.1136 / gut.52.1.57。
Sapone,拉默斯公里,Mazzarella G, Mikhailenko我Carteni M, Casolaro V法:微分粘膜IL-17表达两个gliadin-induced障碍:谷蛋白敏感性和自身免疫性乳糜泻肠下垂。Int拱过敏Immunol。2009年,152:75 - 80。10.1159 / 000260087。
Castellanos-Rubio, Santin我Irastorza我Castano L,卡洛斯VJ,雷蒙奉:TH17 (TH1)签名的CD患者的肠活检对麦胶蛋白的反应。自身免疫。2009年,42:69 - 73。10.1080 / 08916930802350789。
哈里斯公里,法曼DL:前沿:il - 1控制IL-23响应由麦胶蛋白,腹腔疾病的病原体。J Immunol。2008年,181:4457 - 4460。
Monteleone我Pallone F Monteleone G: Interleukin-23 Th17细胞控制的肠道炎症。介质Inflamm。2009年,2009:297645 - 10.1155 - / - 2009/297645。
Monteleone我Sarra M,德尔维奇奥BG, Paoluzi OA, Franze E,国际泳联D, Fabrizi,麦克唐纳TT, Pallone F, Monteleone G: IL-17A-producing乳糜泻粘膜细胞的特征。J Immunol。2010年,184:2211 - 2218。10.4049 / jimmunol.0901919。
日元D,张J, scheeren H F波利特,麦克拉纳罕T,麦肯齐B, Kleinschek妈,欧阳,马特森J,布鲁门夏恩W,墨菲E,萨瑟M, Cua DJ, Kastelein RA, Rennick D: IL-23是必不可少的T细胞介导结肠炎和促进炎症通过IL-17和il - 6。中国投资。2006年,116:1310 - 1316。10.1172 / JCI21404。
斯坦曼L: T的简史H17日,第一次重大修改的TH1 / TH2假设T细胞介导的组织损伤。Nat地中海。2007年,13:139 - 145。10.1038 / nm1551。
Szebeni B, G版本,Dezsofi Rusai K, Vannay, Bokodi G, Vasarhelyi B, Korponay-Szabo IR, Tulassay T, Arato:增加粘膜toll样受体(TLR) 2和TLR4的表达在腹腔疾病。J Pediatr杂志减轻。2007年,45:187 - 193。10.1097 / MPG.0b013e318064514a。
托马斯•柯Sapone,法,傅高义SN:醇溶蛋白刺激小鼠巨噬细胞炎症基因表达和肠道渗透性MyD88-dependent:乳糜泻的先天免疫反应的作用。J Immunol。2006年,176:2512 - 2521。
Zanoni G, Navone R, Lunardi C, Tridente G, Bason C,施华尼年代,Beri R, Dolcino M,瓦莱塔E, Corrocher R, Puccetti答:在腹腔疾病,自身抗体与转谷氨酰胺酶结合的一个子集toll样受体4和诱导激活单核细胞。科学硕士。2006年,3:e358 - 10.1371 / journal.pmed.0030358。
绞死JA, Arranz E, Gomez-Gonzalez E, Leon AJ Farre C,卡尔沃C, D Bernardo, Fernandez-Salazar L, Blanco-Quiros答:白细胞介素6,IL10和TGFB1基因多态性在腹腔疾病:DQ2正面和负面的患者之间的差别。Allergol Immunopathol (Madr)。2005年,33:245 - 249。10.1157 / 13080926。
Granzotto M,木豆Bo年代,Quaglia年代,托马西尼,Piscianz E, Valencic E, F费拉拉,Martelossi年代,文图拉,不是T:乳糜泻监管T细胞功能受损。挖说科学。2009年,54:1513 - 1519。10.1007 / s10620 - 008 - 0501 - x。
Forsberg G, Hernell啊,假期,Israelsson, Hammarstrom年代,Hammarstrom ML:矛盾coexpression down-regulatory和促炎细胞因子在儿童乳糜泻的肠道T细胞。胃肠病学。2002年,123:667 - 678。10.1053 / gast.2002.35355。
Vorobjova T, Uibo O, Heilman K, Rago T, Honkanen J, Vaarala O, Tillmann V, Ojakivi我Uibo R:增加FOXP3小肠粘膜的表达与腹腔疾病的儿童和I型糖尿病。Scand杂志。2009年,44:422 - 430。10.1080 / 00365520802624177。
弗格森,吉列H,汉弗莱斯K,金石凯西:乳糜泻的异质性:临床、病理、免疫、遗传。安N Y科学。1998年,859:112 - 120。10.1111 / j.1749-6632.1998.tb11115.x。
Hadjivassiliou M,桑德斯DS, Grunewald RA, Woodroofe N, Boscolo年代,Aeschlimann D:谷蛋白敏感性:从直觉到大脑。柳叶刀神经。2010年,9:318 - 330。10.1016 / s1474 - 4422 (09) 70290 - x。
一直对EF,阿姆斯特朗D,穆雷JA:乳糜泻和肠易激综合症之间:谷蛋白敏感性的“无人区”。杂志。2009年,104:1587 - 1594。10.1038 / ajg.2009.188。
实习MC, Bistritz L Meddings简森-巴顿:在肠道通透性改变。肠道。2006年,55岁:1512 - 1520。10.1136 / gut.2005.085373。
法,Shea-Donohue T:疾病的机制:肠道屏障功能的作用在胃肠道自身免疫性疾病的发病机制。Nat中国Pract杂志。2005年,2:416 - 422。10.1038 / ncpgasthep0259。
Bjarnason我,彼得斯TJ,李维AJ:肠道通透性:临床相关。挖说。1986年,4:83 - 92。10.1159 / 000171140。
Furuse M, Fujita K, Hiiragi T,藤本K, Tsukita S: Claudin-1和2:小说整体膜蛋白本地化与没有序列相似性occludin紧密连接。J细胞杂志。1998,141:1539 - 1550。10.1083 / jcb.141.7.1539。
休伊特KJ, Agarwal R,莫林PJ: claudin基因家族:表达在正常和肿瘤组织。BMC癌症。2006年,6:186 - 10.1186/1471 - 2407 - 6 - 186。
小杰,马达腊镇Pappenheimer:结构性基础生理调节paracellular通路在肠道上皮细胞。J会员。1987年,100:149 - 164。10.1007 / BF02209147。
范Itallie C, Rahner C,安德森JM:规范的表达claudin-4减少paracellular电导通过选择性降低钠渗透性。中国投资。2001年,107:1319 - 1327。10.1172 / JCI12464。
Cascella NG Kryszak D,巴蒂B,格雷戈里·P,凯莉DL, Mc Evoy JP,法,伊顿WW:腹腔疾病患病率和面筋敏感性在美国临床抗精神病药物试验的干预效果研究。Schizophr公牛。2011年,37:94 - 100。10.1093 / schbul / sbp055。
独立L, Familiari V, Pascotto Sapone, Frolli, Iardino P, Carteni M·德·罗莎M, Francavilla R,格尔G, Militerni R, Bravaccio C:肠道屏障的改变在孤独症谱系障碍患者和他们的直系亲属。J Pediatr杂志减轻。2010年,51:418 - 424。10.1097 / MPG.0b013e3181dcc4a5。
韦弗CT,哈顿RD,摩根公关,哈林顿LE: IL-17家族细胞因子和效应T细胞谱系的扩大多样性。为Immunol。2007年,25岁:821 - 852。10.1146 / annurev.immunol.25.022106.141557。
彰,Hemmi H:承认其为分子TLR家族模式。Immunol。2003年,85:85 - 95。10.1016 / s0165 - 2478 (02) 00228 - 6。
Medzhitov R, Janeway CA:解码模式自我和异物的先天免疫系统。科学。2002年,296:298 - 300。10.1126 / science.1068883。
井JM, Loonen LM, Karczewski JM:天生的角色内稳态信号的宽容和肠道免疫。Int J地中海Microbiol。2010年,300:41-48。10.1016 / j.ijmm.2009.08.008。
汉森T, Ulfgren AK, Lindroos E, DannÆus, Dahlbom我Klareskog L:转变增长factor-β(TGF-β)和小肠组织转谷氨酰胺酶的表达在腹腔疾病的孩子。56 Scand J Immunol。2002: 530 - 537。10.1046 / j.1365-3083.2002.01157.x。
冷藏AJ, Satinover SM Solga医学博士Lannigan是的,阮JT,威尔逊BB, Woodfolk JA: CD25的分析嗨CD4+“监管”T细胞亚型特异反应性皮炎揭示小说TH2人口。J过敏Immunol。2008, 121: 415 - 422。10.1016 / j.jaci.2007.11.003。e3
出版前的历史
这篇论文的出版历史可以访问:http://www.biomedcentral.com/1741-7015/9/23/prepub
确认
作者感谢d Siniscalco博士,p . Pezzella博士答:Papparella博士和m .曼卓林先生给予技术帮助和无条件的鼓励。这些研究部分由国立卫生研究院授予R21DK078699房颤和吉安达Regionale坎帕尼亚Assessorato真主安拉Ricerca Scientifica L.R. 5 28/03/2002 MC。
作者信息
作者和联系
相应的作者
额外的信息
相互竞争的利益
房颤是股东ALBA疗法(巴尔的摩,医学博士,美国)。MTG KML, VC, MC,医学博士,RS,通用,CT,美联社,米尔,PE、FF, MC, GR和LDM没有利益冲突声明。
作者的贡献
,通用和房颤研究构想。房颤支持这项研究。MTG KML, VC,通用汽车、MC, LDM和房颤导致设计研究。和KL进行大部分的分子遗传学研究。MC toll样受体通路的分子分析。医学CT和GR参与序列比对研究。RS和FF进行免疫组织化学分析;米尔和体育参与招聘的病人和内镜程序进行。KML, VC和房颤参与数据的分析和解释。KML, VC,通用和房颤起草了手稿。 AS, KML, VC, MD, CT, MC, GR, LDM and AF critically revised the manuscript. All authors gave their final approval of the version of the manuscript to be published.
作者提交的原始图像文件
权利和权限
开放获取这篇文章发表在生物医学中心有限公司的许可证。这是一个开放的文章是分布式知识共享归属许可的条款(https://creativecommons.org/licenses/by/2.0),允许无限制的使用、分配和复制在任何媒介,提供最初的工作是正确引用。
关于这篇文章
引用这篇文章
Sapone,。,Lammers, K.M., Casolaro, V.et al。肠道通透性的散度和粘膜免疫基因表达在两gluten-associated条件:乳糜泻和面筋敏感性。BMC医学9,23 (2011)。https://doi.org/10.1186/1741 - 7015 - 9 - 23所示
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/1741 - 7015 - 9 - 23所示
关键字
- 乳糜泻
- 肠道通透性
- 紧密连接蛋白
- 乳糜泻病人
- 肠道屏障功能

评论
查看存档的评论(1)