条文本
摘要
肠道菌群现在被认为是有助于调节宿主健康的关键因素之一。事实上,我们身体的所有部位都被微生物占据,这表明我们的器官之间存在着不同类型的相互作用。由于分子工具和技术(即宏基因组学、代谢组学、脂质组学、元转录组学)的发展,宿主和不同微生物之间发生的复杂相互作用正在逐步被破译。如今,肠道菌群偏差与许多疾病有关,包括肥胖、2型糖尿病、肝脂肪变性、肠道疾病(IBDs)和几种癌症。因此,这表明涉及免疫、能量、脂质和糖代谢的各种途径都受到了影响。
在这一审查中,特别注意对这一领域目前的认识进行批判性评价。许多分子机制解释了肠道细菌可能与疾病的保护或发病的因果联系。我们检查了已知的代谢物(即短链脂肪酸、胆油酸、三甲胺n-氧化物),并将其扩展到最近发现的分子作用体(即内源性大麻素、生物活性脂类、酚衍生化合物、晚期糖基化终末产物和肠合成酶)及其特定受体,如过氧化物酶体增殖物激活受体α (PPARα)和γ (PPARγ)、芳基烃受体(AhR)和G蛋白偶联受体(如GPR41、GPR43、GPR119、武田G蛋白偶联受体5)。
总之,了解肠道微生物与健康之间的复杂性和分子方面的联系,将有助于为正在开发的新疗法奠定基础。
- 肠道微生物
- 肥胖
- 肠道屏障功能
- 肝
- 益生菌
这是一篇开放获取的文章,按照创作共用署名4.0未移植(CC BY 4.0)许可发布,该许可允许其他人复制、重新发布、混合、转换和基于此作品的任何目的,只要原始作品被正确引用,提供许可证链接,并说明是否进行了更改。看到的:https://creativecommons.org/licenses/by/4.0/.
来自Altmetric.com的统计
人类肠道微生物群
在这里,人类微生物组被认为是微生物的集合,它们的基因和产物自出生以来就定居在我们的身体,并垂直转移。1 2虽然所有的身体部位都是殖民化的(图1)中,被广泛研究的微生物数量最多的是肠道。3.在这里,我们回顾了肠道微生物、它们的活动和中介分子对我们健康的贡献的方式的主要和最新的发现。

根据身体不同部位的细菌丰度。不同器官中细菌数量的界限,由细菌浓度和体积得出。190 191
在健康的受试者中,口腔和唾液微生物群包含数百万种我们每天随食物吞下的微生物,但它们在肠道中的持久性受到许多因素的阻碍,包括胃的酸度、胆汁酸(BAs)的产生、消化酶和十二指肠及其他部位的抗菌蛋白。许多其他主要变量影响下游微生物的定植,如pH值、氧浓度和氧化还原电位等化学参数、粘液、胆汁和抗体的生物生成,以及包括肠道结构、蠕动和转运时间(图1).因此,沿着小肠发现了微生物的浓度梯度,因为十二指肠吸出物中的微生物丰度比口腔样本低1000倍,尽管组成的微生物类群有点相似。4因此,小肠每克内容物含有数以千计到数亿个细胞,其中部分耐氧厚壁菌门和变形菌门为主要门。5个6这一切都在下肠达到了顶峰,每克多达1000亿个细胞的高潮群落在那里停留了几天,因为在结肠中的转运比在小肠中的转运要长十几倍。因此,结肠微生物群主要由厌氧菌组成,包括数千种和数百万个基因,分布在厚壁菌门(主要是瘤胃球菌科和拉克诺螺旋菌科)、拟杆菌门、放线菌门、变形菌门和疣菌门(Akkermansia)7 - 10(图1).通过粪便排出的这种生物量构成了通常被称为肠道微生物组的东西,它与许多疾病有关,并可通过饮食和药物高度改变(表1).它为粪便菌群移植(FMT)提供了起始材料,该移植已被证明可以治愈复发性腹泻患者Clostridioides固执的感染和其他疾病。11 - 15号
值得注意的是,我们可以没有结肠,但不能没有小肠。小肠是我们身体最大的粘膜表面,在那里我们的食物被进一步消化和吸收,包含大多数肠道受体、免疫细胞和神经细胞,并越来越多地包含在必要的微生物-宿主交叉对话中。虽然很难从实验上接近,但近年来发展出了各种各样的新技术,包括用于取样、递送或检查的导管或胶囊。16日至18日此外,对回肠造口术获得的小肠流出物进行了研究,发现每克湿重含有多达1亿个微生物,形成了个性化的群落,显示出反映食物摄入和加工过程的昼夜节律。19这些样本的功能(转录组学和靶向代谢组学)和宏基因组学分析显示了定植链球菌和乳酸菌SPP表达大量的高效运输系统,与宿主竞争糖的吸收和利用,产生乳酸和醋酸盐,这是基质韦永氏球菌属SPP和转化为丙酸。20.最近使用特殊研制的导管的研究证实了这些群落,并揭示了十二指肠菌群与pH值相关的组成动态高于空肠,空肠是表面最大的肠间隔,负责大部分糖、蛋白质和脂类的消化和吸收。5 21虽然在十二指肠和空肠之间有一个连续体,但更近端的回肠有一个大黏液层,使人联想到结肠,并有一些厌氧菌定植,包括肠的成员Bacteroidia,Ruminococcaceae和Lachnospiraceae,其中一些也包含在BAs转化中(见生物活性脂类/胆汁酸部分)。21日22
十二指肠及其微生物已成为多种代谢和可能的免疫疾病的主要因素。23对这一点的支持和进一步的新见解来自于十二指肠递送FMT,它缓解了代谢综合征或自身免疫疾病的症状。24 - 26日此外,活的或死的十二指肠灌注乳酸菌SPP已被发现影响宿主的免疫反应,为人类发现提供了一个实验系统。-这最近被用来分析单十二指肠剂量的Anaerobutyricum soehngenii(以前称为真细菌hallii)30.使十二指肠中再生胰岛蛋白1B的基因表达水平增加了近10倍,也增加了代谢综合征受试者的血清胰高血糖素样肽-1 (GLP-1)和次生胆盐的表达,从而可能解释了它们对葡萄糖反应的改善。31日32
尽管在肠道中存在明显的垂直梯度,但在结肠中也存在水平梯度,而且研究最为广泛。重要的是,存在氧气、氧化还原和粘液梯度,从粘膜表面开始延伸到管腔,形成了微生物群落的结构。33一般来说,这些开始于黏液降解菌群,通常以黏液降解菌群和微嗜氧菌群为主Akkermansia muciniphila最后是完全厌氧的群落,包括产生丁酸盐和丙酸盐的瘤胃球菌科,拉克诺螺旋菌科和Bacteroidia以及将氢和二氧化碳分别转化为醋酸酯或甲烷的同生乙酰菌和产甲烷菌。
肠道微生物群和各种肠道及肠外疾病
肠道微生物群与几种肠道和肠外疾病有关。34许多针对肠道菌群及其相关性的大型研究已经在特定的胃肠道疾病(GI)中进行,如肠道疾病(IBDs)、35腹腔疾病,36肠易激综合症,37结直肠癌(CRC),38慢性肝脏疾病39 40或胰腺疾病。41 42ibd是肠道的典型炎症性疾病,与偏离肠道微生物组组成有关,确实有报道过兼性厌氧菌的生长,特别是在活性炎症和代谢物紊乱的情况下,包括BAs、短链脂肪酸(SCFAs)和酰基肉碱途径。35对有乳糜泻(另一种常见的炎症性肠道疾病)风险的婴儿的纵向分析显示,几种微生物种类的存在增加,如Dialister invisus, Parabacteroides和某些代谢物,如色氨酸代谢物,而各种抗炎菌株,如Faecalibacterium prausnitzii或clostridioforme梭状芽胞杆菌被降低了。36肠易激综合征是一种常见的胃肠道功能障碍,与肠易激综合征亚型特异性的肠道微生物群和相关代谢物改变有关,其中嘌呤代谢尤其受影响。37结直肠癌是下肠最常见的恶性肿瘤,已经令人信服地与肠道微生物群紊乱相关,并涉及某些细菌,如核梭杆菌,大肠杆菌或脆弱拟杆菌,其中一些来自口腔微生物群。38慢性肝病,特别是像肝硬化这样的晚期肝病,其特征是严重的微生物畸变,而益生元、益生菌和抗生素的介入研究数据已经证实,肠道微生物群在这些疾病中起着关键作用。40胰腺癌,在西方世界越来越被承认的恶性肿瘤,也被认为与肠道微生物组受损有关,因为肿瘤内微生物组组成影响宿主免疫反应和疾病的自然史。42
在过去的几年里,肠道微生物群在肥胖和肥胖相关疾病(如2型糖尿病(T2D)和非酒精性脂肪肝(NAFLD))中被广泛研究。许多研究试图将改变的肠道微生物群与肥胖联系起来,事实上,一些介入研究也涉及某些细菌菌株,如Akkermansia muciniphila对肥胖相关参数有影响。43在亚洲和欧洲人群中,T2D的特征还包括肠道微生物群受损。44 45在T2D中,微生物变异与胰岛素抵抗的存在密切相关,一些研究表明肠道微生物组影响葡萄糖调节。46NAFLD是目前西方世界最常见的慢性肝病,被认为是一种典型的代谢障碍,介于肥胖、代谢综合征和T2D之间。越来越多的证据表明,肠道微生物-肝脏轴在NAFLD中发挥作用,特别是在纤维化和向更晚期疾病进展的情况下,如非酒精性肝脂肪变性。47目前已有几项研究表明,NAFLD的特征是某些肠杆菌科细菌大量繁殖、大肠杆菌减少了f . prausnitzii.最近的数据还表明,在NAFLD中,微生物组的偏差和不稳定可能存在多年,甚至可能先于NAFLD和T2D的发展。48有越来越多的胃肠道和代谢疾病的肠道菌群已被调查(见表1概述)。
肠道微生物和代谢紊乱:分子因素
肠道细菌群落在代谢紊乱的多个方面起着重要的调节作用。除其他外,这种调节取决于微生物群产生各种各样的代谢物,以及它们与宿主细胞上的受体的相互作用,这些受体可以激活或抑制信号通路,对宿主健康有益或有害(图2).

肠道菌群根据营养物质或代谢源及其衍生化合物产生的分子和代谢物。BSCFA支SCFA;有限合伙人,脂多糖;PAMPs,病原体相关分子模式;短链脂肪酸。
参与这些相互作用的细菌代谢物是非常多样的,从小分子到大分子都有。它们包括细菌代谢的副产物,如SCFAs,以及维持细菌完整性所必需的复杂大分子,如肽聚糖和脂多糖(LPS) (图2).
这些代谢物的丰度和有效性取决于微生物的组成,因此受饮食和环境因素的调节。49-51下面讨论主要的分子作用体。
短链脂肪酸及其对宿主健康的影响:分子机制
小肠高度专门分解、乳化和吸收营养物质,很少有营养物质会逃过消化系统。例如,在正常情况下,每天不到5克的脂肪会到达结肠。同样的原理也适用于简单碳水化合物(分解为糖分子)和大多数蛋白质(转化为氨基酸)的消化和吸收,尽管,根据摄入量的不同,有些蛋白质会到达结肠。相反,复杂的碳水化合物,如膳食纤维是不可消化的,这意味着身体缺乏必要的酶来消化它们,使它们在小肠中逃脱消化。然而,在结肠中,它们可以被特定的驻留细菌用作能量来源。各种肠道微生物将这些不可消化的碳水化合物代谢成不同的SCFAs分子(如醋酸盐、丁酸盐和丙酸盐)。短链脂肪酸的化学特征很好,其对健康的影响已经有大量文献记载。52-54这些化合物在肠道和肝脏、脂肪组织、肌肉和大脑等远处调节许多代谢途径。图3).55-57如今,这些微生物代谢物被认为有助于许多生理效应,从调节能量稳态,葡萄糖/脂质代谢,炎症,甚至免疫和癌症。52
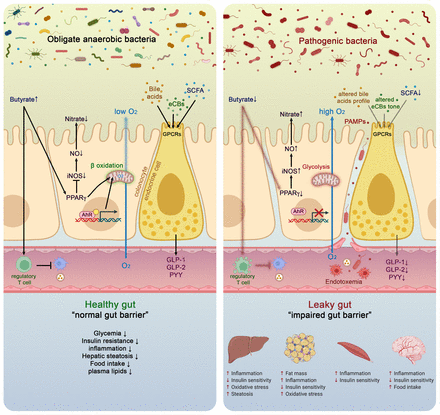
健康和病理状态下肠道菌群与宿主健康的分子机制。在正常情况下,结肠细胞通过线粒体中的-氧化以丁酸盐为能量底物,从而消耗氧气,直接有助于维持腔内的无氧状态。丁酸盐还与过氧化物酶体增殖物激活受体γ (PPARγ)结合,进而抑制诱导型一氧化氮合酶(iNOS),减少一氧化氮的产生(NO),最终减少硝酸盐的产生。相反,在病理情况下,腔内丁酸含量低与PPARγ活性降低、糖酵解增加和耗氧量降低相关。这与iNOS的高表达有关,iNOS反过来产生更多的NO,并最终增加特定病原体的硝酸盐可用性。丁酸盐还可以刺激调节性T细胞(Treg)等免疫细胞,减少炎症。核转录因子芳基烃受体(AhR)在健康结肠细胞中高度表达和激活,而AhR激动剂活性降低或降低可导致肠道屏障功能改变。肠内分泌细胞(l -细胞)表达由短链脂肪酸(SCFAs)、特异性内源性大麻素(eCBs)和胆汁酸(BAs)激活的几种关键受体。激活这些受体会增加关键肠道肽的分泌,如胰高血糖素样肽(GLP)-1、GLP-2和肽YY (PYY)。总之,肠道微生物和这些分子作用体之间的相互作用有助于降低肠道通透性,改善胰岛素分泌和胰岛素敏感性,减少食物摄入,降低血脂,避免肝脏脂肪变性和代谢性内毒素血症。 All these effects are associated with lower inflammation. Conversely, opposite effects have been observed in pathological situations.
通过一系列的实验研究,人们发现了富含可发酵膳食纤维(如益生元)的饮食能够减少体重增加、脂肪块形成、胰岛素抵抗和能量摄入的许多分子机制。58 - 62其中,研究发现,使用益生元调节肠道菌群可导致l细胞产生的几种肠道肽如GLP-1、GLP-2和肽YY (PYY)的内源性生产(即mRNA和肽)和门静脉分泌增加(图3).59 - 61 63 - 65
这些影响不仅仅局限于一种可发酵碳水化合物,因为微生物将抗性淀粉或阿拉伯木聚糖发酵为SCFAs会产生与血浆GLP-1和PYY水平升高相关的类似生理效应。66 - 69然而,可发酵纤维的化学结构与短链脂肪酸的生产情况直接相关,因为生成的丁酸、乙酸或丙酸的数量将取决于纤维的类型。例如,菊粉被描述为丙酸原性,而抗性淀粉则更多是丁酸原性。值得注意的是,一些结肠细菌也使用其他途径从氨基酸如赖氨酸或从植物化合物如植酸盐中产生丁酸盐。70 71值得注意的是,短链脂肪酸的来源来自于饮食,它们可以通过覆盖在肠上皮细胞上的肠粘液的发酵来自宿主本身。72
SCFAs通过作用于肠内分泌l细胞表面表达的特定g蛋白偶联受体来刺激肠肽的分泌,这些细胞在回肠末端和结肠中特别丰富。这些受体被命名为G蛋白偶联受体(GPR)43(或自由脂肪酸受体2 (FFAR2))和GPR41(或FFAR3) (图4),73也在多种组织和细胞类型中表达(如脂肪细胞、免疫细胞)。74 - 76通过使用缺乏GPR43或GPR41的小鼠模型,已经阐明了微生物组在肠道肽分泌中的关键作用。缺乏这些受体的小鼠暴露于SCFAs或特定的益生元后,GLP-1和PYY的分泌减少(图3).77 - 79
结肠细胞和内分泌细胞表达多种受体,能够感知和传输来自微生物环境的信号。微生物/病原体相关分子模式(PAMPs)、来自微生物群的脂多糖(LPS)被模式识别受体检测,包括toll样受体(TLRs)。Amuc_1100是一种表达于细胞膜外的蛋白Akkermansia muciniphila它被证明可以通过TLR2发出信号,改善肠道屏障功能,减少炎症。某些微生物分泌的代谢物(如内源性大麻素(eCBs)),由微生物消化膳食成分(如短链脂肪酸(SCFAs))或转化宿主源性因子(如eCBs和胆汁酸)产生,可通过各种受体和途径被感知,从而改变肠道完整性和宿主健康。CB1, CB2,大麻素受体1型和2型;TRPV1,瞬时受体电位阳离子通道亚族V成员1;FXR,法尼类X受体;AhR,芳基烃受体;GPR119、GPR43、GPR41、g蛋白偶联受体119、43、41;MYD88,髓样分化初级反应88;PPARα/γ,过氧化物酶体增殖物激活受体α和γ;武田G蛋白偶联受体5;
除了众所周知的作用和作用机制外,一些SCFAs也可能发挥不同于以前所认为的功能。例如,丁酸盐被多次描述为结肠细胞增殖和维持肠道屏障的基本能量来源。然而,最近的证据表明,丁酸盐还通过与结肠细胞的通信强烈影响微生物环境。事实上,肠道腔内的充足氧气和逐渐向上皮细胞下降的浓度是厌氧菌保持在上皮细胞附近的关键条件,而不是兼任性厌氧菌,如肠杆菌科(变形菌门),已被证明会增加肠道炎症的风险(图3).80 81丁酸有助于通过激活线粒体中的β-氧化来控制结肠中的厌氧状态。通过激活结肠细胞中的核受体过氧化物酶体增殖物激活受体γ (PPARγ),丁酸盐限制了氧从结肠细胞扩散到管腔部分,从而维持厌氧条件。PPARγ的激活也抑制编码诱导型一氧化氮合酶的基因表达,从而减少NO的产生和最终的腔内硝酸盐水平,而硝酸盐是被推定为致病兼性厌氧菌(肠杆菌科)增殖的特定能量来源。图3).
类似的观察已经在患有严重肠道炎症的人身上进行,比如在IBD、癌症、肥胖和糖尿病期间,52 82 - 84检测到肠杆菌科的丰度增加。
引人注目的是,许多论文都指出,所有这些疾病都与产生SCFAs(主要是丙酸和丁酸)的细菌数量减少有关。85以细菌为例就是这样F. prausnitzii, A. muciniphilia而最近Dysosmobacter welbionis.86有一个特殊的例子Anaerostipes和Anaerobutyricum在乙酸存在的情况下,通过乙酰辅酶a途径从乳酸中生成丁酸的spp。87这些可以在小肠和结肠中形成营养链,在结肠中各种细菌产生乳酸。乳酸(一种不需要的酸)在肠道环境中的积累会导致胃肠道紊乱,这可能解释了丁酸原干预的一些好处答:soehngenii代谢综合征的研究对象。88年32
除了丙酸和丁酸,琥珀酸的影响也在研究中。琥珀酸盐是克雷布斯循环的中间产物,被认为是线粒体氧化磷酸化的底物,但也是细菌的代谢产物。在这种情况下,琥珀酸一直被忽略,因为它被认为主要是丙酸合成的关键中间体。目前,琥珀酸的作用在很大程度上仍是一个有争议的问题89由于已有报告显示琥珀酸与胰岛素抵抗、肥胖和炎症之间既有有益的也有相反的联系。90 - 93
Lipopolyscaccharides /其分子模式
肠道屏障是一个复杂而动态的物理和化学结构的集合,它监视着环境,保护宿主免受微生物入侵和有害刺激。这些来自环境的有害成分中的一些是所谓的病原体相关分子模式(PAMPs),其中细菌LPS是典型的一类。94
在革兰氏阴性菌细胞膜上发现的内毒素LPS是炎症反应的强力激活剂,即使少量的LPS释放到循环中也足以引起炎症反应。
LPS和其他pamp通过激活特定的模式识别受体(PRRs)来发挥它们的活性,PRRs可以感知微生物和感染因子,并发出防御性反应的信号。PRRs有四个主要的亚家族:toll样受体(TLRs),含有核苷酸结合寡聚结构域富含亮氨酸重复序列(LRR)的受体,视黄酸诱导基因1 (RIG-1)样受体(又名RIG-1样解旋酶)和c型凝集素受体。95在这些tlr受体中,一个在人类中包含10个成员(在小鼠中包含13个成员)的受体家族是最具特征的。每一种TLRs都介导对来自病原体的不同微生物成分的反应。两个典型的例子是TLR2,它能感知细菌脂蛋白,96以及识别细菌LPS的TLR4。97tlr加起来涵盖了两种外部刺激(pamp)的广泛范围。98和来自组织损伤的内部信号(损伤相关分子模式(DAMPs)) (图3和4).99这些配体有多种形式和大小:从核酸到脂类,从小化合物到大分子。TLRs广泛分布于免疫细胞中,包括巨噬细胞、中性粒细胞、树突状细胞、自然杀伤细胞、肥大细胞、嗜碱性粒细胞和嗜酸性粒细胞,99但也存在于其他身体细胞中,如肠上皮细胞。它们的激活诱导抗原递呈细胞激活,从而连接先天和适应性免疫反应,并刺激信号级联,试图抵御微生物入侵者或修复受损组织。虽然这种炎症反应是消除感染所必需的,但过度激活TLRs可导致免疫稳态的破坏,持续的促炎细胞因子和趋化因子的产生可增加炎症疾病和自身免疫性疾病的风险。这就是代谢性内毒素血症的情况,在这种情况下,高脂肪饮食和体重增加与较高的肠道通透性和随后全身(轻度)循环血浆LPS升高有关。One hundred.这导致一种低级别炎症状态,这是一系列慢性疾病的病理特征,包括T2D、NAFLD、慢性肾病和动脉粥样硬化。38 39 101 102有趣的是,来自不同类型细菌的LPS对肠道屏障功能、脂肪炎症、肠道葡萄糖吸收、血糖、胰岛素和肠促胰岛素有不同的影响,这表明代谢性内毒素血症水平对宿主代谢的净影响可能因肠道菌群组成的功能而不同。103
PRRs表达的中断与有利于炎症的菌群组成的改变有关。例如,由细菌鞭毛蛋白激活的TLR5缺乏的小鼠,会发生结肠炎或代谢综合征,这与微生物群的改变有关。104 105
下游信号通路的TLR激活依赖于髓系分化因子88蛋白(MyD88) (图4).MyD88是除TLR3外的所有TLRs的必需适配蛋白106肠道中MyD88的缺失在一定程度上防止了饮食诱导的肥胖、糖尿病和炎症,增加了抗炎内源性大麻素(eCBs),恢复了抗菌肽的产生,并在饮食诱导的肥胖期间增加了肠道调节性T细胞。107
尽管在我们完全了解PAMS/DAMPS、PRRs、微生物组和疾病状态如何相互作用之前,还有许多问题有待回答,但我们对这种复杂相互作用的日益加深的了解为炎症依赖性疾病提供了新的治疗可能性。
生物活性脂质
神经系统
在过去的二十年中,eCB系统因其广泛的生理作用而被广泛研究。在其多效作用中,eCB信号系统似乎在调节能量、葡萄糖和脂质代谢中发挥关键作用,但在免疫、炎症以及最近的微生物-宿主相互作用中也发挥关键作用。108,109
历史上,第一个内源性大麻素受体1型(CB1)被证实是由一种精神活性化合物激活的大麻,Δ9-tetrahydrocannabinol,110随后在1993年发现了第二种受体,大麻素受体2型(CB2).111这两种受体都是GPRs,具有共同的信号机制。112第一个确定的内源性激动剂是酰胺(N-arachidonoylethanolamide (AEA))。AEA是一大类生物活性脂类的关键成员之一N-acylethanolamine(美国)的家庭。113第二个关键配体是2-花生四烯醇甘油(2-AG)。114自从发现这两种主要化合物以来,eCB家族得到了扩展,不再局限于对CB具有特定活性的eCBs1和CB2受体。例如,一些ecb也与PPARα和PPARγ相互作用,以及与其他膜受体如GPR55或瞬时受体潜在的香草素1型(TRPV1)相互作用(图4).除了所谓的“真正的”ecb,也就是能够绑定CB的ecb1和CB2,许多其他结构类似于原型eCBs的化合物已被证明可以干扰eCB反应,而不直接激活CB1或CB2欧洲央行的受体。所有这些分子都被称为ecb样化合物或同源物,是生物活性脂类,包括其他NAEs或酰基甘油家族成员。115 116然而,类ecb化合物也可以发挥其自身的药理活性。例如,N-oleoylethanolamine (OEA)或N-棕榈酰乙醇胺(PEA)可激活PPARα、TRPV1和OEA,N-亚麻酰乙醇胺(LEA)和2-油酰甘油(2-OG)能够激活GPR119。117最近,研究表明1-棕榈酰甘油(1-PG)和2-棕榈酰甘油(2-PG)都是PPARα激动剂(图4).118
2010年,研究发现在参与调节肠道屏障功能的代谢系统中,eCB系统起着主要作用。108研究开始时发现,在肥胖和糖尿病期间,肠道eCB系统发生了改变,AEA的丰度增加,通过结肠肠炎触发肠道通透性1端依赖机制。108有趣的是,eCB系统音调的这种改变与肠道菌群的变化有关。此外,强效eCB激动剂对eCB系统的药理学激活增加了脂肪生成并破坏了肠道屏障。119在一系列独立研究中,肠道菌群、脂肪组织代谢和eCB系统之间的联系已被证实,因为遗传肥胖和糖尿病小鼠(ob / ob和db / db)表明他们的肠道菌群组成发生了深刻的变化,这与改变全身组织代谢和eCB系统色调有关。120 121总的来说,这些数据有力地支持了属于eCB系统的特定生物活性脂类与肠道菌群、脂肪组织和肠道功能的发展之间的联系。
为了进一步探索潜在的机制,并证明这些NAEs的合成是否可能参与代谢障碍的发生和肠道菌群的变化,已经生成了几个小鼠模型N-酰基磷脂酰乙醇胺水解特异性磷脂酶D (NAPE-PLD)是一种关键的合成酶,在脂肪细胞、肠上皮细胞和肝细胞中均被灭活。122 - 125
在正常热量饮食中,脂肪细胞缺乏NAPE-PLD的小鼠自发地发展为肥胖、胰岛素抵抗和炎症,并对高脂肪饮食诱导的代谢紊乱更敏感。122NAPE-PLD的脂肪细胞特异性缺失减少了脂肪组织中的产热程序(即褐变/褐变),导致了肠道菌群组成的深刻变化。此外,将脂肪组织NAPE-PLD缺失小鼠的微生物群转移到无菌受体小鼠,复制了整体表型,122这说明了肠道菌群的因果作用。当删除肠上皮细胞中的NAPE-PLD时,出现了不同的表型。小鼠在第一次接触高脂肪饮食时就开始暴饮暴食,然后发展为加重的饮食诱导的肥胖和肝脏脂肪变性。机制上,这归因于肠道到大脑轴的缺陷,因为发现了下丘脑Pomc神经元的改变,可能是由肠道和血浆ecb的变化解释的。值得注意的是,肠道菌群在这个模型中也受到影响,调节菌群可以部分恢复表型。123在最后一个模型中,在正常饮食下,肝细胞中缺失NAPE-PLD的小鼠出现了高脂肪饮食样表型(即脂肪量增加,肝脏脂肪变性,肝脏炎症)。这些影响与其他关键的生物活性脂类的变化有关,这些脂类已知会受到肠道菌群(如BAs)的影响。124总的来说,所有这些数据和动物模型都表明eCB系统通过NAPE-PLD,通过产生生物活性脂质与肠道菌群进行对话,而这种酶的任何失调都可能导致代谢并发症。
为了进一步探索肠道菌群与eCB系统调节之间的潜在联系,我们将无菌小鼠与常规小鼠在不同时间点的内源性大麻素组(eCBome)进行了比较。eCBome是eCB系统的延伸,包括超过50个受体和代谢酶,>20个具有重要功能的脂质介质。126发现了肠道eCBome基因表达和脂质介质水平的年龄依赖性修饰。引人注目的是,将对照组小鼠供体的粪便材料移植到年龄匹配的无菌小鼠,仅在1周后就逆转了这些改变。126总之,这组研究表明,肠道菌群直接影响宿主eCBome。
总之,所有的证据都指向宿主的eCB系统和肠道菌群之间的双向交流。然而,进一步的调查有必要解开这一关系的许多剩余的谜团。更复杂的是,最近有研究表明,肠道菌群本身能够产生特定的ecb。127这为探索宿主相互作用的菌群提供了新的机会,并为治疗提供了一些新的假定靶点。
胆汁酸
初级BAs,如人体内的胆酸(CA)和鹅脱氧胆酸(CDCA)(以及啮齿动物体内的鼠胆酸(MCA)),是肝脏中由胆固醇合成的两亲性分子。128在分泌到胆汁和储存在胆囊之前,它们可以与甘氨酸或牛磺酸结合。当食物被摄入时,BAs被释放到小肠,在那里它们帮助消化和吸收膳食脂肪。大约95%的肠内BAs在回肠被重新吸收,然后返回肝脏重新分泌。BAs的这种肠肝循环每天发生几次,是维持全身葡萄糖、脂质和能量稳态的重要生理机制,以防止高血糖、血脂异常和肥胖,并预防消化和心血管系统的炎症代谢疾病。129只有一小部分的BAs会逃脱这个高效的循环到达结肠。然后,这些BAs要么被被动地重新吸收到循环中,要么通过粪便排出体外。BAs的损失通过肝脏新生合成得到补偿,这是由人体内的成纤维细胞生长因子-19 (FGF19)在小肠中发出信号(FGF15在啮齿动物中)调节的。
尽管BAs的主要功能是调节胆固醇、甘油三酯和脂溶性维生素的消化和吸收,但最近已经认识到BAs还具有内分泌功能,因为它们作为信号分子。此外,BAs已被证明可以通过激活多个受体调节上皮细胞增殖、基因表达、脂质、葡萄糖和能量代谢。这些受体就是维生素D受体,130孕烷X受体,131本构雄烷受体,132法梨类X受体和G蛋白偶联胆汁酸受体-1(也称为武田G蛋白偶联受体5 (TGR5)) (图4).这些受体存在于许多组织中,包括肝脏、肠道、肌肉、棕色脂肪组织和中枢和外周神经系统,并介导信号级联,激活参与BA代谢、脂类和碳水化合物、能量消耗和炎症的基因表达。通过FXR和TGR5受体发出的信号也与PYY和GLP-1等GI激素的分泌有关(图3和4),被认为是维持能量和代谢稳态不可或缺的。BAs在控制葡萄糖、脂质和能量代谢中的作用已在前面进行了综述128 133 134因此在此不再详细讨论。
原发性BAs易受肠道微生物的修饰。这些修饰包括通过胆盐水解酶(BSH)活性去混溶(去除氨基酸残基)和通过去除羟基(去羟基化)、氧化(脱氢)或外酯化进一步代谢。135 136这导致了次生胆酸的形成,如脱氧胆酸、石胆酸和熊脱氧胆酸(在人类中是次生胆酸,但在啮齿动物中是初级胆酸)。这种细菌代谢改变了BAs的生物利用度和生物活性,从而影响了它们所参与的代谢反应。137由于其信号传递能力和BAs被肠道菌群化学转化的事实,因此可以认为BAs是微生物群衍生的信号代谢产物。有趣的是,当摄入食物后释放BAs,然后在肠道遇到不同的微生物群落时,有一个时空模式可识别。虽然BSH的活性可以由分布在许多系统发育不同的细菌分类中的各种各样的细菌进行,包括能够定植小肠的物种,138其他反应被认为更局限于居住在肠道末端的更特殊的细菌种类。因此,为了充分了解肠道菌群在宿主代谢中的作用,有必要研究能够转化BAs的不同细菌的参与。最近一项针对百岁老人的研究表明,他们特定的肠道菌群特征可能通过产生独特的继发性BAs,部分解释了他们对衰老相关疾病、慢性炎症和传染病的易感性降低。这意味着通过调节肠道菌群组成来控制BA池可能是一种对抗疾病的可行方法。139
芳基烃受体:与能量代谢、炎症和肠道微生物群有关
芳基烃受体(AhR)在脊椎动物细胞中广泛表达,该转录因子在配体结合后被激活。许多AhR配体存在,包括环境触发、营养来源信号、各种植物化学物质和细菌代谢物,如色氨酸(图2).AhR配体结合导致AhR转位进入细胞核,在那里它与二聚体分子AhR核转位器结合,导致许多参与免疫和炎症过程的基因的转录(图3).细菌产物和代谢物作为激活剂发挥着关键作用,因此过去几年的一些报告试图弄清AhR与肠道菌群(图3和4).48 140重要的是,这一AhR途径也与能量代谢和代谢综合征有关,因为在临床前和临床环境中,代谢综合征中色氨酸转化为AhR结合衍生物的能力都降低了。141这些作者表明,AhR配体的增加是通过给药a乳酸菌菌株改善了代谢功能,同时改善了肠道屏障,减少了肝脏脂肪变性。靛蓝,一种天然存在的AhR配体,具有强大的抗炎活性,保护对抗高脂肪饮食诱导的肥胖和代谢紊乱上调乳酸菌spp和关键屏障细胞因子白细胞介素(IL)-10和IL-22。142微生物色氨酸代谢物如吲哚-3-乙醇、吲哚-3-丙酮酸和吲哚-3-醛通过影响包括肌球蛋白IIA和ezrin在内的根尖连接复合体的完整性来保护肠道上皮屏障。143实验性酒精性肝病是一种肠道微生物群严重受损的疾病,144诱导AhR配体并给予6-甲酰基林多洛(3,2-b)咔唑(Ficz)可改善酒精性肝病。145Caspase招募域家族成员9−−/小鼠更容易患结肠炎,而且它们的微生物群不能将色氨酸代谢为相应的代谢物。146这种菌群转移到野生型小鼠会增加结肠炎,可以通过治疗改善乳酸菌提供大量AhR配体的菌株。AhR途径可能对其他炎症性胃肠道疾病也有重要意义,如腹腔疾病。147与非腹腔对照的受试者相比,患有活动性腹腔疾病的患者肠道中AhR配体的生成减少,而且在表达DQ8(一种只携带人类MHC II类DQ8的转基因小鼠)的非肥胖糖尿病小鼠中,使用高色氨酸饮食治疗这种Limosilactobacillus一种产生大量AhR配体的菌株或用AhR配体Ficz处理后,谷蛋白暴露后的肠道病理降低。147无菌小鼠表现出表皮屏障的分化和修复受损,角质形成细胞中缺乏AhR的小鼠对皮肤感染和屏障损伤非常敏感,用一组确定的细菌定植恢复了屏障。在这个模型中,肠道细菌可能在推定的肠道-皮肤轴中发挥何种作用还有待建立。148因此,AhR途径反映了微生物-上皮屏障-代谢和免疫功能界面的一个原型途径。
关键细菌及其特定分子
大多数信号代谢产物可以由大量不同的肠道细菌产生,因此特异性有限。然而,各种细菌可以制造特定的分子,与宿主有独特的相互作用(图2 - 4).由于显而易见的原因,这些已经在病原体中得到了很好的描述,病原体可以制造特定的毒素,合成多糖来躲避免疫系统,或诱导宿主合成受体,允许它们入侵。然而,最近的研究发现,在潜在的共生肠道细菌中发现了新的和独特的宿主信号分子。这些包括免疫调节多糖和鞘磷脂产生拟杆菌仕达屋优先计划149 150肽是由肠球菌spp。151
一类特殊的独特分子是由同一物种的一个或几个品系编码的蛋白质。其中一些已经被详细研究过,通常涉及到稳定的或翻译后修饰的蛋白质,这些蛋白质在被分泌或位于细胞包膜时具有与宿主受体相互作用的潜力。其中一些来自已经作为益生菌广泛销售的细菌,包括l .嗜酸的NCFM产生一个大的,可能是糖基化的表面层蛋白,向DC-SIGN受体发出信号,15290 kDa的毛状蛋白SpaC喂食GG是一种部分糖基化的黏液结合蛋白,对树突状细胞上的DC-SIGN受体具有不寻常的信号能力152 153以及在一些菌毛中发现的Tad蛋白质双歧杆菌属促进结肠持续和上皮细胞增殖的SPP。154 155最近研究的蛋白质是酪蛋白水解蛋白酶B (ClpB)大肠杆菌这是一种α -黑素细胞刺激激素的抗原模拟物,通过增加血浆GLP-1和PYY的产生来增加饱腹感。156ClpB蛋白是众所周知的兼职蛋白,被发现部分由多种细菌分泌,包括乳酸菌和双歧杆菌。然而,ClpB的特异性可能没有ClpB产生的那么高二氧化铪alvei在人体试验中也发现它能在一定程度上抑制饱腹感。157
考虑到活的和巴氏消毒的有效性答:muciniphila在一项原则性验证的人体试验中,43 118 158这并不奇怪,几个蛋白质从答:muciniphila最近被发现具有潜在的信号能力。最近的一种是一种名为P9的84 kDa蛋白(由Amuc_1831基因编码),口服给药后发现可诱导小鼠血清GLP-1。体外研究表明P9与细胞间粘附分子2受体相互作用。159 160另一种最近发现的蛋白质是答:muciniphilaAmuc_1434*蛋白通过肿瘤坏死因子相关凋亡诱导配体(TRAIL)介导的凋亡途径抑制LS174T细胞活力。161然而,这两种蛋白质都存在于许多细菌中答:muciniphila,两者都被注释为蛋白酶,表明具有酶活性,而且两者都没有在细胞外定位,这并不排除它们的活性需要细胞裂解的可能性。更重要的是,它们的稳定性没有被处理,这是巴氏杀菌的有趣之处答:muciniphila在人类和小鼠模型中,细胞和活细胞一样有效,甚至更有效。43 162 163所有这些论点都不适用于另一个论点答:muciniphila被发现可以向TLR2传递信号的蛋白(图4).163这就是30 kDa的Amuc_1100蛋白,它被定义为一种外膜蛋白,与Verrucomicrobia以外的其他细菌几乎没有同源性,实际上被认为是一种与菌毛相关的蛋白质。164进一步的研究表明,在小鼠模型中,Amuc_1100具有耐热性,并能预防饮食诱导的肥胖。163当比较这三个蛋白的绝对丰度时,很明显,Amuc_1100在蛋白质组中比其他两个信号候选者的丰度要高得多答:muciniphila种植在粘蛋白。165因此,未来的比较研究应该确定哪些蛋白质或它们的组合可以解释观察到的活性答:muciniphila在人类身上。
新发现的分子,对健康的影响及其靶标
除了经典分子如SCFAs, BAs或PAMPs和肠道肽(即GLP-1, PYY),都被描述为宿主代谢,肠道屏障和炎症的调节者,一类名为“肠合成酶”的新分子的作用正在显现。肠合成酶的概念最近被引入并定义为来自肠道的分子,有能力通过针对肠神经系统(ENS)调节十二指肠收缩。肠合成酶的化学成分多种多样,与激素、生物活性肽/脂类、营养物质、菌群和免疫因子有关。.166
这一概念的起源是基于对T2D受试者的观察,其特征是十二指肠高运动,有利于葡萄糖吸收,导致高血糖。166 167已经证明十二指肠收缩是由下丘脑感知的167 - 170在糖尿病期间十二指肠的高运动性会给大脑带来异常的传入神经信息。169 171相反,通过作用于ENS神经元恢复十二指肠的自然收缩,可以恢复肠-脑轴,提高胰岛素敏感性。166
肠道微生物群、大脑功能和葡萄糖代谢之间的联系正在成为这一研究领域的热门话题,ENS的作用成为治疗糖尿病等疾病的新靶点。尽管各种论文都在讨论调节肠道菌群的策略,如益生菌、益生元和粪便移植,以缓解代谢综合征的特征,但很少(如果不是没有的话)有肠道作用者的特征,如肠synes。
为了寻找参与葡萄糖代谢的新的肠道分子和受体,研究人员探索了已知的改变肠道菌群和改善糖尿病的特定纤维的作用。低聚果糖通过控制肠内神经元活性降低十二指肠收缩频率。这降低了糖尿病小鼠脂肪组织中的高血糖和炎症标记物。170通过脂质组学分析发现,这种低聚果糖饲料选择性地增加了结肠细胞中肠道生物活性脂质(12-羟基二十碳四烯酸(12-HETE))的丰度。引人注目的是,给糖尿病小鼠服用12-HETE能改善葡萄糖代谢。体外实验也证实了12-HETE的作用。此外,他们发现这种生物活性脂质作用于十二指肠收缩力的分子机制依赖于mu-阿片受体(MOR)(由脑啡肽激活)和PPARγ的存在。与健康受试者相比,糖尿病患者十二指肠中12-HETE水平降低,前脑啡肽和MOR表达降低,这一临床前发现得到了人类数据的支持。170
通过膳食补充剂的各种方法来治疗IBDs,发现了新的具有抗炎特性的生物活性脂类。172利用质谱分析大肠杆菌nisissle 1917 (EcN)是一种经过充分研究的菌株,作为治疗结肠炎的益生菌上市,它导致了3-羟基十八烯酸(C18-3OH)浓度增加的发现。他们发现口服C18-3OH可以减少结肠炎。为了确定存在于肠道菌群中的其他细菌是否产生C18-3OH,使用低聚果糖调节肠道菌群。作者发现,低聚果糖的抗炎特性与结肠C18-3OH浓度的增加有关。最后,他们发现了产生这种生物活性脂质的特定细菌,并发现C18-3OH通过激活PPARγ发挥作用。172
总之,这两个例子表明,肠道菌群是推定的许多生物活性化合物的来源(图2)作用于参与调节代谢和炎症的宿主受体(图3).
尽管有些代谢物是健康所需要的,但其他的可能是有害的,但证据只来自相关研究或动物试验。最近的研究发现了三种具有负面影响的代谢物,包括果糖赖氨酸,一种高级糖基化终产物(AGE),氧化三甲胺(TMAO)和丙酸咪唑(IMP)。
AGEs是在我们的食物中经过热处理形成的美拉德反应产物,当蛋白质和氨基酸的游离氨基与还原性碳水化合物发生反应,形成生物可利用性差的化合物。大量的机制证据表明AGEs与T2D和CRC相关,通过激活AGEs受体刺激促炎反应,173 174肠道通透性的增加——允许AGEs与结肠上皮更紧密的相互作用——以及由此导致的细菌毒素渗漏进入体循环。175果糖赖氨酸是由赖氨酸和葡萄糖形成的阿玛多里产物,是主要的膳食AGEs之一。早期的研究表明大肠杆菌具有呼吸果糖赖氨酸的能力。176然而,最近的分析表明,它可以转化为丁酸属成员Intestinimonas通过一种新的途径。70值得注意的是,果糖赖氨酸的降解能力只在配方奶喂养的婴儿中观察到,而没有在母乳喂养的婴儿中观察到,这可能与热处理后配方奶中该化合物的高含量有关。177应进一步研究果糖赖氨酸和其他AGEs在T2D和其他疾病中的因果关系以及肠道细菌参与它们的转化。最近的一项研究也描述了N-ε-羧甲基赖氨酸,另一种主要的AGE的完全利用Cloacibacillus和潜在的Oscillibacterspp。178
氧化三甲胺与甜菜碱、胆碱、左旋肉碱等季胺的摄入有关,这些胺常存在于蔬菜、水果、肉类和海鲜中,是众所周知的细菌渗透保护剂。179 180包括变形菌门在内的几种肠道细菌可以通过TMA裂解酶及其激活酶(CutCD)将这些季铵离子转化为乙醛和三甲胺(TMA)。然后TMA可以进入血液,并被肝脏中的黄素单加氧酶转化为TMAO。最近的研究表明,血清中的氧化三甲胺与动脉粥样硬化和心血管风险密切相关。181此外,在小鼠模型中,氧化三甲胺已被证明能促进动脉粥样硬化斑块的形成。182此外,氧化三甲胺是一种常见的尿毒症毒素。183因此,人们对了解这些季铵离子代谢为不导致TMA或其他TMAO前体的化合物的过程有相当大的兴趣。从生物化学和途径分析得到了新的见解真细菌limosum和它相关的肠道分离物大肠maltosivorans在一种涉及细菌细胞间室的新过程中,发现了甜菜碱和其他季胺的脱胺作用,并导致醋酸盐和丁酸盐的产生。184 - 186而后者是高度相关的,似乎有一种独特的维生素B12-依赖的代谢途径,这并不适用于可能导致IMP产生的组氨酸代谢。已有研究表明,T2D患者血清中IMP浓度升高。187最近研究发现,通过雷帕霉素复合物1依赖通路的哺乳动物靶点,肠道细菌从组氨酸中产生IMP,破坏胰岛素信号转导和糖耐量。188两个不相关的细菌,变形链球菌和Eggerthella lenta已经被确认为IMP的产生者,证实了许多代谢物是由几组肠道细菌产生的事实,这些细菌可能没有任何系统发育关系。总之,这些例子表明肠道细菌参与产生不需要的化合物,但也发现了新的厌氧菌,可以解毒这些化合物,甚至将它们转化为具有有利信号潜力的丁酸盐(图2和3).
总结与展望
在过去二十年中,已经取得了相当大的进展。从最初的临床观察到更机械的方法,肠道菌群和健康的领域正在演变为无可辩驳的因果关系。然而,仍然有许多研究声称有因果关系,而实际上只是证明了相关性。从相关性转向因果关系仍然是一个重要和必要的步骤,以更好地设计基于肠道菌群调节或使用特定活性化合物的假定干预措施。50 189由于大量的努力和组学分析的进步,科学界正在逐渐走向个性化医疗,微生物组学时代显然是未来医学和营养方法范式转变的重要组成部分。
伦理语句
病人同意发表
伦理批准
这项研究不涉及人类参与者。
参考文献
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
脚注
推特@matthias_vanhul, @MicrObesity
WMdV、HT、MVH和PDC贡献相同。
调整通知这篇文章在Online First发布后进行了修改。图3已放大。
贡献者PDC编写了一份关于稿件总体内容构想的建议。PDC、HT、WMdV、MVH对提案进行了修订、修改并通过。PDC、HT、WMdV和MVH对稿件内容进行了收集,选择了重点参考文献,并对稿件内容进行了撰写和批判性审查。PDC和MVH已经准备好数据。PDC、HT、WMdV、MVH都对最终稿进行了修改。PDC、HT、WMdV和MVH对本文的贡献相同。
资金PDC是FRS-FNRS (Fonds de la Recherche science fique)的研究主任,也是FNRS(研究项目PDR-convention: FNRS T.0030.21, CDR-convention: J.0027.22, FRFS-WELBIO: WELBIO-CR-2017C-02E, WELBIO-CR-2019C-02R, EOS:项目编号:FNRS;30770923和EOS项目号。40007505)。WMDV得到了荷兰科学研究组织SIAM引力基金(024.002.002)的支持。HT得到卓越倡议VASCage(促进老龄社区血管健康中心)的支持,这是一个研发k中心(COMET项目-优秀技术能力中心),由奥地利交通、创新和科技部、奥地利数字和经济事务部以及联邦州蒂罗尔、萨尔茨堡和维也纳资助。
相互竞争的利益PDC和WMdV是专利申请的发明者,处理使用Akkermansia muciniphila以及它在代谢紊乱治疗中的作用。PDC和WMdV是A-Mansia Biotech的联合创始人。PDC是Enterosys的联合创始人。WMdV是Caelus Health的联合创始人和专利发明人真细菌hallii.
来源和同行评审委托;内部同行评议。